Clear Sky Science · es
Dinámica de la cromatina en el locus Klf4 de células pluripotentes de ratón
Cómo se mueve el ADN dentro de las células vivas
En el interior de cada una de nuestras células, largas hebras de ADN se pliegan y retuercen formando una estructura compacta llamada cromatina. Cómo se contonea y desplaza esta cromatina por el núcleo importa, porque fragmentos de ADN distantes necesitan a menudo encontrarse para activar o desactivar genes. Este estudio investiga si activar un gen cambia realmente cómo se mueve su tramo de ADN, usando como caso de prueba Klf4, un gen clave de células madre, en células de ratón vivas.
Observando un vecindario genético individual
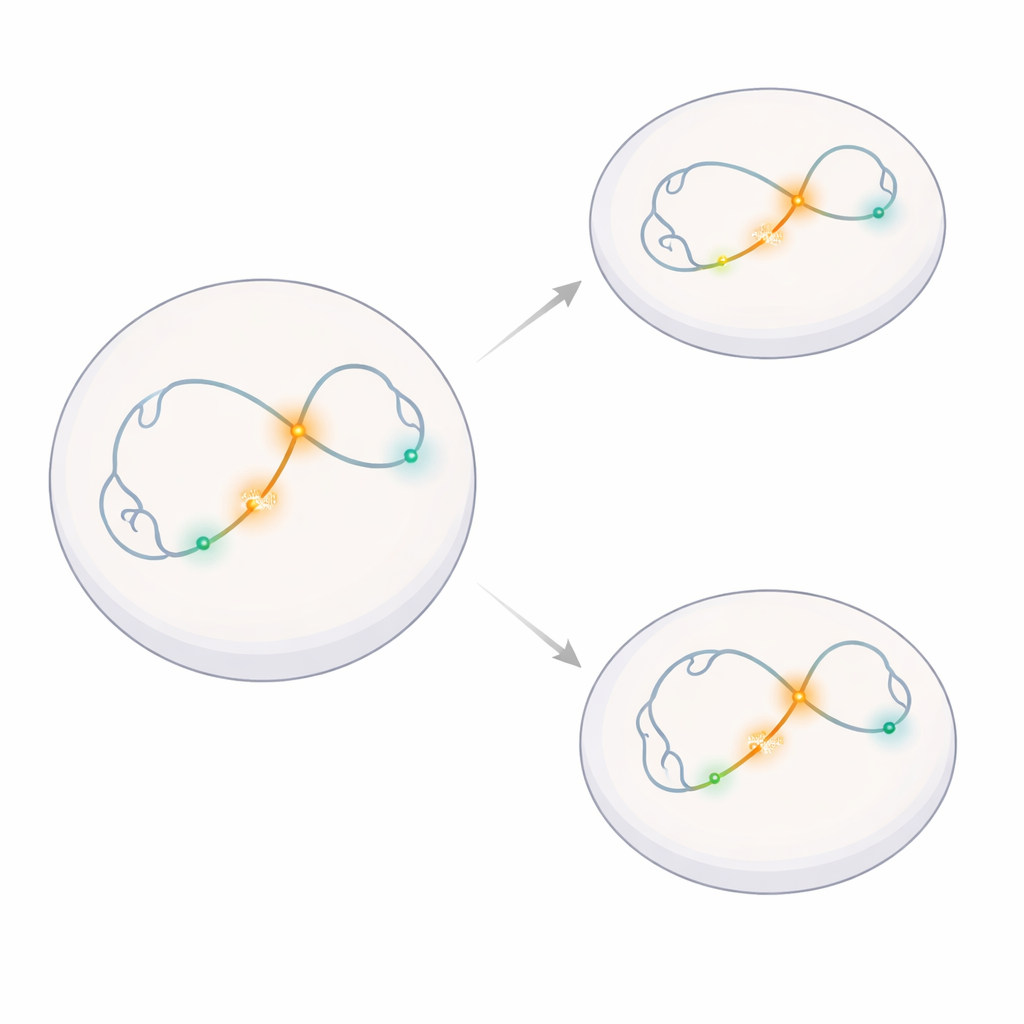
Los investigadores se centraron en una pequeña región del genoma que contiene Klf4, un gen importante para mantener a las células madre en un estado flexible y temprano, y su vecino próximo Rad23b, un gen de “mantenimiento” rutinario. Modificaron células madre embrionarias de ratón para que pequeñas etiquetas fluorescentes se fijaran en cinco puntos elegidos a lo largo de este vecindario: el principal centro regulador de Klf4 (un superenhancer), el sitio de inicio del gen Klf4, el sitio de inicio del gen Rad23b y dos tramos cercanos de ADN que no regulan activamente genes. Esto les permitió seguir el movimiento de esos puntos exactos en células vivas a lo largo del tiempo mediante microscopía de alta velocidad.
Apagar un gen sin cambiar su baile
Para evaluar si la actividad génica afecta el movimiento, el equipo utilizó una transición bien conocida en células madre. En células madre embrionarias “naïve”, Klf4 está fuertemente activo y ayuda a mantener su capacidad de convertirse en muchos tipos celulares. Cuando estas células se inducen a convertirse en células tipo epiblasto—un estado más avanzado—el superenhancer principal se silencia químicamente y la expresión de Klf4 cae bruscamente. Los científicos confirmaron que este cambio genético ocurría como se esperaba, mientras que Rad23b permaneció activo en ambos estados celulares, y que la inserción de su sistema de etiquetado fluorescente no alteró de forma medible la actividad génica normal.
Midiendo la sutil deriva del ADN
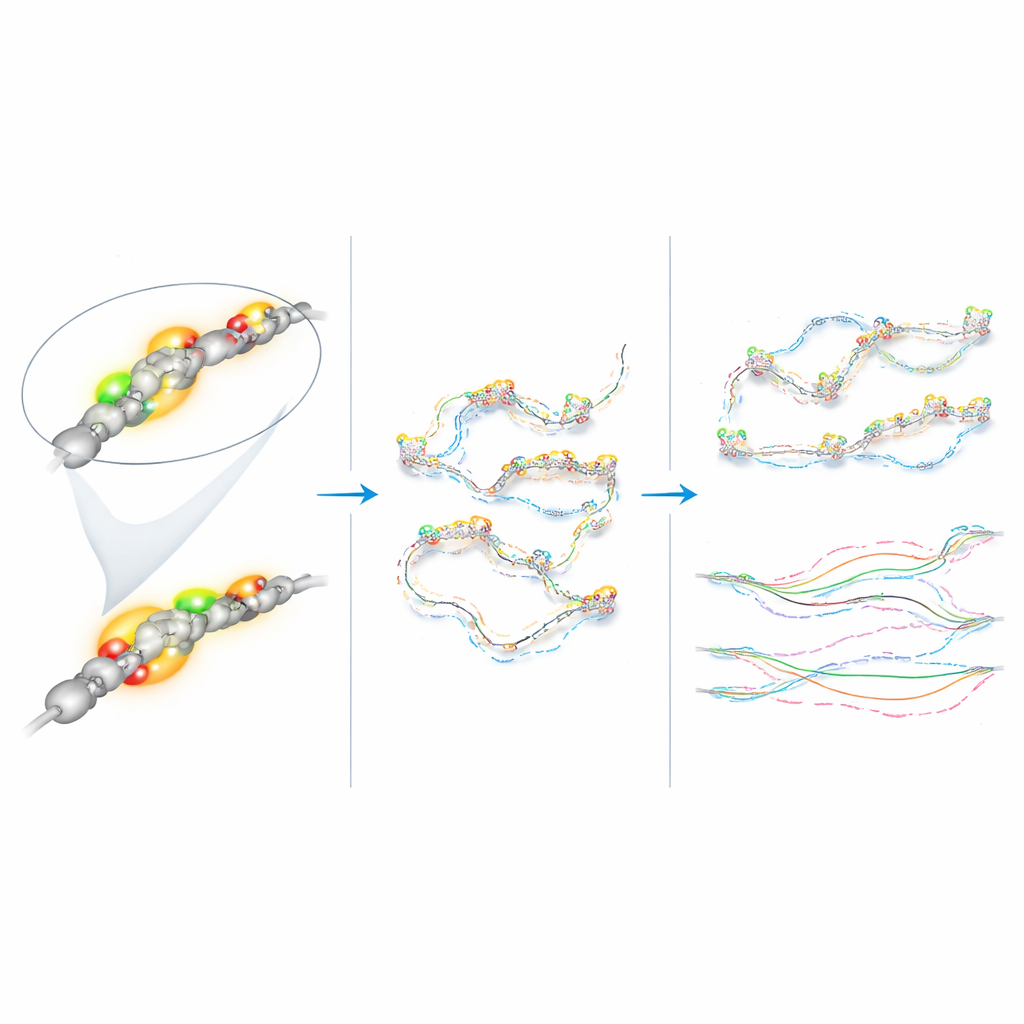
Usando software de seguimiento automatizado y análisis personalizado, los investigadores convirtieron las posiciones cambiantes de cada punto fluorescente en medidas cuantitativas de movimiento. Las cinco regiones etiquetadas se movieron de forma “subdifusiva”: en lugar de vagar libremente como humo en el aire, sus trayectorias estaban restringidas, como si se desplazaran por un entorno elástico y saturado. De forma crucial, el superenhancer y el promotor de Klf4 no se movieron de modo distinto a las dos regiones de control cercanas, y su movimiento fue esencialmente el mismo tanto cuando Klf4 estaba activo en células naïve como cuando estaba mayormente apagado en células tipo epiblasto. Esto cuestiona la idea de que la transcripción—el acto de leer un gen en ARN—automáticamente aprieta o relaja cómo se mueve ese tramo de ADN.
Un vecino que se mueve rápido
Surgió una excepción notable. El promotor del gen de mantenimiento vecino Rad23b mostró de forma consistente un movimiento más rápido que todos los puntos de vista de Klf4 en ambos estados celulares. Incluso dentro de un segmento relativamente pequeño del genoma, fragmentos de ADN separados por apenas cientos de miles de pares de bases pudieron moverse de forma bastante diferente. Los autores también detectaron cambios sutiles en el movimiento de una de las regiones de control a medida que las células maduraban, lo que sugiere que cambios más amplios en el panorama de la cromatina—no solo el estado encendido/apagado de genes individuales—pueden alterar cómo deriva el ADN dentro del núcleo.
Qué significa esto para el control génico
Juntando estas observaciones, el estudio sugiere que simplemente activar o desactivar un gen no reconfigura necesariamente de forma importante los movimientos locales de su ADN. Para la región de Klf4, la transcripción activa no hizo que sus elementos de control clave se volvieran claramente más confinados ni más móviles que tramos de cromatina cercanos. En cambio, el movimiento de la cromatina parece depender de una mezcla de contexto local, organización cromosómica más amplia y las propiedades particulares de genes individuales como Rad23b. Para el lector, la conclusión es que la regulación génica no consiste solo en accionar interruptores; también depende de cómo los trozos de ADN vagan y se encuentran entre sí, y ese vagar puede ser sorprendentemente estable incluso cuando la actividad génica cambia.
Cita: van Staalduinen, J., Kabbech, H., Yavuz, S. et al. Chromatin dynamics of the Klf4 locus in mouse pluripotent cells. Sci Rep 16, 10941 (2026). https://doi.org/10.1038/s41598-026-45230-9
Palabras clave: dinámica de la cromatina, regulación génica, células madre, Klf4, imagen celular en vivo