Clear Sky Science · de
Chromatin-Dynamik des Klf4-Locus in pluripotenten Mauszellen
Wie sich DNA innerhalb lebender Zellen bewegt
Tief in jeder unserer Zellen falten und verdrehen sich lange DNA-Stränge zu einer kompakten Form, dem Chromatin. Wie dieses Chromatin im Zellkern zittert und driftet, ist wichtig, weil entfernte DNA-Stücke sich oft begegnen müssen, um Gene ein- oder auszuschalten. Diese Studie untersucht, ob das Anschalten eines Gens tatsächlich die Bewegungen des entsprechenden DNA-Abschnitts verändert, und zwar am Beispiel des wichtigen Stammzellgens Klf4 in lebenden Mauszellen.
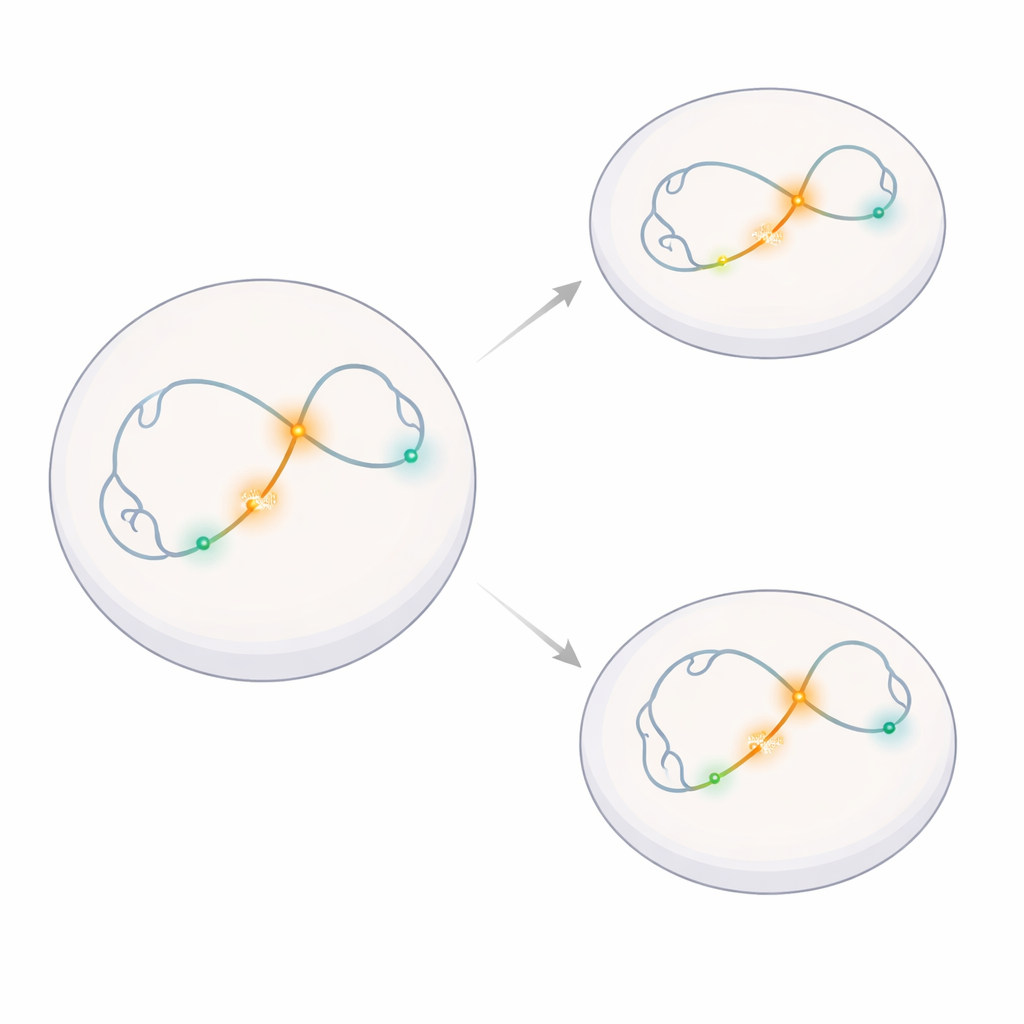
Eine einzelne Gen-Nachbarschaft beobachten
Die Forschenden konzentrierten sich auf eine kleine Genomregion, die Klf4 enthält — ein Gen, das wichtig ist, um Stammzellen in einem flexiblen, frühen Zustand zu halten — sowie auf seinen Nachbarn Rad23b, ein routinemäßiges „Housekeeping“-Gen. Sie konstruierten maussembryonale Stammzellen so, dass winzige fluoreszierende Markierungen an fünf ausgewählten Stellen dieser DNA-Nachbarschaft anhafteten: am Hauptkontrollzentrum von Klf4 (einem Superenhancer), am Transkriptionsstartpunkt von Klf4, am Transkriptionsstartpunkt von Rad23b und an zwei benachbarten DNA-Abschnitten, die nicht aktiv Gene regulieren. So konnten sie die Bewegung dieser exakt definierten Punkte in lebenden Zellen über die Zeit mit Hochgeschwindigkeitsmikroskopie verfolgen.
Ein Gen ausschalten, ohne seinen Tanz zu verändern
Um zu prüfen, ob Genaktivität die Bewegung beeinflusst, nutzte das Team einen bekannten Übergang in Stammzellen. In „naiven“ embryonalen Stammzellen ist Klf4 stark aktiv und trägt zur Erhaltung ihrer Vielseitigkeit bei. Wenn diese Zellen in einen epiblastähnlichen Zustand — einen fortgeschritteneren Zustand — gebracht werden, wird der Hauptenhancer chemisch stillgelegt und die Klf4-Expression fällt stark ab. Die Wissenschaftler bestätigten, dass dieser genetische Schalter wie erwartet eintrat, während Rad23b in beiden Zellzuständen aktiv blieb, und dass das Einfügen ihres fluoreszierenden Markierungssystems die normale Genaktivität nicht messbar störte.
Das subtile Driften der DNA messen
Mithilfe automatisierter Tracking-Software und maßgeschneiderter Analyse konvertierten die Forschenden die sich ändernden Positionen jeder fluoreszierenden Markierung in quantitative Bewegungsgrößen. Alle fünf markierten Regionen bewegten sich auf „subdiffusive“ Weise: Anstatt frei wie Rauch in Luft umherzuschweifen, waren ihre Bahnen eingeschränkt, als würden sie sich durch eine überfüllte, elastische Umgebung bewegen. Entscheidend war, dass sich der Klf4-Superenhancer und der Promotor nicht anders bewegten als die beiden nahegelegenen Kontrollregionen, und ihre Bewegung sah im Wesentlichen gleich aus, egal ob Klf4 in naiven Zellen aktiv war oder in epiblastähnlichen Zellen weitgehend abgeschaltet war. Das stellt die Vorstellung infrage, dass die Transkription — das Ablesen eines Gens in RNA — automatisch die Beweglichkeit dieses DNA-Abschnitts deutlich einschränkt oder lockert.
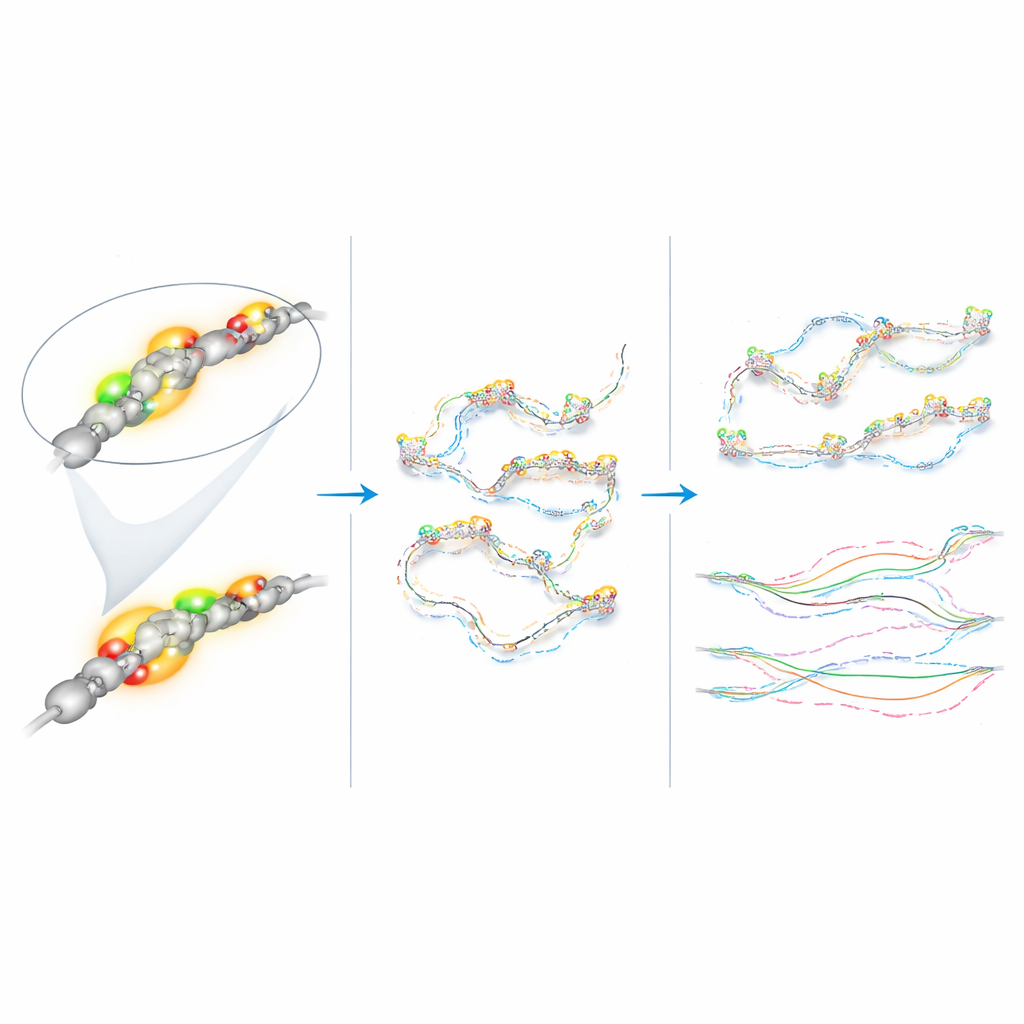
Ein schnell bewegter Nachbar
Eine Ausnahme stach hervor. Der Promotor des benachbarten Housekeeping-Gens Rad23b zeigte durchgehend stärkere Bewegungen als alle Klf4-Sichtpunkte in beiden Zellzuständen. Selbst innerhalb eines relativ kleinen Genomsegments konnten DNA-Abschnitte, die nur Hunderttausende Basen voneinander entfernt liegen, sich ganz unterschiedlich bewegen. Die Autor:innen detektierten auch subtile Bewegungsänderungen für eine der Kontrollregionen während der Zellreifung, was darauf hindeutet, dass breit angelegte Verschiebungen in der Chromatin-Landschaft — nicht nur der Ein‑/Aus‑Zustand einzelner Gene — die Art und Weise verändern können, wie DNA im Zellkern driftet.
Was das für die Gensteuerung bedeutet
Setzt man diese Beobachtungen zusammen, legt die Studie nahe, dass das einfache Ein- oder Ausschalten eines Gens nicht zwangsläufig die lokalen Bewegungen seiner DNA stark umgestaltet. Für die Klf4-Region führte aktive Transkription nicht dazu, dass ihre zentralen Kontrollelemente deutlich stärker eingeschränkt oder beweglicher waren als benachbarte Chromatinabschnitte. Stattdessen scheint die Chromatinbewegung von einer Mischung aus lokalem Kontext, übergeordneter Chromosomenorganisation und den besonderen Eigenschaften einzelner Gene wie Rad23b abzuhängen. Die Kernaussage für die Leserschaft lautet: Genregulation ist nicht nur das Umlegen von Schaltern; sie hängt auch davon ab, wie DNA‑Stücke umherwandern und aufeinandertreffen — und dieses Wandern kann überraschend stabil sein, selbst wenn sich die Aktivität der Gene ändert.
Zitation: van Staalduinen, J., Kabbech, H., Yavuz, S. et al. Chromatin dynamics of the Klf4 locus in mouse pluripotent cells. Sci Rep 16, 10941 (2026). https://doi.org/10.1038/s41598-026-45230-9
Schlüsselwörter: Chromatin-Dynamik, Genregulation, Stammzellen, Klf4, Lebendzellbildgebung