Clear Sky Science · fr
Le raloxifène détend l’aorte du rat via un mécanisme dépendant des mitochondries
Pourquoi il est important de garder les vaisseaux sanguins souples
Avec l’âge, nos vaisseaux sanguins peuvent devenir plus raides et plus susceptibles de se rétrécir, augmentant le risque d’hypertension, d’infarctus et d’accidents vasculaires cérébraux. De nombreuses femmes prennent le raloxifène pour protéger leurs os après la ménopause, et les cliniciens ont remarqué qu’il semble aussi bénéficier au cœur et aux vaisseaux. Cette étude pose une question simple mais importante : comment, précisément, le raloxifène favorise-t-il la relaxation vasculaire ? La réponse implique les minuscules « centrales » des cellules — les mitochondries — et les molécules réactives qu’elles produisent.
Un médicament osseux aux bénéfices cardiovasculaires discrets
Le raloxifène est surtout connu comme traitement préventif de l’ostéoporose et pour réduire le risque de certains cancers du sein et de l’utérus chez les femmes ménopausées. Il agit sur les récepteurs aux œstrogènes de manière spécifique aux tissus, bloquant l’action des œstrogènes dans certains organes tout en l’imitant dans d’autres. Des travaux antérieurs ont montré que le raloxifène peut abaisser la pression artérielle chez des rats hypertendus et détendre artères et veines chez plusieurs espèces. On avait proposé des explications telles qu’une augmentation de l’oxyde nitrique, un blocage de l’entrée du calcium dans les cellules musculaires ou une réduction de l’inflammation. Cependant, ces hypothèses n’expliquaient pas complètement comment le médicament élargit les vaisseaux, notamment à court terme.
Tester la réponse des artères de rat
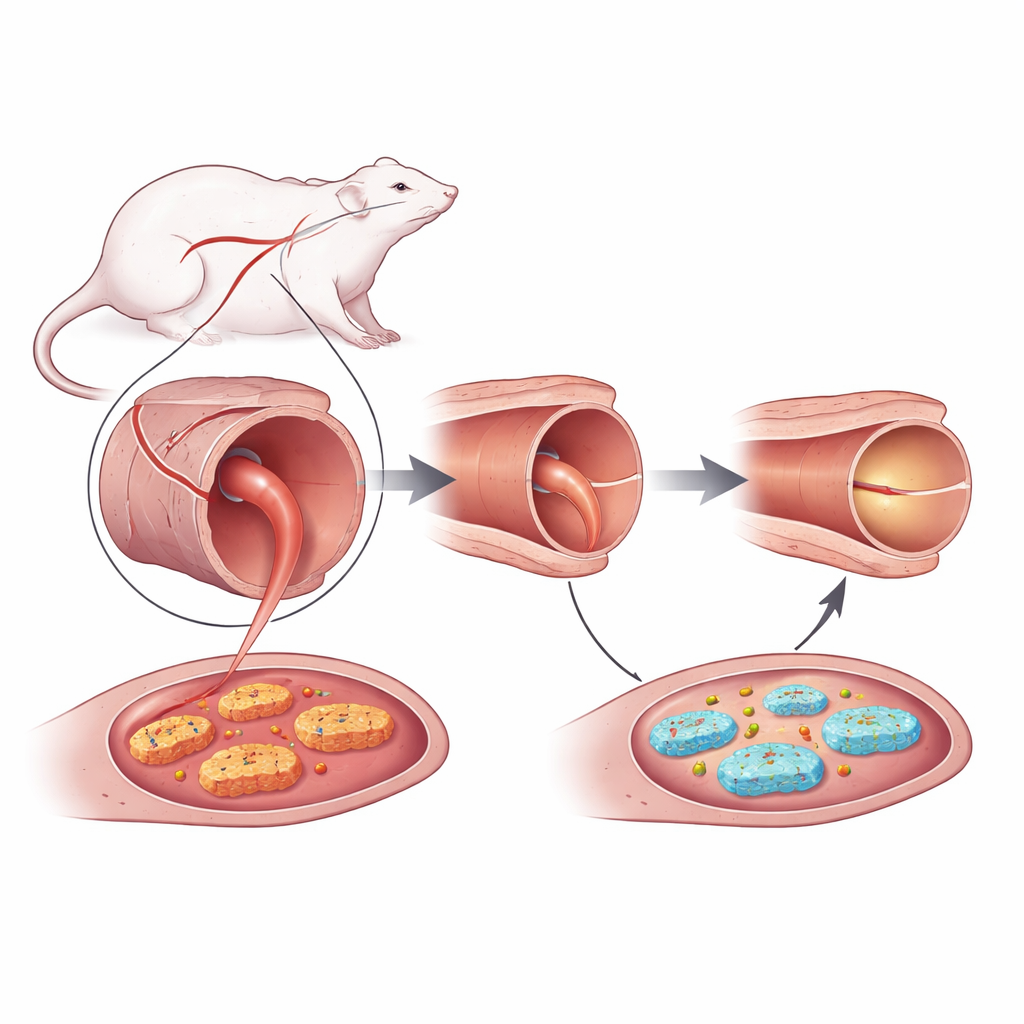
Les chercheurs se sont concentrés sur l’aorte, l’artère principale de l’organisme, prélevée chez des rats mâles, et ont étudié de petits anneaux de ce vaisseau en laboratoire. Ils ont d’abord contracté les anneaux avec de la phényléphrine, un composé qui provoque la constriction vasculaire. Puis ils ont ajouté des concentrations croissantes de raloxifène et mesuré la diminution de la tension dans les anneaux. L’ablation de la fine couche interne du vaisseau — l’endothélium — a réduit, sans éliminer, l’effet relaxant du raloxifène. Le blocage des prostaglandines (avec l’indométhacine) ou des récepteurs aux œstrogènes a eu peu d’impact. Cela montre que, si l’endothélium contribue, l’action principale relaxante du raloxifène ne dépend pas du signalement œstrogénique classique ni de messagers hormonaux courants.
Zoom sur les centrales énergétiques cellulaires
L’attention s’est alors portée sur les espèces réactives de l’oxygène — formes d’oxygène de courte durée de vie et chimiquement actives souvent qualifiées de « stress oxydatif ». Ces molécules sont produites par plusieurs systèmes enzymatiques, y compris un complexe membranaire (la NADPH oxydase) et la chaîne respiratoire mitochondriale. Dans des artères dépourvues d’endothélium, l’équipe a utilisé des médicaments qui atténuent les espèces réactives issues de différentes sources. Le blocage de la NADPH oxydase n’a que modestement affaibli la contraction induite par la phényléphrine, tandis que viser les mitochondries avec la roténone ou un antioxydant ciblant les mitochondries réduisait clairement la constriction. Lorsqu’ils ont combiné ces approches avec le raloxifène, ils ont constaté que perturber la machinerie mitochondriale diminuait fortement la capacité du raloxifène à relaxer le vaisseau, désignant les espèces réactives mitochondriales comme un acteur central.
Comment les cellules calment leurs étincelles internes
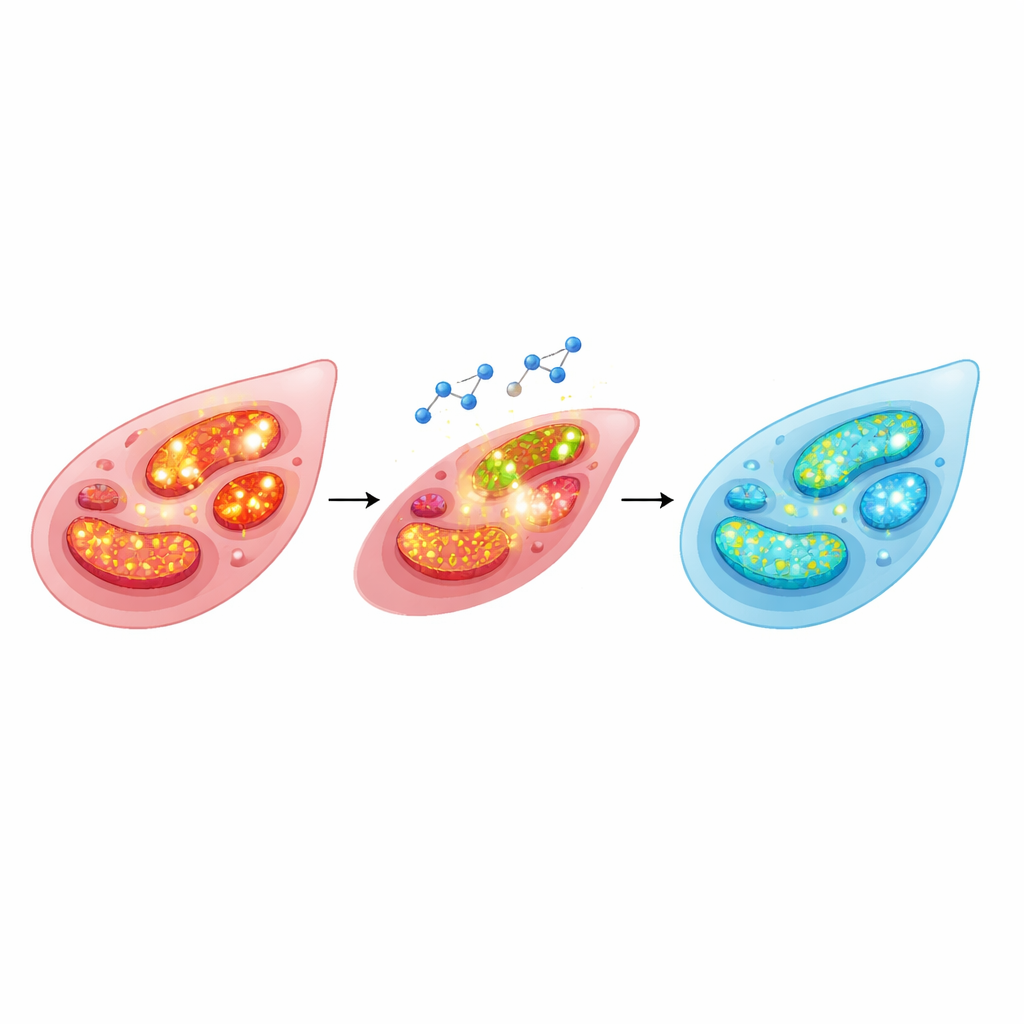
Pour voir ce qui se passe à l’intérieur des cellules musculaires lisses vasculaires, celles qui contractent réellement l’artère, les scientifiques ont utilisé des sondes fluorescentes qui s’allument en présence d’espèces réactives de l’oxygène ou lorsque le potentiel mitochondrial est élevé. La phényléphrine a provoqué une hausse à la fois des espèces réactives totales et mitochondriales, et a augmenté le potentiel de membrane mitochondrial — signes que les centrales cellulaires fonctionnaient dans un mode surchargé et générateur de stress. Le raloxifène a inversé ces changements, faisant revenir à la baisse à la fois les niveaux d’espèces réactives et le potentiel mitochondrial. L’équipe a aussi examiné une protéine appelée UCP2, qui agit comme un « frein » intégré en laissant fuir légèrement le gradient énergétique à travers la membrane mitochondriale et en limitant ainsi la production d’espèces réactives. La phényléphrine diminuait les niveaux d’UCP2, mais le prétraitement au raloxifène les préservait, contribuant à stabiliser l’environnement mitochondrial.
Ce que cela signifie pour les traitements futurs
Globalement, l’étude montre que le raloxifène aide les artères de rat à se détendre en réduisant en grande partie les signaux de stress provenant des mitochondries de la paroi vasculaire. En maintenant l’activité d’UCP2 et en assouplissant modestement le gradient énergétique mitochondrial, le raloxifène diminue l’accumulation d’espèces réactives nocives qui favorisent autrement la constriction et les dommages vasculaires. Pour le grand public, le message clé est qu’un médicament déjà utilisé pour protéger les os pourrait aussi protéger les vaisseaux en calmant les « étincelles » à l’intérieur des centrales cellulaires. Cette voie mitochondriale pourrait devenir une cible pour de nouveaux traitements visant à prévenir ou atténuer les maladies vasculaires liées au stress oxydatif.
Citation: Ji, KD., Song, B., Shen, WL. et al. Raloxifene relaxes the rat aorta via a mitochondria-dependent mechanism. Sci Rep 16, 14175 (2026). https://doi.org/10.1038/s41598-026-44551-z
Mots-clés: raloxifène, mitochondries, espèces réactives de l’oxygène, relaxation vasculaire, UCP2