Clear Sky Science · de
Raloxifen entspannt die Rataorta über einen mitochondrienabhängigen Mechanismus
Warum es wichtig ist, Blutgefäße flexibel zu halten
Mit zunehmendem Alter können unsere Blutgefäße steifer werden und leichter verengen, wodurch das Risiko für Bluthochdruck, Herzinfarkte und Schlaganfälle steigt. Viele Frauen nehmen das Medikament Raloxifen zur Knochenschutz nach den Wechseljahren ein, und Ärztinnen und Ärzte haben beobachtet, dass es auch Herz und Gefäße zu nützen scheint. Diese Studie stellt eine einfache, aber wichtige Frage: Wie genau fördert Raloxifen die Entspannung von Blutgefäßen? Die Antwort betrifft die winzigen „Kraftwerke“ in den Zellen — die Mitochondrien — und die reaktiven Moleküle, die sie produzieren.
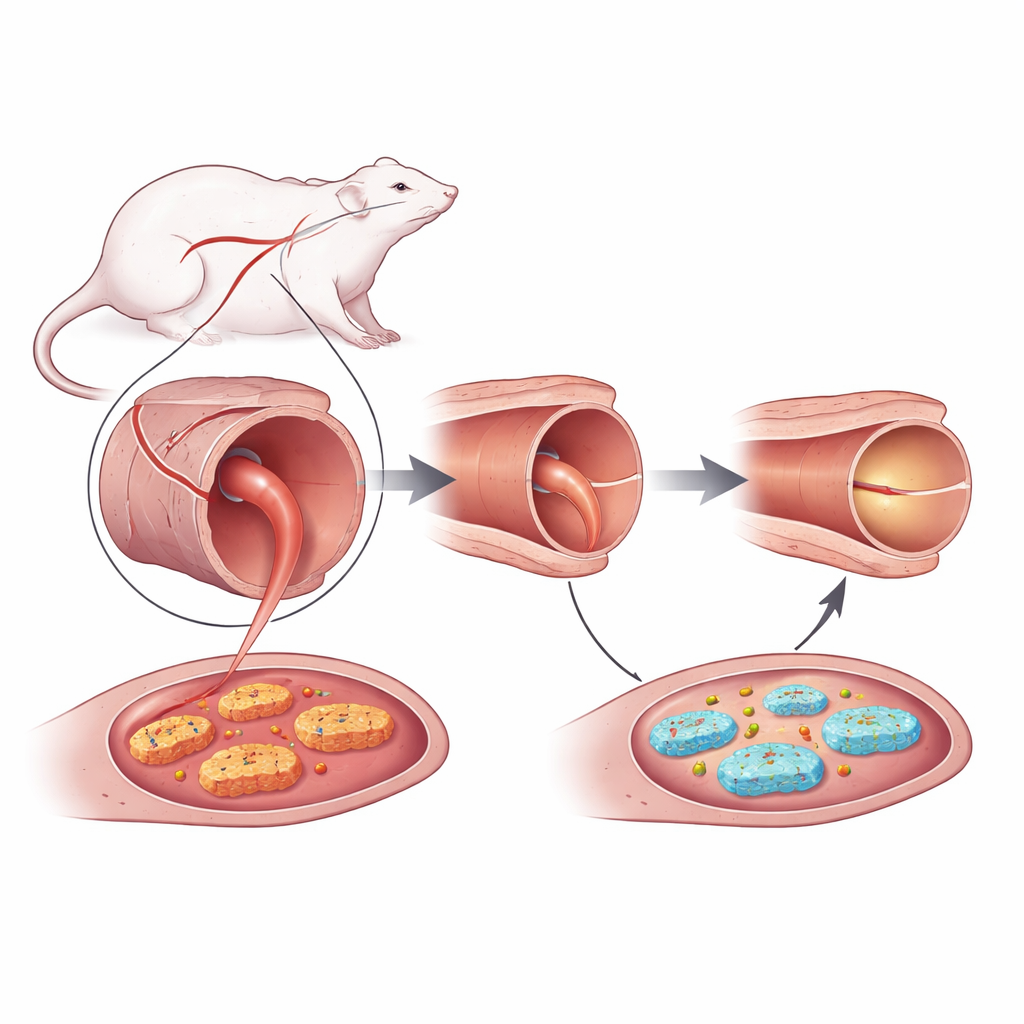
Ein Knochensmittel mit verstecktem Herzvorteil
Raloxifen ist vor allem als Behandlung zur Vorbeugung von Osteoporose und zur Senkung des Risikos bestimmter Brust- und Gebärmutterkrebserkrankungen bei postmenopausalen Frauen bekannt. Es wirkt auf Östrogenrezeptoren gewebespezifisch, indem es in einigen Organen die Wirkung von Östrogen blockiert und in anderen imitiert. Frühere Arbeiten zeigten, dass Raloxifen den Blutdruck bei hypertensiven Ratten senken und Arterien und Venen bei mehreren Arten entspannen kann. Vorgeschlagene Erklärungen umfassten eine Verstärkung von Stickstoffmonoxid, die Blockade von Kalziumeinstrom in Muskelzellen und die Abschwächung von Entzündungen. Diese Ideen erklärten jedoch nicht vollständig, wie das Medikament kurzfristig die Gefäßweite vergrößert.
Untersuchung der Reaktion von Rattenarterien
Die Forschenden konzentrierten sich auf die Hauptkörperarterie (Aorta) männlicher Ratten und untersuchten kleine Ringsegmente dieses Gefäßes im Labor. Zuerst spannten sie die Ringe mit Phenylephrin, einer Verbindung, die Gefäße verengt. Dann gaben sie zunehmend höhere Mengen Raloxifens zu und maßen, wie stark die Spannung in den Ringen abnahm. Das Entfernen der empfindlichen inneren Auskleidung des Gefäßes — des Endothels — verringerte, aber beseitigte nicht den entspannenden Effekt von Raloxifen. Die Blockade von Prostaglandinen (mit Indomethacin) oder von Östrogenrezeptoren machte wenig Unterschied. Das zeigte, dass die Gefäßauskleidung zwar beiträgt, die Hauptwirkung von Raloxifen auf Entspannung aber nicht auf klassischer Östrogensignalgebung oder üblichen hormonähnlichen Botenstoffen beruht.
Scheinwerfer auf die zellulären Kraftwerke
Der Blick richtete sich dann auf reaktive Sauerstoffspezies — kurzlebige, chemisch aktive Formen von Sauerstoff, oft als „oxidativer Stress“ beschrieben. Diese Moleküle entstehen in mehreren Enzymsystemen, darunter ein Membran-Enzymkomplex (NADPH-Oxidase) und die mitochondriale Elektronentransportkette. In entkleideten Arterien verwendete das Team Wirkstoffe, die reaktive Sauerstoffspezies aus verschiedenen Quellen reduzieren. Die Blockade der NADPH-Oxidase schwächte die Phenylephrin-induzierte Verengung nur geringfügig, während das Anvisieren der Mitochondrien mit Rotenon oder einem mitochondrienfokussierten Antioxidans die Kontraktion deutlich verringerte. Kombiniert man diese Ansätze mit Raloxifen, zeigte sich, dass das Eingreifen in die mitochondriale Maschinerie Raloxifens Fähigkeit zur Gefäßentspannung stark abschwächt — ein Hinweis darauf, dass mitochondriale reaktive Sauerstoffspezies eine zentrale Rolle spielen.
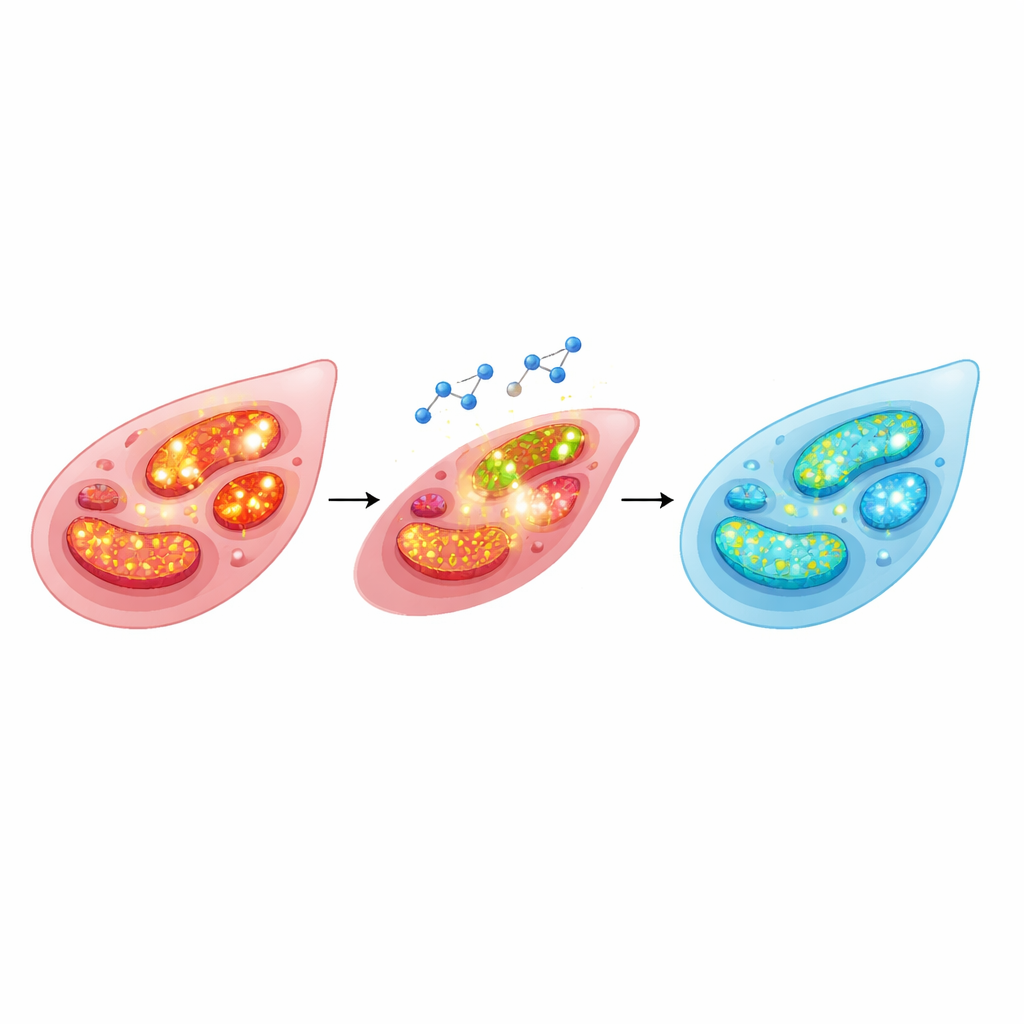
Wie Zellen ihre inneren Funken beruhigen
Um zu sehen, was in einzelnen vaskulären Glattmuskelzellen — den Zellen, die die Arterie tatsächlich zusammenziehen — passiert, verwendeten die Wissenschaftler fluoreszierende Farbstoffe, die bei Anwesenheit reaktiver Sauerstoffspezies oder bei hoher mitochondrialer Spannung aufleuchten. Phenylephrin verursachte einen Anstieg sowohl der gesamten als auch der mitochondrialen reaktiven Sauerstoffspezies und erhöhte das mitochondriale Membranpotenzial — Zeichen dafür, dass die zellulären Kraftwerke im Überladungsmodus arbeiteten und Stress erzeugten. Raloxifen kehrte diese Veränderungen um und senkte sowohl die Reaktiv-Oxid-Spezies-Level als auch das mitochondriale Potenzial wieder. Das Team untersuchte außerdem ein Protein namens UCP2, das als eingebautes „Bremssystem“ wirkt, indem es den Energiegradienten über die mitochondriale Membran leicht ableitet und so die Produktion reaktiver Sauerstoffspezies begrenzt. Phenylephrin senkte die UCP2-Spiegel, während eine Raloxifen-Vorbehandlung sie erhielt und so zur Stabilität der mitochondrialen Umgebung beitrug.
Was das für künftige Therapien bedeutet
Insgesamt zeigt die Studie, dass Raloxifen Rattenarterien weitgehend dadurch entspannt, dass es Stresssignale aus den Mitochondrien der Gefäßwand abschwächt. Indem es die Aktivität von UCP2 erhält und den mitochondrialen Energiegradienten moderat lockert, verringert Raloxifen die Anhäufung schädlicher reaktiver Sauerstoffspezies, die sonst Gefäßverengung und Schäden fördern würden. Für Laien lautet die zentrale Botschaft: Ein bereits zur Knochenprotektion eingesetztes Medikament könnte auch Blutgefäße schützen, indem es die ‚Funken‘ in den zellulären Kraftwerken beruhigt. Dieser mitochondriale Weg könnte ein Ziel für neue Behandlungen werden, die darauf abzielen, vaskuläre Erkrankungen zu verhindern oder zu lindern, die durch oxidativen Stress getrieben sind.
Zitation: Ji, KD., Song, B., Shen, WL. et al. Raloxifene relaxes the rat aorta via a mitochondria-dependent mechanism. Sci Rep 16, 14175 (2026). https://doi.org/10.1038/s41598-026-44551-z
Schlüsselwörter: raloxifen, Mitochondrien, reaktive Sauerstoffspezies, vaskuläre Relaxation, UCP2