Clear Sky Science · fr
Le polymorphisme FOXE1 rs965513 : un locus de risque pléiotrope associé à la fonction thyroïdienne, à la mutation BRAFV600E et à la susceptibilité au carcinome papillaire de la thyroïde
Pourquoi votre thyroïde et vos gènes comptent
Le carcinome papillaire de la thyroïde est le type le plus fréquent de cancer thyroïdien, et les diagnostics ont fortement augmenté ces dernières années, notamment avec la généralisation des échographies cervicales de routine. La plupart des nodules thyroïdiens sont bénins, mais certains sont malins, et les examens actuels nécessitent souvent une ponction ou une intervention chirurgicale pour en être sûrs. Cette étude pose une question simple mais importante : un tout petit changement dans notre ADN peut‑il aider à expliquer qui est plus susceptible de développer un carcinome papillaire de la thyroïde, et ce même changement peut‑il aussi influencer le fonctionnement de la thyroïde et l’agressivité d’une tumeur ?
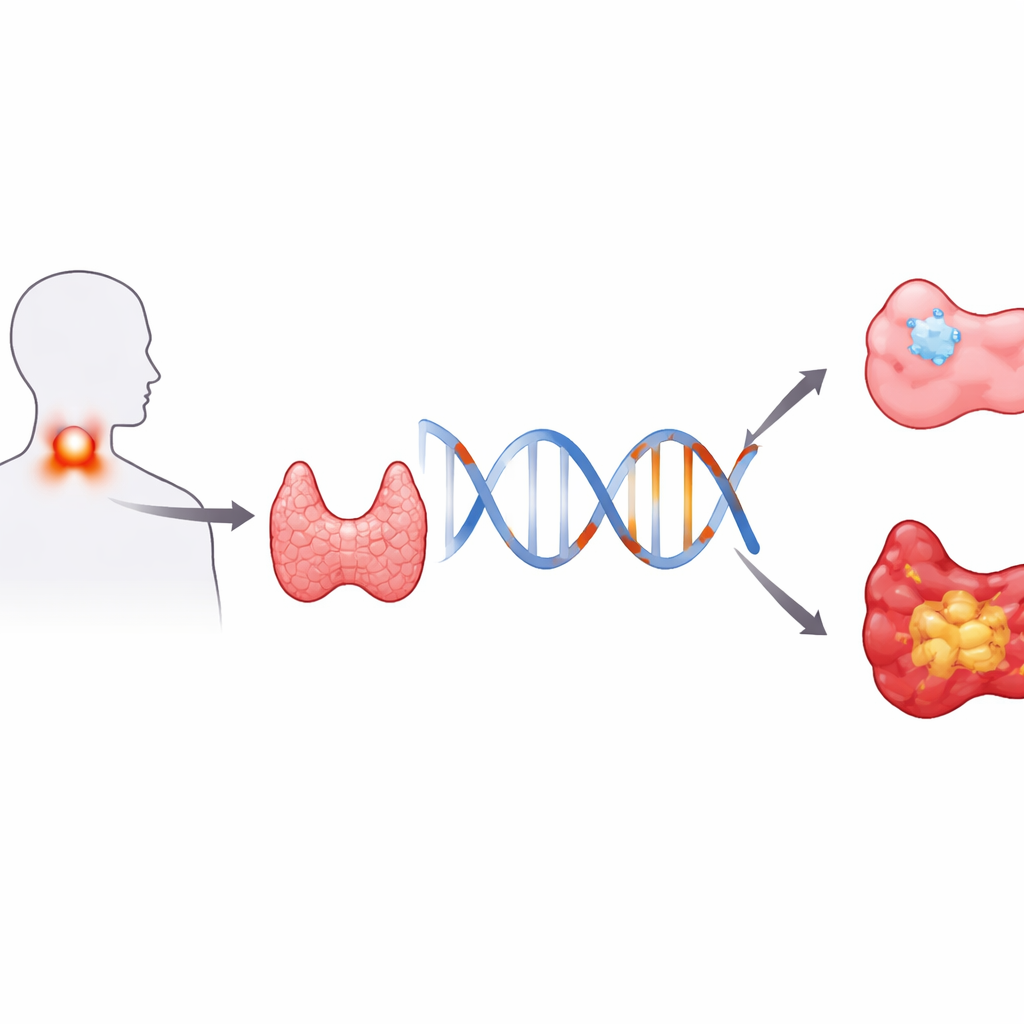
Un petit changement d’ADN aux grandes conséquences
Les chercheurs se sont concentrés sur une seule « lettre » de notre code génétique, connue sous le nom de rs965513, située près d’un gène appelé FOXE1. FOXE1 contribue au développement et au fonctionnement de la glande thyroïde. À cet endroit de l’ADN, une personne peut porter soit la version G, soit la version A, ou une copie de chaque. Les scientifiques ont étudié 346 adultes en Chine présentant des nodules thyroïdiens : 75 avaient un carcinome papillaire et 271 avaient des nodules bénins, non cancéreux. En comparant la fréquence de chaque version génétique dans ces deux groupes, ils ont pu vérifier si la version A ou la version G favorisait l’apparition du cancer.
Qui porte un risque accru et qui est protégé
L’équipe a testé plusieurs modèles de regroupement des génotypes et a trouvé une histoire cohérente. Les personnes portant au moins une copie de la version A du rs965513 avaient plus de deux fois plus de chances d’avoir un carcinome papillaire de la thyroïde que celles présentant deux copies de la version G, même après ajustement pour l’âge, le sexe, le poids et la tension artérielle. La version G semblait jouer un rôle protecteur, étant plus fréquente chez les personnes dont les nodules étaient bénins. Chaque copie supplémentaire de la version A augmentait le risque, ce qui suggère une relation dose–réponse plutôt qu’un mécanisme binaire tout ou rien. Ces effets étaient particulièrement marqués chez les patients plus jeunes et dans certains sous‑groupes cliniques, laissant penser que ce changement d’ADN pourrait avoir plus d’importance tôt dans la vie ou dans des contextes biologiques particuliers.
Liens avec une mutation tumorale majeure et les taux hormonaux
L’étude a également examiné une mutation oncogénique bien connue dans un autre gène, BRAF. Lorsque cette mutation, appelée BRAFV600E, est présente dans les tumeurs papillaires de la thyroïde, les cancers ont souvent une croissance et une propension à la dissémination plus agressives. Parmi l’ensemble des patients porteurs de nodules thyroïdiens, ceux qui avaient la version A du rs965513 étaient environ deux fois et demie plus susceptibles de présenter la mutation BRAFV600E que les personnes avec deux copies de la version G. Autrement dit, le même changement hérité qui augmentait le risque global de cancer rendait aussi plus probable la présence de cette mutation majeure dans les tumeurs. Les chercheurs ont par ailleurs analysé des bilans sanguins et observé que les personnes avec deux copies G avaient tendance à présenter des taux plus élevés d’hormone stimulant la thyroïde (TSH), tandis que les porteurs de la version A avaient tendance à avoir une TSH plus basse. De grandes études génétiques ont déjà lié une TSH plus basse à un risque accru de cancer thyroïdien, de sorte que ce schéma s’intègre dans une vision plus large où hormones thyroïdiennes et variants hérités interagissent pour façonner la susceptibilité au cancer.
Ce que cela pourrait signifier pour le dépistage et la prise en charge
Parce que ce changement génétique est présent dès la naissance, il ne peut à lui seul diagnostiquer un cancer dans un nodule particulier et ne remplace pas l’imagerie ou la biopsie. Cependant, connaître si une personne porte la version A ou G pourrait, à l’avenir, faire partie d’un profil de risque plus personnalisé. Par exemple, les personnes porteuses de la version A, surtout si elles sont plus jeunes ou présentent d’autres signes préoccupants, pourraient bénéficier d’un suivi plus rapproché des nodules thyroïdiens ou d’un test moléculaire précoce comme la recherche de BRAFV600E. À l’inverse, les personnes avec le génotype G–G pourraient avoir un risque de base quelque peu inférieur. Combiner ce marqueur héréditaire simple avec le statut mutationnel de la tumeur et les dosages hormonaux de routine pourrait améliorer la capacité des médecins à distinguer les nodules dangereux de ceux qui peuvent être surveillés en toute sécurité.
Comment ces résultats s’inscrivent dans le tableau d’ensemble
Pour le lecteur non spécialiste, l’essentiel est qu’une seule lettre héritée près du gène FOXE1 semble orienter la thyroïde vers un risque accru de cancer de plusieurs façons simultanément : elle augmente la probabilité de carcinome papillaire, favorise la présence de la mutation agressive BRAFV600E et s’accompagne d’une TSH légèrement plus basse qui peut favoriser la transformation maligne. L’étude, menée dans une population chinoise, confirme et étend des travaux antérieurs réalisés chez des Européens et d’autres populations, suggérant que ce marqueur génétique a une portée mondiale. Si des études plus larges et complémentaires sont nécessaires avant que ce type de test ne devienne courant, ce travail apporte une pièce importante au puzzle expliquant pourquoi certaines personnes portant des nodules thyroïdiens développent un cancer et d’autres non, et il ouvre la voie à un futur où le dépistage et le traitement du cancer thyroïdien seraient mieux adaptés au profil génétique de chaque individu.
Citation: Zhang, W., Gao, Y., Zeng, S. et al. The FOXE1 rs965513 polymorphism: a pleiotropic risk locus associated with thyroid function, BRAFV600E mutation, and susceptibility to papillary thyroid cancer. Sci Rep 16, 13945 (2026). https://doi.org/10.1038/s41598-026-44229-6
Mots-clés: carcinome papillaire de la thyroïde, gène FOXE1, risque génétique, mutation BRAFV600E, hormones thyroïdiennes