Clear Sky Science · es
El polimorfismo FOXE1 rs965513: un locus de riesgo pleiotrópico asociado con la función tiroidea, la mutación BRAFV600E y la susceptibilidad al cáncer papilar de tiroides
Por qué importan tu tiroides y tus genes
El cáncer papilar de tiroides es el tipo más común de cáncer tiroideo, y los diagnósticos han aumentado notablemente en los últimos años, sobre todo a medida que más personas se someten a ecografías de cuello de rutina. La mayoría de los nódulos tiroideos son inocuos, pero algunos son malignos, y las pruebas actuales con frecuencia requieren punciones o cirugía para confirmarlo. Este estudio plantea una pregunta simple pero importante: ¿puede un pequeño cambio en nuestro ADN ayudar a explicar quién tiene más probabilidades de desarrollar cáncer papilar de tiroides, y podría ese mismo cambio también influir en cómo funciona la tiroides y en cuán agresivo se vuelve un tumor?
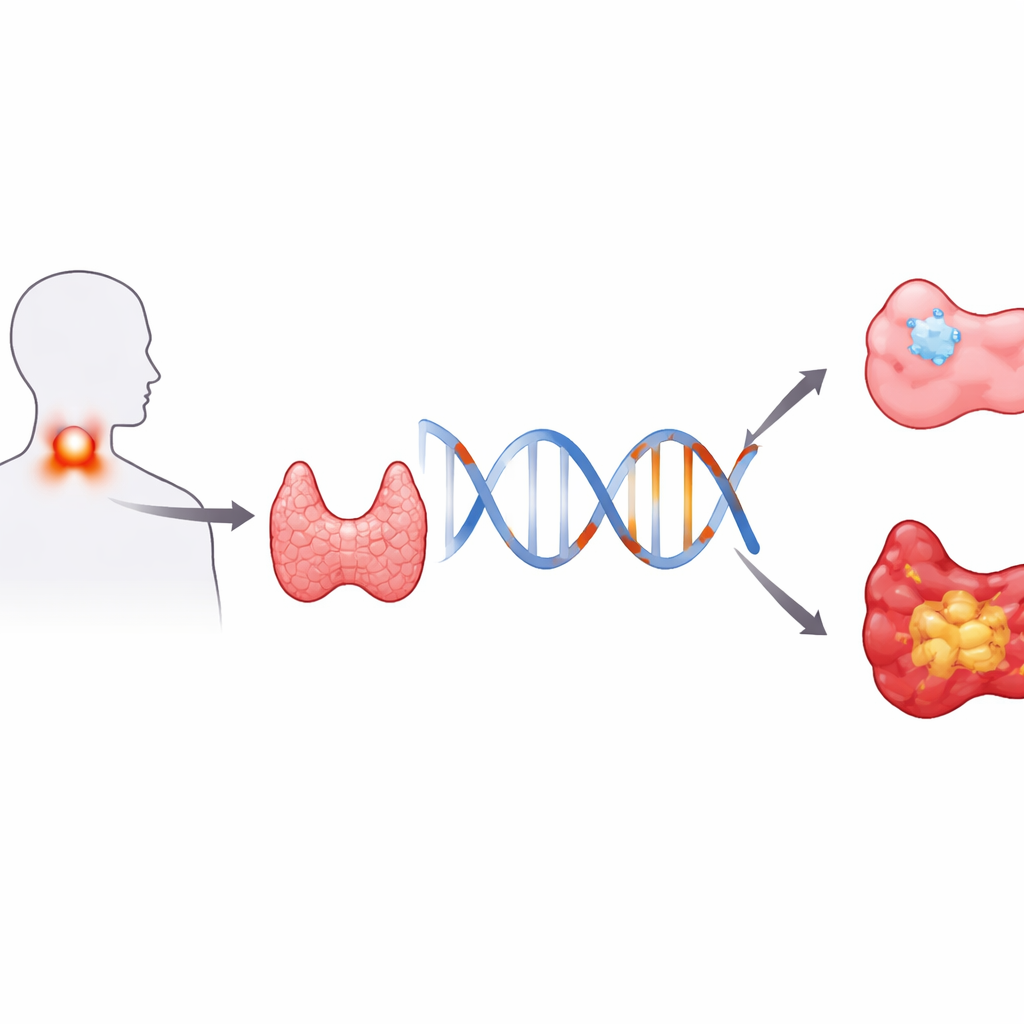
Un pequeño cambio en el ADN con un gran impacto
La investigación se centra en un único cambio de “letra” en nuestro código genético, conocido como rs965513, ubicado cerca de un gen llamado FOXE1. FOXE1 ayuda a orientar cómo se forma y funciona la glándula tiroidea. En ese lugar del ADN, las personas pueden portar la versión G, la versión A, o una de cada una. Los científicos estudiaron a 346 adultos en China que tenían nódulos tiroideos: 75 presentaban cáncer papilar de tiroides y 271 tenían nódulos benignos, no cancerosos. Al comparar la frecuencia de cada versión genética en estos dos grupos, pudieron ver si la versión A o la G inclinaba la balanza hacia el cáncer.
Quién carga con mayor riesgo y quién está protegido
El equipo probó varias formas de agrupar los patrones genéticos y encontró un mensaje consistente. Las personas que portaban al menos una copia de la versión A de rs965513 tenían más del doble de probabilidad de presentar cáncer papilar de tiroides que aquellas con dos copias de la versión G, incluso tras ajustar por edad, sexo, peso corporal y presión arterial. La versión G pareció actuar como un escudo, siendo más común en personas cuyos nódulos eran benignos. Cada copia adicional de la versión A aumentaba el riesgo, lo que sugiere una relación dosis‑respuesta en lugar de un interruptor simple de encendido/apagado. Estos efectos fueron especialmente claros en pacientes más jóvenes y en algunos subgrupos clínicos, lo que insinúa que este cambio en el ADN puede importar más temprano en la vida o bajo determinadas condiciones biológicas.
Vínculos con una mutación tumoral clave y con los niveles hormonales
El estudio también examinó un conocido fallo productor de cáncer en otro gen, BRAF. Cuando esta mutación, llamada BRAFV600E, está presente en tumores papilares de tiroides, los cánceres suelen crecer y diseminarse con mayor agresividad. Entre todos los pacientes con nódulos tiroideos, quienes portaban la versión A de rs965513 tenían alrededor de dos veces y media más probabilidad de albergar la mutación BRAFV600E que las personas con dos copias de la G. En otras palabras, el mismo cambio hereditario en el ADN que aumentó el riesgo general de cáncer también hizo más probable que los tumores llevaran este potente impulsor mutacional. Los investigadores examinaron además análisis de sangre y hallaron que las personas con dos copias de la G tendían a presentar niveles más altos de la hormona estimulante de la tiroides (TSH), mientras que las portadoras de la versión A tendían a tener TSH más baja. Estudios genéticos a gran escala han relacionado previamente una TSH más baja con mayor riesgo de cáncer tiroideo, por lo que este patrón encaja en una imagen más amplia en la que las hormonas tiroideas y las variantes hereditarias interactúan para moldear la susceptibilidad al cáncer.
Qué puede significar esto para el cribado y la atención
Puesto que este cambio genético está presente desde el nacimiento, no puede por sí solo diagnosticar cancer en un nódulo específico, ni sustituye a la imagenología o a la biopsia. Sin embargo, saber si alguien porta la versión A o la G podría, en el futuro, formar parte de un perfil de riesgo más personalizado. Por ejemplo, las personas con la versión A, especialmente si son más jóvenes o presentan otros rasgos preocupantes, podrían beneficiarse de un seguimiento más estrecho de los nódulos tiroideos o de pruebas moleculares más tempranas, como la detección de BRAFV600E. Por el contrario, quienes tienen el patrón G–G podrían tener un riesgo basal algo menor. Combinar este marcador hereditario sencillo con el estado mutacional del tumor y con mediciones hormonales de rutina podría afinar la capacidad de los médicos para juzgar qué nódulos son peligrosos y cuáles pueden observarse con seguridad.
Cómo encajan los hallazgos en el panorama general
Para un lector no especializado, la conclusión es que una sola letra heredada del ADN, situada cerca del gen FOXE1, parece inclinar la tiroides hacia el cáncer de varias maneras a la vez: aumenta la probabilidad de cáncer papilar de tiroides, hace más probable la presencia de la agresiva mutación BRAFV600E y se asocia con niveles ligeramente inferiores de TSH que podrían favorecer el cambio maligno. El estudio, realizado en una población china, respalda y amplía trabajos anteriores en europeos y otros grupos, lo que sugiere que este marcador genético tiene relevancia a escala global. Aunque se necesitan estudios más amplios y numerosos antes de que este tipo de pruebas se convierta en algo rutinario, este trabajo añade una pieza importante al rompecabezas de por qué algunas personas con nódulos tiroideos desarrollan cáncer y otras no, y apunta hacia un futuro en el que el cribado y el tratamiento del cáncer tiroideo estén mejor adaptados al perfil genético de cada persona.
Cita: Zhang, W., Gao, Y., Zeng, S. et al. The FOXE1 rs965513 polymorphism: a pleiotropic risk locus associated with thyroid function, BRAFV600E mutation, and susceptibility to papillary thyroid cancer. Sci Rep 16, 13945 (2026). https://doi.org/10.1038/s41598-026-44229-6
Palabras clave: cáncer papilar de tiroides, gen FOXE1, riesgo genético, mutación BRAFV600E, hormonas tiroideas