Clear Sky Science · de
Das FOXE1-rs965513-Polymorphismus: ein pleiotroper Risikolocus, verbunden mit Schilddrüsenfunktion, BRAFV600E-Mutation und Anfälligkeit für papillärer Schilddrüsenkarzinom
Warum Ihre Schilddrüse und Ihre Gene wichtig sind
Das papilläres Schilddrüsenkarzinom ist die häufigste Form von Schilddrüsenkrebs, und die Diagnosen sind in den letzten Jahren stark gestiegen, insbesondere weil mehr Menschen routinemäßige Halsultraschalluntersuchungen erhalten. Die meisten Schilddrüsenknoten sind harmlos, aber einige sind bösartig, und aktuelle Tests erfordern oft eine Nadeluntersuchung oder eine Operation, um sicher zu sein. Diese Studie stellt eine einfache, aber wichtige Frage: Kann eine winzige Veränderung in unserer DNA erklären, wer eher ein papilläres Schilddrüsenkarzinom entwickelt, und könnte dieselbe Veränderung auch beeinflussen, wie die Schilddrüse arbeitet und wie aggressiv ein Tumor wird?
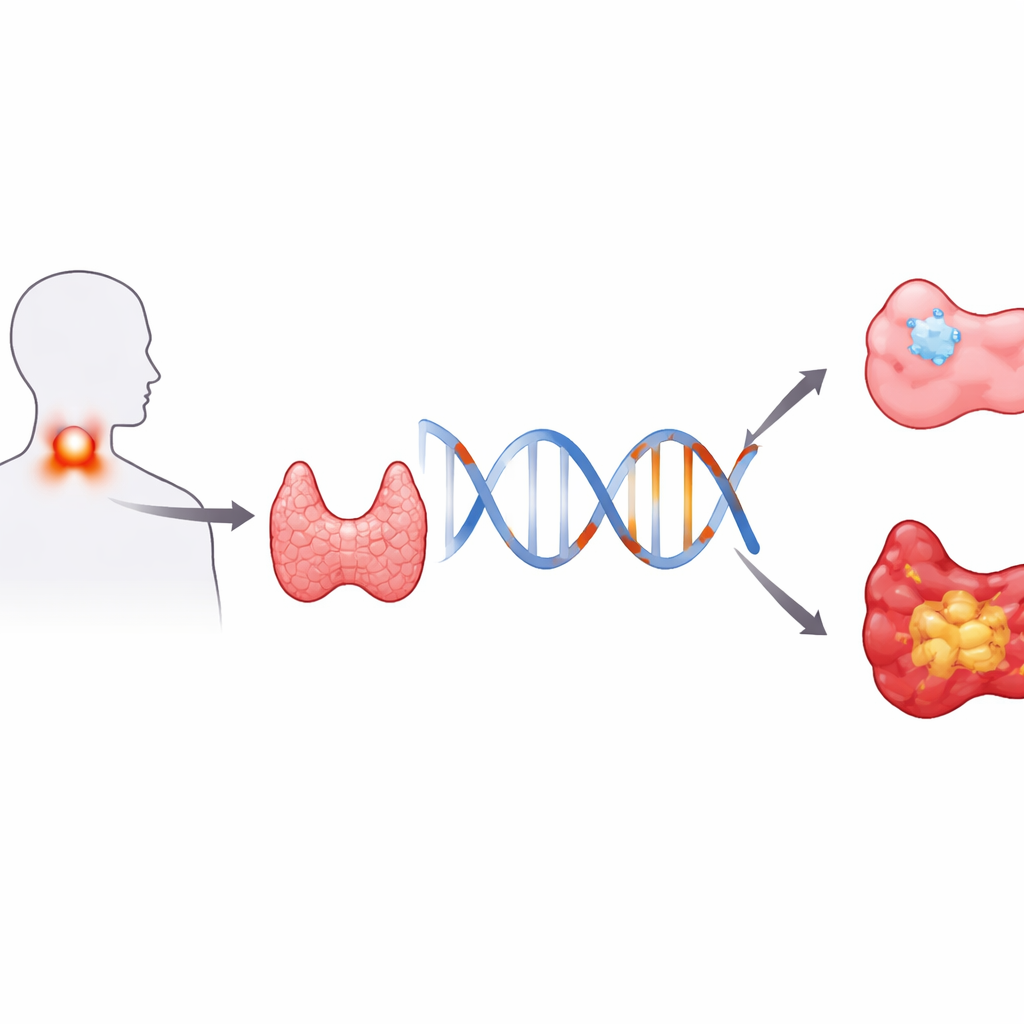
Eine kleine DNA-Änderung mit großer Wirkung
Die Forschung konzentriert sich auf eine einzelne "Buchstaben"-Veränderung in unserem genetischen Code, bekannt als rs965513, die in der Nähe eines Gens namens FOXE1 liegt. FOXE1 steuert mit, wie sich die Schilddrüse bildet und funktioniert. An dieser Stelle in der DNA können Menschen entweder die G-Variante, die A-Variante oder je eine Kopie von beidem tragen. Die Wissenschaftler untersuchten 346 Erwachsene in China mit Schilddrüsenknoten: 75 hatten ein papilläres Schilddrüsenkarzinom und 271 hatten gutartige, nicht bösartige Knoten. Durch den Vergleich, wie häufig jede genetische Variante in diesen beiden Gruppen vorkam, konnten sie feststellen, ob die A- oder die G-Variante das Risiko für Krebs erhöht.
Wer ein erhöhtes Risiko trägt und wer geschützt ist
Das Team testete mehrere Modelle zur Gruppierung der genetischen Muster und fand eine konsistente Geschichte. Personen, die mindestens eine A-Variante von rs965513 tragen, hatten mehr als doppelt so häufig ein papilläres Schilddrüsenkarzinom wie Personen mit zwei G-Varianten, selbst nachdem Alter, Geschlecht, Körpergewicht und Blutdruck berücksichtigt wurden. Die G-Variante schien als Schutz zu wirken und war häufiger bei Personen mit gutartigen Knoten. Jede zusätzliche Kopie der A-Variante erhöhte das Risiko weiter, was auf eine Dosis-Wirkungs-Beziehung hindeutet, statt eines einfachen An- oder Aus-Effekts. Diese Effekte waren besonders klar bei jüngeren Patientinnen und Patienten und in einigen klinischen Untergruppen, was darauf hindeutet, dass diese DNA-Veränderung besonders früh im Leben oder unter bestimmten biologischen Bedingungen von Bedeutung sein könnte.
Verbindungen zu einer wichtigen Tumormutation und Hormonwerten
Die Studie untersuchte auch eine bekannte krebsfördernde Veränderung in einem anderen Gen, BRAF. Wenn diese Mutation, BRAFV600E genannt, in papillären Schilddrüsentumoren vorhanden ist, wachsen und streuen die Tumore oft aggressiver. Unter allen Patientinnen und Patienten mit Schilddrüsenknoten waren diejenigen mit der A-Variante von rs965513 etwa zweieinhalbmal wahrscheinlicher, die BRAFV600E-Mutation zu tragen als Personen mit zwei G-Varianten. Anders gesagt: Dieselbe vererbte DNA-Veränderung, die das Gesamtrisiko für Krebs erhöhte, machte es wahrscheinlicher, dass Tumore diesen starken Treiber aufweisen. Die Forschenden untersuchten außerdem Blutwerte und stellten fest, dass Personen mit zwei G-Varianten tendenziell höhere Werte des schilddrüsenstimulierenden Hormons (TSH) hatten, während Träger der A-Variante eher niedrigere TSH-Werte aufwiesen. Große genetische Studien haben zuvor niedrigere TSH-Werte mit einem höheren Schilddrüsenkrebsrisiko in Verbindung gebracht, sodass dieses Muster in ein größeres Bild passt, in dem Schilddrüsenhormone und vererbte Varianten zusammenwirken, um die Krebsanfälligkeit zu formen.
Was das für Screening und Versorgung bedeuten könnte
Weil diese genetische Veränderung von Geburt an vorhanden ist, kann sie allein kein Krebsdiagnose für einen spezifischen Knoten liefern und ersetzt weder Bildgebung noch Biopsie. Das Wissen darüber, ob jemand die A- oder G-Variante trägt, könnte jedoch künftig Teil eines personalisierteren Risikoprofils werden. Beispielsweise könnten Personen mit der A-Variante, besonders wenn sie jünger sind oder andere besorgniserregende Merkmale aufweisen, von einer engeren Überwachung von Schilddrüsenknoten oder früheren molekularen Tests wie BRAFV600E profitieren. Umgekehrt könnte Personen mit dem G–G-Muster ein etwas geringeres Grundrisiko zugeschrieben werden. Die Kombination dieses einfachen vererbten Markers mit dem Tumormutationsstatus und routinemäßigen Hormonmessungen könnte die Fähigkeit von Ärztinnen und Ärzten verbessern, einzuschätzen, welche Knoten gefährlich sind und welche sicher beobachtet werden können.
Wie die Ergebnisse ins größere Bild passen
Für eine nichtfachliche Leserin oder einen nichtfachlichen Leser lautet die Schlussfolgerung, dass ein einzelner vererbter DNA-Buchstabe in der Nähe des FOXE1-Gens die Schilddrüse in mehrfacher Hinsicht in Richtung Krebs zu neigen scheint: Er erhöht die Wahrscheinlichkeit für ein papilläres Schilddrüsenkarzinom, macht die aggressive BRAFV600E-Mutation wahrscheinlicher und steht im Zusammenhang mit leicht niedrigeren TSH-Werten, die maligne Veränderungen begünstigen können. Die Studie, durchgeführt an einer chinesischen Population, stützt und erweitert frühere Arbeiten in europäischen und anderen Gruppen und legt nahe, dass dieser genetische Marker globale Relevanz besitzt. Obwohl vor einer routinemäßigen Anwendung größere und weitere Studien nötig sind, fügt diese Arbeit ein wichtiges Puzzleteil hinzu zur Antwort auf die Frage, warum einige Menschen mit Schilddrüsenknoten Krebs entwickeln und andere nicht, und sie weist in eine Zukunft, in der Screening und Behandlung von Schilddrüsenkrebs stärker an die genetische Ausstattung einzelner Personen angepasst werden.
Zitation: Zhang, W., Gao, Y., Zeng, S. et al. The FOXE1 rs965513 polymorphism: a pleiotropic risk locus associated with thyroid function, BRAFV600E mutation, and susceptibility to papillary thyroid cancer. Sci Rep 16, 13945 (2026). https://doi.org/10.1038/s41598-026-44229-6
Schlüsselwörter: papilläres Schilddrüsenkarzinom, FOXE1-Gen, genetisches Risiko, BRAFV600E-Mutation, Schilddrüsenhormone