Clear Sky Science · fr
La fonction NvashA révèle des différences temporelles dans la génération de sous-types neuronaux chez les cnidaires
Comment de simples réseaux nerveux racontent une histoire ancienne
L’anémone étoilée peut sembler simple, mais son réseau nerveux contient des indices sur la manière dont les cerveaux animaux se sont d’abord formés. Cette étude pose une question étonnamment moderne chez une créature très ancienne : pas seulement où les cellules nerveuses se forment, mais quand différents types de neurones naissent et si le temps contribue à diversifier le système nerveux. En suivant des vagues de cellules nerveuses nouvellement formées sur plusieurs jours de développement, les auteurs montrent que ce modeste animal marin utilise le temps, autant que l’espace, pour produire une riche palette de types cellulaires neuronaux — laissant entendre que cette stratégie pourrait remonter à l’ancêtre commun de la plupart des animaux dotés de nerfs.
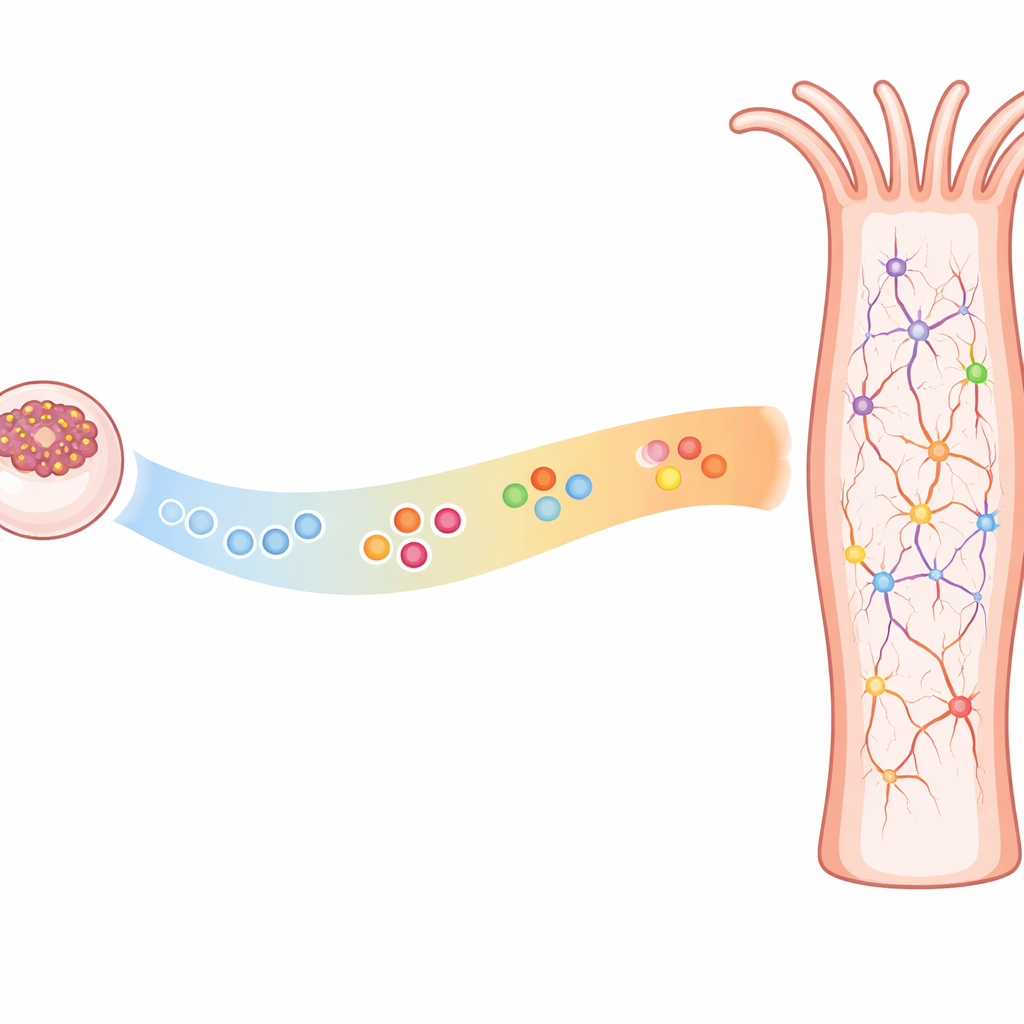
Construire un réseau nerveux au fil du temps
Les cnidaires, comme les anémones et les méduses, possèdent un réseau nerveux diffus plutôt qu’un cerveau centralisé, mais ils partagent beaucoup des mêmes outils génétiques qui façonnent les systèmes nerveux chez des animaux plus complexes. Des travaux antérieurs ont montré que les anémones et les animaux bilatériens (comme les mouches et les mammifères) utilisent des réseaux de gènes similaires pour activer l’identité neuronale, choisir les cellules progénitrices et délimiter de larges régions du corps où certains neurones apparaissent. Ce qui n’était pas clair, c’était si le chronométrage importait aussi dans ces réseaux simples — si des sous-types neuronaux spécifiques apparaissent dans une séquence définie au fur et à mesure du développement, comme c’est le cas dans les cerveaux et la moelle épinière des animaux plus complexes.
Suivre un interrupteur neural clé
Pour examiner cela, les chercheurs se sont concentrés sur un gène nommé NvashA, connu pour s’activer lorsque les neurones immatures émergent de leurs cellules mères, puis s’estomper à mesure que ces neurones atteignent leur maturité. Parce que NvashA couvre cette fenêtre allant de « juste né » à « presque terminé », sa présence marque les cellules en train de devenir des neurones. L’équipe a utilisé le séquençage d’ARN mono-cellule pour profiler des milliers de cellules positives pour NvashA collectées chez des embryons et des larves libres nageuses à quatre moments différents, puis a regroupé ces cellules en clusters selon leurs signatures d’expression génique. Ils ont aussi recoupé ces clusters avec des atlas cellulaires existants pour identifier des types neuronaux, des cellules sécrétoires et des cellules urticantes.
Vagues précoces et tardives de types neuronaux
L’analyse a révélé deux grands groupes de neurones marqués par NvashA. Un groupe contenait des cellules présentes dès les premiers stades embryonnaires et jusqu’aux stades larvaires ultérieurs, incluant des neurones immatures et plusieurs sous-types neuronaux décrits auparavant qui apparaissent tôt puis continuent de mûrir. Le second groupe, en revanche, était constitué quasi exclusivement de neurones trouvés seulement aux stades larvaires. Dans ce groupe tardif, l’équipe a identifié des cellules immatures et plusieurs sous-types neuronaux distincts qui semblent émerger uniquement après que l’animal a déjà établi un plan corporel de base. Les analyses de pseudotemps et de trajectoire — une façon d’ordonner les cellules le long de parcours développementaux — ont montré des embranchements partant de ces états immatures vers plusieurs types neuronaux spécialisés, les neurones des stades tardifs étant clairement séparés de l’ensemble né plus tôt.
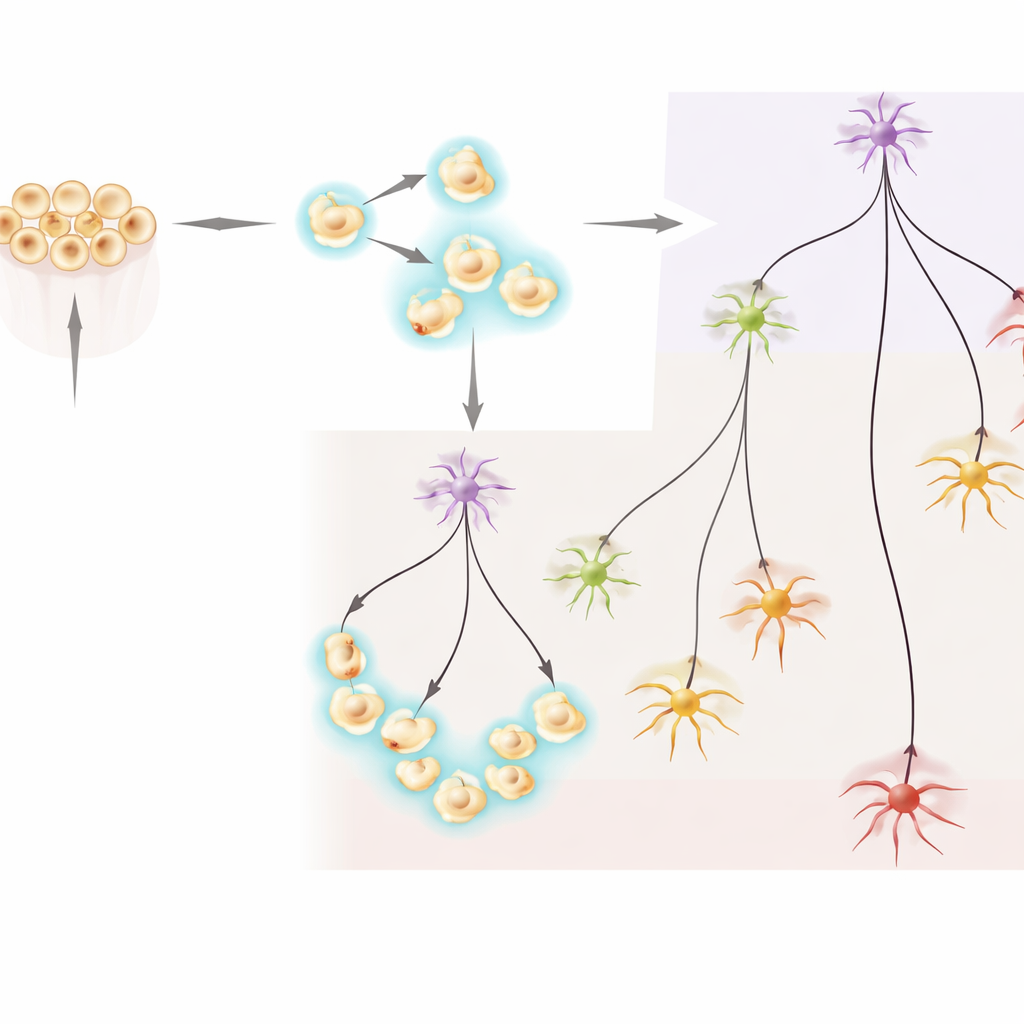
Où apparaissent les nouveaux neurones dans le corps
Les auteurs ont ensuite cherché où ces types neuronaux formés tardivement apparaissent le long de l’axe oral–aboral principal de l’animal (de la bouche à l’extrémité opposée). À l’aide d’hybridation in situ, ils ont visualisé des gènes marqueurs enrichis dans des clusters neuronaux tardifs spécifiques. Ces marqueurs montraient des motifs dispersés chez les larves, mais leurs positions correspondaient à des régions corporelles — comme le tronc et les territoires aboraux — qui sont connues pour être établies bien plus tôt dans le développement. Certains marqueurs de neurones tardifs étaient surtout confinés à l’extrémité aborale, tandis que d’autres étaient restreints au tronc, faisant écho à des « bandes » spatiales cartographiées précédemment. Cela indique que les mêmes domaines spatiaux peuvent générer différents types de neurones à des moments distincts, ce qui implique que l’information temporelle se superpose à la cartographie corporelle préexistante pour élargir la diversité neuronale.
Tester ce que NvashA fait réellement
Pour déterminer l’importance de NvashA dans la construction de ces neurones, les chercheurs ont réduit ou supprimé son activité par deux approches : l’inhibition par ARN court en épingle (shRNA) et un knockout génique précis créé par CRISPR. Chez les embryons précoces, la diminution de NvashA a fortement réduit l’expression de plusieurs gènes cibles neuronaux connus, confirmant son rôle central dans la neurogenèse précoce. Aux stades larvaires tardifs, beaucoup de ces mêmes gènes ont partiellement récupéré leur expression, mais des expériences temporelles plus fines ont montré que leur activation était retardée lorsque NvashA était altéré. Les marqueurs de sous-types neuronaux tardifs étaient aussi affaiblis, bien que pas complètement perdus, chez les animaux mutants. Ensemble, ces résultats suggèrent que NvashA n’est pas un interrupteur tout‑ou‑rien pour des classes neuronales entières, mais qu’il aide à contrôler le calendrier et la maturation correcte des sous‑types neuronaux nés tôt et tard.
Ce que cela signifie pour l’origine des cerveaux
En termes simples, ce travail montre que le réseau nerveux d’une anémone de mer n’est pas une grille statique de cellules identiques ; il se construit par vagues, avec différents types de neurones émergeant à des moments distincts au sein de régions corporelles spécifiques. Cet « axe temporel » de la mise en place du système nerveux — connu depuis longtemps chez les organismes dotés de cerveaux complexes — opère aussi chez un animal simple à symétrie radiale. Cela soutient l’idée que l’utilisation conjointe d’indices spatiaux (où dans le corps) et temporels (quand pendant le développement) pour générer une variété de neurones est une stratégie ancienne, probablement présente chez l’ancêtre commun des cnidaires et des bilatériens. Si les molécules exactes codant l’information temporelle peuvent différer entre espèces, la logique sous-jacente — réutiliser les mêmes régions du corps à différents moments pour produire de nouveaux types neuronaux — semble être une solution profondément conservée pour bâtir des systèmes nerveux diversifiés.
Citation: Havrilak, J.A., Cheng, M., Al-Shaer, L. et al. NvashA function reveals temporal differences in neural subtype generation in cnidarians. Sci Rep 16, 12151 (2026). https://doi.org/10.1038/s41598-026-41460-z
Mots-clés: neurogenèse, anémone de mer, réseau nerveux, évolution des systèmes nerveux, séquençage ARN mono-cellule