Clear Sky Science · de
NvashA-Funktion zeigt zeitliche Unterschiede bei der Generierung neuronaler Subtypen bei Nesseltiere
Wie einfache Nervennetze eine uralte Geschichte erzählen
Die Kegelschnecken-Anemone (starlet sea anemone) mag einfach wirken, doch ihr Nervennetz birgt Hinweise darauf, wie die Gehirne aller Tiere ursprünglich entstanden sind. Diese Studie stellt in einem sehr alten Lebewesen eine überraschend moderne Frage: nicht nur wo Nervenzellen entstehen, sondern wann verschiedene Neuronentypen geboren werden und ob die Zeitsteuerung zur Diversifizierung des Nervensystems beiträgt. Indem die Autorinnen und Autoren Wellen neugeborener Nervenzellen über mehrere Tage der Entwicklung verfolgten, zeigen sie, dass dieses unscheinbare Meereswesen neben dem Raum auch die Zeit nutzt, um eine vielfältige Gruppe neuronaler Zelltypen aufzubauen — was nahelegt, dass diese Strategie bis zum gemeinsamen Vorfahren der meisten namentlich mit Nerven ausgestatteten Tiere zurückreichen könnte.
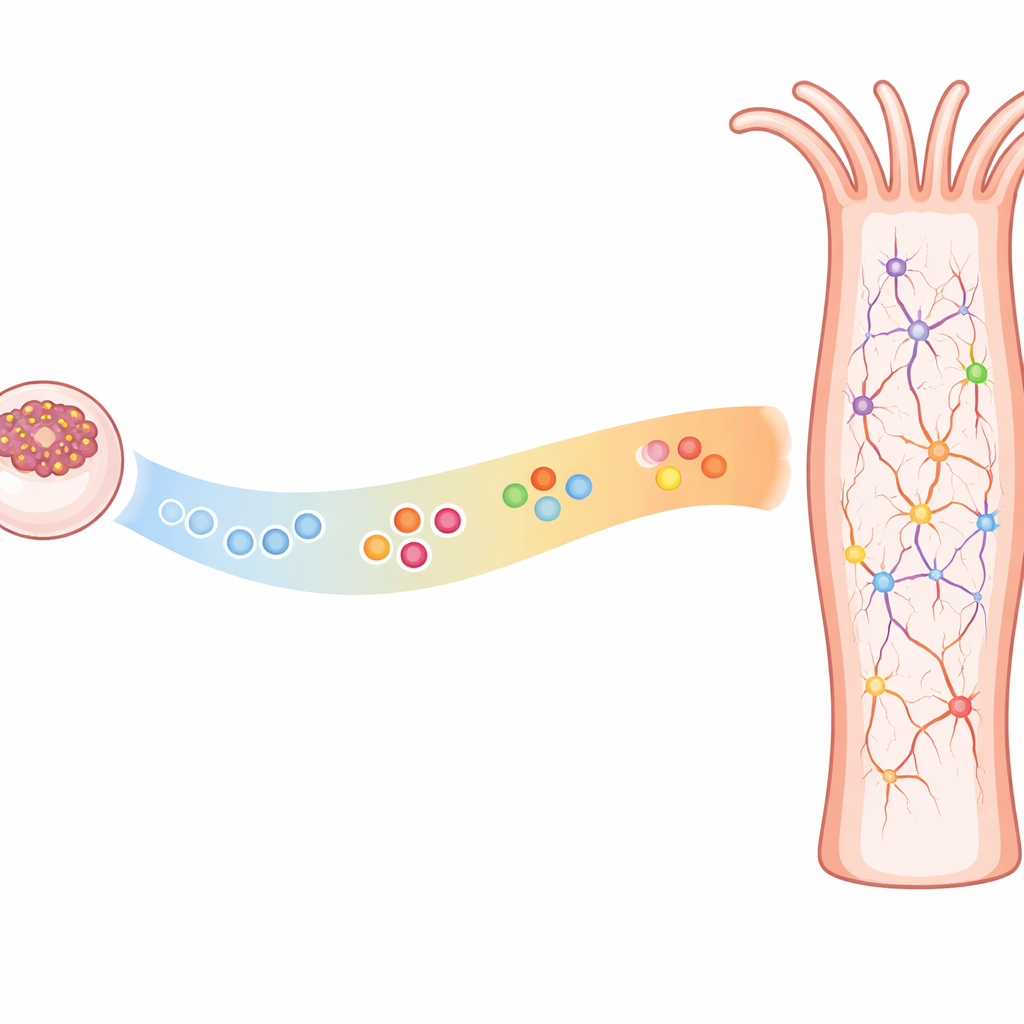
Ein Nervennetz im Zeitverlauf aufbauen
Nesseltiere wie Anemonen und Quallen besitzen kein zentrales Gehirn, sondern ein diffuses Nervennetz, teilen aber viele der genetischen Werkzeuge, die in komplexeren Tieren Nervensysteme formen. Frühere Arbeiten zeigten, dass Seeanemonen und bilateralsymmetrische Tiere (wie Fliegen und Säugetiere) ähnliche Gen-Netzwerke nutzen, um neuronale Identität zu aktivieren, Vorläuferzellen auszuwählen und breite Körperregionen zu markieren, in denen bestimmte Neuronen entstehen. Unklar war jedoch, ob auch die Zeit eine Rolle in diesen einfachen Nervennetzen spielt — ob bestimmte Neuronensubtypen in einer festen Reihenfolge während der Entwicklung auftreten, wie es in Gehirn und Rückenmark komplexerer Tiere der Fall ist.
Einem wichtigen neuronalen Schalter folgen
Um dies zu untersuchen, konzentrierten sich die Forschenden auf ein Gen namens NvashA, das dafür bekannt ist, beim Austritt unreifer Neuronen aus ihren Mutterzellen anzuspringen und dann wieder abzunehmen, wenn diese Neuronen vollständig reifen. Weil NvashA dieses Fenster vom „gerade geboren“ bis zum „fast fertig“ überspannt, markiert seine Präsenz Zellen im Akt der neuronalen Differenzierung. Das Team nutzte Einzelzell-RNA-Sequenzierung, um Tausende NvashA-positiver Zellen aus Embryonen und frei schwimmenden Larven zu vier Zeitpunkten zu profilieren und gruppierte diese Zellen anhand ihrer Genexpressionsmuster in Cluster. Zudem verglichen sie diese Cluster mit vorhandenen Zellatlanten, um Neuronentypen, sekretorische Zellen und Nesselkapselzellen zu identifizieren.
Frühe und späte Wellen von Neuronentypen
Die Analyse offenbarte zwei große Gruppen von NvashA-markierten Neuronen. Eine Gruppe umfasste Zellen, die von frühen Embryonalstadien bis in spätere Larvenstadien vorhanden sind, darunter unreife Neuronen und mehrere zuvor beschriebene Neuronensubtypen, die früh auftreten und dann weiter reifen. Die zweite Gruppe bestand dagegen nahezu ausschließlich aus Neuronen, die nur in Larvenstadien zu finden sind. Innerhalb dieser späteren Gruppe identifizierte das Team unreife Zellen und mehrere ausgeprägte Neuronensubtypen, die offenbar ausschließlich entstehen, nachdem das Tier bereits einen grundlegenden Körperplan gebildet hat. Pseudotime- und Trajektorieanalysen — Methoden, um Zellen entlang entwicklungsbiologischer Pfade zu ordnen — zeigten Verzweigungen, die von diesen unreifen Zuständen in mehrere spezialisierte Neuronentypen führten, wobei die später entstandenen Neuronen deutlich von der früh geborenen Gruppe separiert waren.
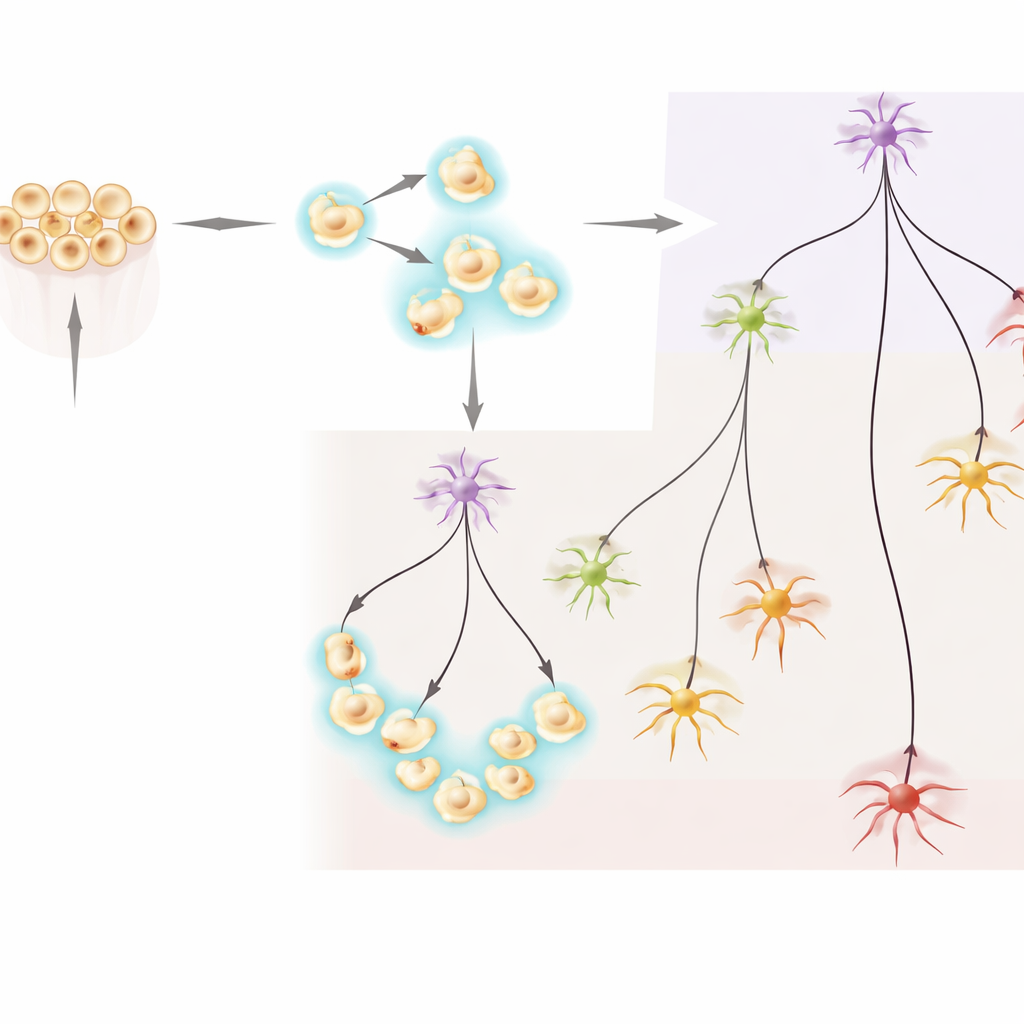
Wo neue Neuronen im Körper erscheinen
Die Autorinnen und Autoren fragten anschließend, wo diese spät entstehenden Neuronentypen entlang der Hauptachse des Tieres (oral–aboral, also von der Mundöffnung zum gegenüberliegenden Ende) auftreten. Mit in-situ-Hybridisierung visualisierten sie Markergene, die in bestimmten spätstadialen neuronalen Clustern angereichert waren. Diese Marker zeigten verstreute Muster in den Larven, doch ihre Positionen stimmten mit Körperregionen überein — etwa Rumpf und aborale Bereiche —, die bereits früher in der Entwicklung festgelegt werden. Einige späte Neuronenmarker waren größtenteils auf das aborale Ende beschränkt, andere hauptsächlich auf den Rumpf, was zuvor kartierten räumlichen „Streifen“ entspricht. Das deutet darauf hin, dass dieselben räumlichen Domänen zu verschiedenen Zeiten unterschiedliche Neuronentypen erzeugen können; Timing-Informationen legen sich also über bereits bestehende Körpermusterung und erweitern so die neuronale Vielfalt.
Untersuchen, was NvashA tatsächlich bewirkt
Um zu klären, wie essenziell NvashA für den Aufbau dieser Neuronen ist, reduzierten oder entfernten die Forschenden seine Aktivität mit zwei Ansätzen: durch short-hairpin-RNA-Knockdown und durch eine präzise Gen-Deletierung mittels CRISPR. In frühen Embryonen führte die Verringerung von NvashA zu einer starken Reduktion der Expression mehrerer bekannter neuronaler Zielgene, was seine zentrale Rolle in der frühen Neurogenese bestätigte. In späteren Larvenstadien erholten sich viele dieser Gene teilweise, detailliertere Zeitverlaufsexperimente zeigten jedoch, dass ihre Aktivierung bei beeinträchtigtem NvashA verzögert war. Marker für spätstadiale Neuronensubtypen waren ebenfalls abgeschwächt, aber nicht vollständig verloren, in den Mutanten. Zusammen deuten diese Ergebnisse darauf hin, dass NvashA kein Ein-/Aus-Schalter für ganze Neuronenklassen ist, sondern vielmehr die zeitliche Steuerung und die korrekte Reifung sowohl früh- als auch spätgeborener neuronaler Subtypen unterstützt.
Was das für den Ursprung von Gehirnen bedeutet
Einfach ausgedrückt zeigt diese Arbeit, dass das Nervennetz einer Seeanemone kein statisches Geflecht identischer Zellen ist; es entsteht in Wellen, wobei verschiedene Neuronentypen zu unterschiedlichen Zeiten in bestimmten Körperregionen auftreten. Diese „Zeitachse“ der Musterbildung im Nervensystem — lange bekannt bei Organismen mit komplexen Gehirnen — wirkt demnach auch in einem einfachen, radiärsymmetrischen Tier. Das stützt die Idee, dass die Kombination räumlicher Hinweise (wo im Körper) und zeitlicher Hinweise (wann während der Entwicklung) zur Erzeugung vielfältiger Neuronen eine alte Strategie ist, vermutlich bereits im gemeinsamen Vorfahren von Nessel- und bilateralen Tieren vorhanden. Während die genauen Moleküle, die zeitliche Information codieren, zwischen Arten variieren mögen, scheint die zugrunde liegende Logik — dieselben Körperregionen zu unterschiedlichen Zeiten zu nutzen, um neue Neuronentypen hervorzubringen — eine tief konservierte Lösung zum Aufbau vielfältiger Nervensysteme zu sein.
Zitation: Havrilak, J.A., Cheng, M., Al-Shaer, L. et al. NvashA function reveals temporal differences in neural subtype generation in cnidarians. Sci Rep 16, 12151 (2026). https://doi.org/10.1038/s41598-026-41460-z
Schlüsselwörter: Neurogenese, Seeanemone, Nervennetz, Evolution der Nervensysteme, Einzelzell-RNA-Sequenzierung