Clear Sky Science · fr
Cartographier l’activité ligand-cible spatiale avec Renoir
Comment les cellules communiquent dans leur voisinage
Nos corps sont constitués d’innombrables cellules qui « dialoguent » en permanence pour maintenir la santé des tissus, construire les organes et, dans certains cas, conduire des maladies comme le cancer. Cet article présente Renoir, une méthode informatique qui exploite des cartes à grande échelle de l’activité génique pour déterminer où et comment ces échanges cellulaires ont lieu dans de vrais tissus. En combinant la génomique spatiale moderne et l’analyse à l’échelle cellulaire, Renoir aide les chercheurs à voir non seulement qui parle à qui, mais aussi où dans le tissu ces conversations sont les plus intenses et quels effets elles produisent.
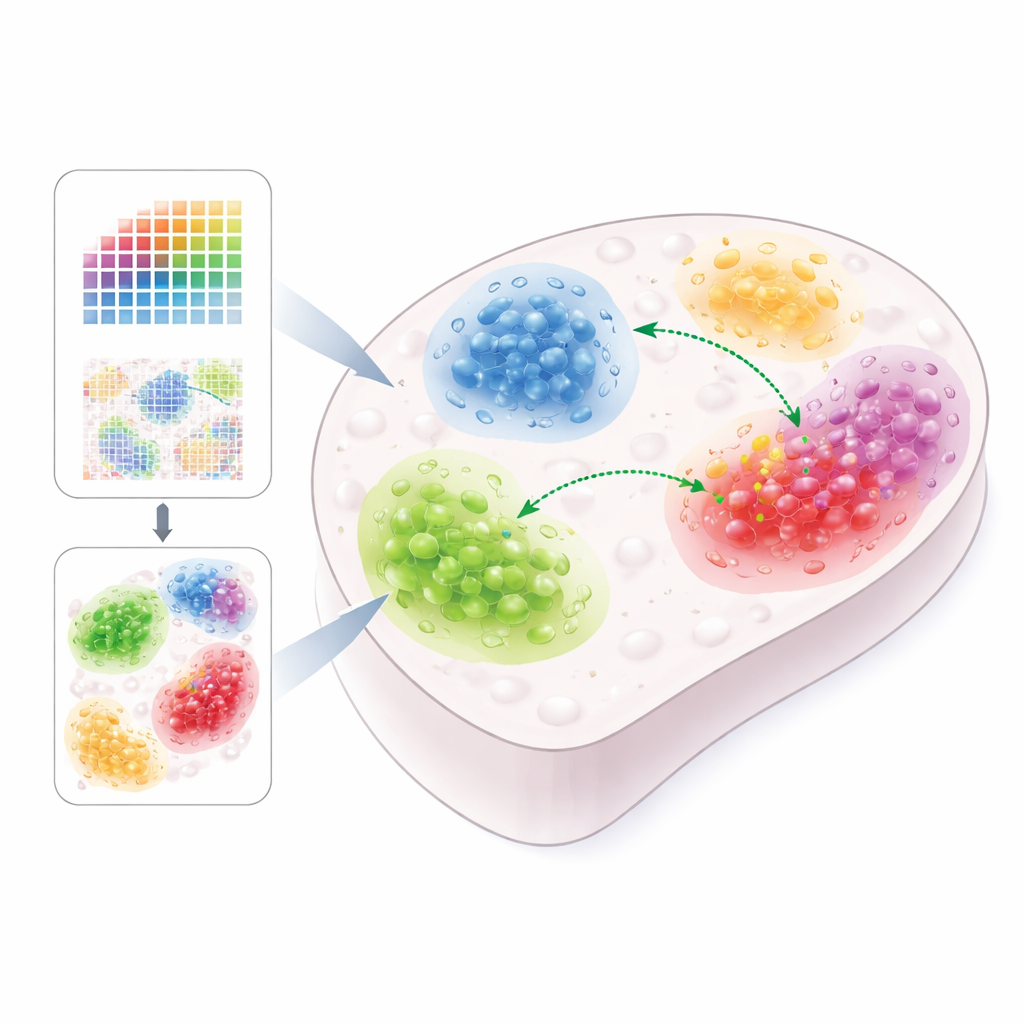
Signaux, messagers et conversations cellulaires
Les cellules communiquent via de petits messagers protéiques appelés ligands, libérés par une cellule et détectés par des cellules voisines par l’intermédiaire de récepteurs à leur surface. Quand un ligand se lie à son récepteur, il peut déclencher une cascade de gènes « cibles » à l’intérieur de la cellule réceptrice, modifiant son comportement. De nombreux outils existants tentent d’inférer ces interactions à partir de données d’activité génique, mais ils ignorent souvent la localisation physique des cellules. Or, comme beaucoup de signaux agissent sur de courtes distances, perdre ce contexte spatial peut conduire à des résultats trompeurs — laissant croire à une communication entre types cellulaires qui, en réalité, sont éloignés dans le tissu.
Ce qui distingue Renoir
Renoir est conçu spécifiquement pour réintroduire l’espace dans l’équation. Il accepte soit des jeux de données spatiales à résolution monocellulaire, soit une combinaison de données spatiales à résolution plus faible et de données single-cell classiques provenant du même tissu. À partir de listes sélectionnées de ligands et de leurs gènes cibles potentiels, Renoir calcule un « score d’activité de voisinage » pour chaque paire ligand–cible à chaque emplacement du tissu. Ce score combine plusieurs informations : quels types cellulaires sont présents à proximité, à quel degré ils expriment le ligand et le gène cible, si les cellules réceptrices expriment effectivement le récepteur adapté, et dans quelle mesure ligand et cible varient conjointement entre types cellulaires. Le résultat est une carte spatiale qui met en évidence où des relations de signalisation particulières sont susceptibles d’être actives.
Détecter des voisinages cachés dans tissus sains et malades
Une fois les scores de voisinage calculés, Renoir peut regrouper les emplacements en « domaines de communication » — des zones du tissu partageant des schémas de signalisation similaires. Appliqué à des données de cerveau de souris, ces domaines correspondaient aux régions cérébrales connues et ont révélé des communications spécifiques entre astrocytes et différents types de neurones. Dans le cancer du sein triple négatif, Renoir a mis au jour des niches tumorales distinctes où cellules cancéreuses, cellules immunitaires et cellules du tissu conjonctif échangent des signaux liés à la croissance, à l’invasion et à la suppression immunitaire. Dans le foie fœtal humain en développement, il a identifié une niche où les hépatocytes et des macrophages spécialisés interagissent via une molécule appelée plasminogène, suggérant un rôle dans la croissance et le remodelage du foie.
Évaluer Renoir face à d’autres méthodes
Les auteurs ont évalué rigoureusement Renoir en créant des jeux de données semi-synthétiques où les véritables schémas de signalisation étaient connus à l’avance. Ils ont comparé Renoir à plusieurs outils de pointe qui infèrent la communication cellulaire à partir de données spatiales. Dans des tissus tels que l’intestin, le cerveau et le cancer du sein, Renoir distinguait plus précisément les emplacements présentant une réelle activité ligand–cible de ceux n’en ayant pas, et il rapportait moins d’interactions fausses dans des zones dépourvues des récepteurs adéquats. Même lorsque les données étaient rendues plus bruyantes — en réduisant la profondeur de séquençage ou en brouillant certaines annotations cellulaires — les performances de Renoir demeuraient stables. Dans une région bien étudiée du cerveau humain, les domaines de communication inférés par la méthode correspondaient mieux aux couches tissulaires définies par des experts que ceux proposés par d’autres approches.
Des cartes de communication aux pistes thérapeutiques
Renoir n’est pas seulement un outil de cartographie ; il peut aussi classer les ligands les plus influents dans chaque domaine et résumer l’activité de voies de signalisation entières. Dans le cancer du foie, cela a mis en lumière des circuits de signalisation « onco-fœtaux » où des cellules associées à la tumeur réactivent des programmes du développement observés dans le foie fœtal. Renoir a prédit que des ligands comme l’interleukine‑6 issus de cette niche pourraient reprogrammer des cellules hépatiques proches de type souches ; des expériences en laboratoire ont confirmé que l’interleukine‑6 pousse les cellules de cancer du foie vers un état plus proche de la cellule souche. Dans l’ensemble, l’étude montre comment la combinaison de la génomique spatiale et d’un calcul intelligent peut transformer des cartes géniques statiques en portraits dynamiques du dialogue cellulaire, offrant de nouvelles pistes pour des thérapies visant à perturber les conversations néfastes tout en préservant les échanges bénéfiques.
Citation: Rao, N., Kumar, T., Kazemi, D. et al. Charting spatial ligand-target activity using Renoir. Nat Commun 17, 3983 (2026). https://doi.org/10.1038/s41467-026-72388-7
Mots-clés: transcriptomique spatiale, communication cellulaire, signalisation par ligands, microenvironnement tumoral, biologie computationnelle
En savoir plus sur le site web de l'équipe de recherche: https://sites.google.com/view/cosmiclab-iitk/home