Clear Sky Science · fr
Viser le domaine de transactivation intrinsèquement désordonné du récepteur des androgènes
Pourquoi cette nouvelle approche contre le cancer de la prostate est importante
Beaucoup de cancers de la prostate avancés finissent par contourner les meilleurs médicaments disponibles aujourd’hui. La plupart des traitements actuels agissent en bloquant une poche rigide du récepteur des androgènes, une protéine qui alimente la croissance tumorale. Les tumeurs s’adaptent fréquemment en produisant des versions altérées de ce récepteur qui n’ont plus cette poche, rendant les médicaments standards inefficaces. Cette étude explore une alternative audacieuse : concevoir des médicaments qui s’attachent à une portion souple et changeante à l’autre extrémité du récepteur, longtemps considérée comme « indrogable », et montre que cette stratégie peut fortement arrêter la croissance tumorale en laboratoire et chez l’animal.
Une région protéique flexible jadis jugée hors de portée
Le récepteur des androgènes contrôle la croissance et la survie des cellules prostatiques en activant ou en réprimant des gènes. Son extrémité avant, appelée domaine de transactivation, est exceptionnellement longue et n’a pas de forme 3D fixe. Elle se comporte plutôt comme un filament flexible, explorant constamment de nombreuses conformations. Ce type de région, qualifié d’intrinsèquement désordonné, a été considéré comme un cauchemar pour les développeurs de médicaments, qui cherchent traditionnellement des poches bien définies où les molécules peuvent se loger. Pourtant, ce segment flexible est crucial : il interagit avec des centaines de protéines partenaires et reste intact même dans des variantes du récepteur résistantes aux médicaments qui n’ont pas la poche habituelle. Cela en fait une cible attrayante — si difficile — pour de nouvelles thérapies.
Affiner des composés de première classe
Les chercheurs ont conçu et testé une grande collection de petites molécules, appelées inhibiteurs du domaine de transactivation de l’AR (ARTADIs), dérivées de candidats cliniques antérieurs tels que la ralanitène et la masofanitène. En ajustant des caractéristiques comme des atomes d’halogène sur des anneaux aromatiques, en supprimant ou ajoutant certains groupes alcool et en modulant la liposolubilité, ils ont suivi systématiquement comment de petits changements chimiques modifiaient la puissance, la sélectivité et le comportement dans les cellules et chez la souris. Certaines modifications, comme des groupes contenant du chlore spécifiques, ont généralement renforcé l’activité sur cible et aidé à épargner les cellules qui ne dépendent pas du récepteur des androgènes. Au fil de cycles de synthèse et de tests, ils ont identifié des composés de nouvelle génération — en particulier un nommé BU3-12 et un autre nommé BU170 — qui surpassaient les versions précédentes et, dans certains contextes, rivalisaient avec ou dépassaient le médicament standard enzalutamide.
Bloquer à la fois la signalisation classique et résistante aux médicaments
Les tumeurs prostatiques échappent souvent aux thérapies en produisant des variantes raccourcies du récepteur, telles que AR-V7, qui n’ont pas la poche de liaison habituelle mais restent constamment actives. L’enzalutamide ne peut pas agir sur ces variantes. En revanche, plusieurs ARTADIs ont efficacement supprimé l’activité à la fois du récepteur des androgènes en pleine longueur et de AR-V7 dans plusieurs lignées cellulaires de cancer de la prostate. Ils ont réduit l’expression des gènes qui stimulent la division et la survie cellulaires, et ralenti ou arrêté la croissance de tumeurs implantées chez la souris, y compris des modèles dépendants d’AR-V7 et résistants à l’enzalutamide. Chez des animaux dont les tumeurs étaient alimentées par des niveaux normaux de testostérone, les ARTADIs ont conservé une forte activité et, dans certains cas, surpassé l’enzalutamide, suggérant qu’ils pourraient être particulièrement utiles plus tôt dans l’évolution de la maladie.
Comment ces molécules s’agrippent à une cible changeante
Pour comprendre comment ces médicaments agissent sur une région si flexible, l’équipe a purifié le segment de transactivation désordonné du récepteur et mesuré la liaison directement. Des tests biophysiques ont montré que les principaux ARTADIs se liaient avec une force remarquable, avec des affinités apparentes dans la gamme picomolaire à bas nanomolaire, comparables ou supérieures aux médicaments haut de gamme ciblant des poches rigides. Des études cinétiques détaillées ont révélé au moins deux états de liaison : une rencontre rapide et non permanente suivie d’une association beaucoup plus stable. Sur des durées plus longues, la spectrométrie de masse a détecté que certains ARTADIs formaient des liens covalents avec une cystéine spécifique de la région désordonnée, « épinglant » effectivement le médicament au récepteur. Cet ancrage sélectif aide probablement à verrouiller la protéine dans des conformations moins actives et rend l’inhibition durable même lorsque les cellules renouvellent continuellement les molécules du récepteur.
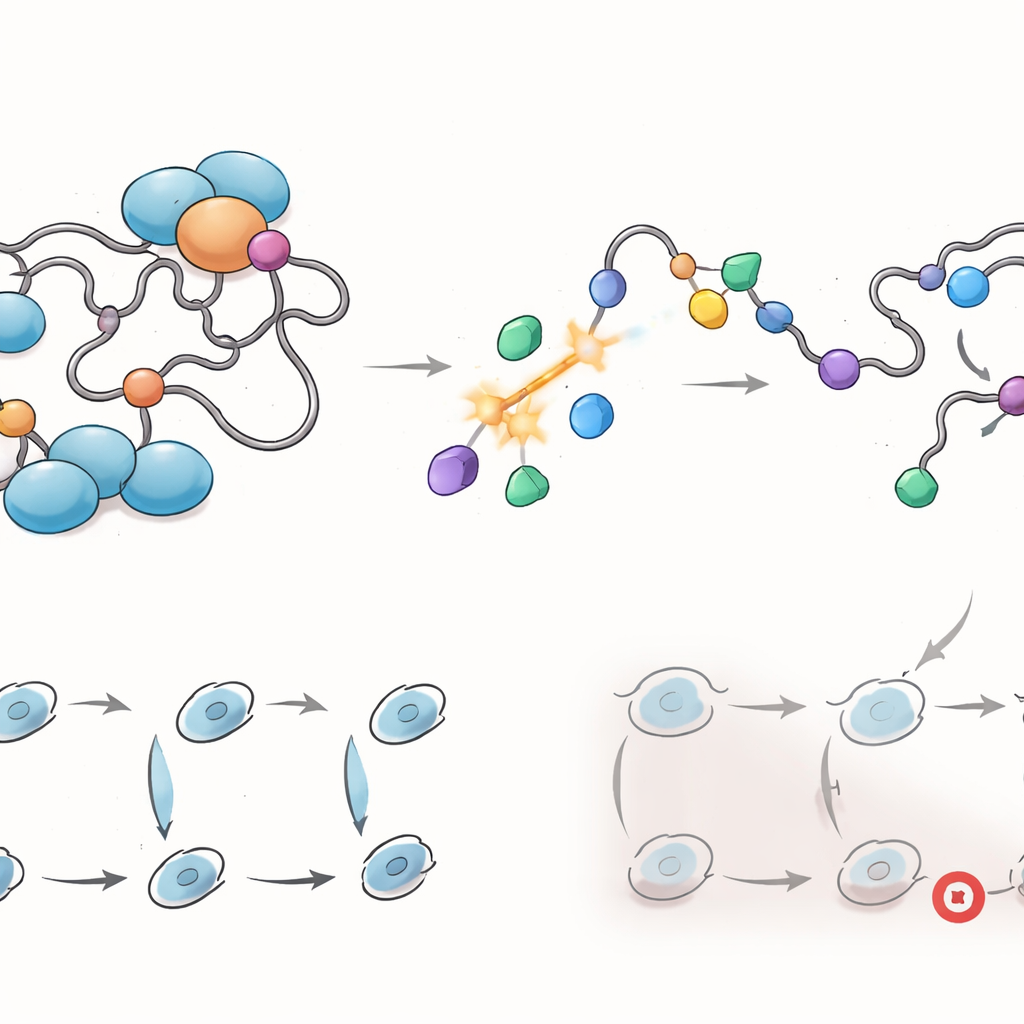
Reconfigurer les programmes génétiques et les réseaux de partenaires
Parce que le domaine de transactivation orchestre de nombreuses interactions, les chercheurs ont examiné comment les ARTADIs reconfiguraient le réseau du récepteur. À l’aide d’un séquençage ARN à l’échelle du génome, ils ont constaté que ces composés atténuaient largement des programmes génétiques liés à la progression du cycle cellulaire, à la réparation de l’ADN et à la ségrégation des chromosomes — moteurs clés de la croissance tumorale — de façons différentes de l’enzalutamide. Des essais cellulaires ont confirmé que certains ARTADIs forçaient les cellules cancéreuses à marquer une pause à des points distincts du cycle de division et, dans certains cas, déclenchaient des signaux de dommages à l’ADN. La cartographie des interactions protéiques a montré que les ARTADIs perturbaient les contacts entre le récepteur et plusieurs co-régulateurs connus, y compris des facteurs qui l’aident à se lier à l’ADN et à remodeler la chromatine, et, de façon cruciale, bloquaient des interactions impliquant AR-V7 que l’enzalutamide ne pouvait pas atteindre.
Ce que cela signifie pour le traitement futur du cancer de la prostate
Ce travail démontre qu’une cible désordonnée et mobile sur une protéine clé du cancer peut, en réalité, être ciblée par un médicament avec une grande spécificité et puissance. En se liant et parfois en se verrouillant de façon covalente sur l’extrémité avant flexible du récepteur des androgènes, les ARTADIs réduisent à la fois la signalisation normale et résistante aux médicaments, modifient des voies critiques de croissance et de réparation, et ralentissent les tumeurs dans des modèles animaux, même lorsque les niveaux d’hormones mâles sont élevés. Pour les patients, cette stratégie pourrait un jour compléter ou remplacer les thérapies actuelles, retardant l’apparition de résistances et offrant des options efficaces même après l’échec des médicaments ciblant la poche habituelle du récepteur.
Citation: Obst, J.K., Banuelos, C.A., Jian, K. et al. Drugging the intrinsically disordered transactivation domain of androgen receptor. Sig Transduct Target Ther 11, 157 (2026). https://doi.org/10.1038/s41392-026-02642-3
Mots-clés: cancer de la prostate, récepteur des androgènes, protéines intrinsèquement désordonnées, résistance aux médicaments, régulation transcriptionnelle