Clear Sky Science · ar
استهداف نطاق التنشيط غير المنظم جوهرياً لمستقبل الأندروجين
لماذا تهم هذه المقاربة الجديدة لسرطان البروستات
في مراحل متقدمة، يتغلب العديد من سرطانات البروستات في نهاية المطاف على أفضل الأدوية المتاحة اليوم. تعمل معظم العلاجات الحالية عن طريق حجب جيب صارم في مستقبل الأندروجين، وهو بروتين يغذي نمو الورم. كثيراً ما تتكيف الأورام بإنتاج نسخ معدلة من هذا المستقبل تفقد ذلك الجيب، مما يجعل الأدوية القياسية غير فعالة. تستكشف هذه الدراسة بديلًا جريئًا: تصميم أدوية تلتصق بجزء مرن متغير الشكل عند الطرف الآخر للمستقبل، والذي طالما اعتُبر "غير قابل للعلاج"، وتُظهر أن هذه الاستراتيجية قادرة بقوة على إيقاف نمو السرطان في المختبر وفي نماذج حيوانية.
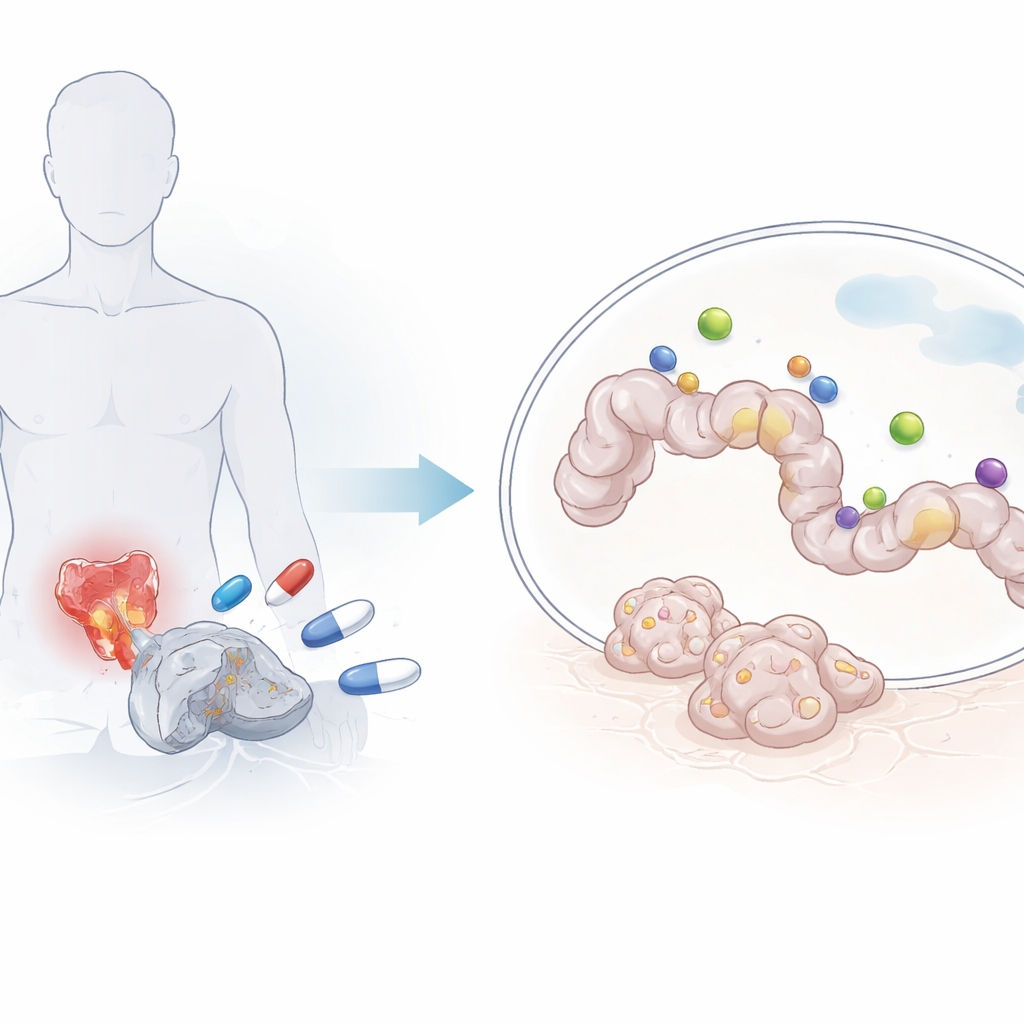
منطقة بروتينية مرنة كانت تُعتبر خارج نطاق الوصول
يتحكم مستقبل الأندروجين في كيفية نمو خلايا البروستات وبقائها من خلال تشغيل وإطفاء الجينات. الطرف الأمامي منه، المسمى نطاق التنشيط النسخي، طويل بشكل غير عادي ويفتقر إلى شكل ثلاثي الأبعاد ثابت. بدلاً من ذلك، يتصرف مثل «معكرونة» مرنة، مستكشفًا باستمرار العديد من التشكلات. هذا النوع من المناطق، المعروف بالبلا ترتيب الجوهرية، اعتُبر هدفًا مرعبًا لمطوري الأدوية، الذين يفضلون عادة جيوبًا محددة يمكن للجزيئات أن تستقر فيها. ومع ذلك، فإن هذا الجزء المرن حاسم: يتفاعل مع المئات من البروتينات الشريكة ويظل سليمًا حتى في متغيرات المستقبل المقاومة للأدوية التي تفتقد الجيب المعتاد لارتباط الدواء. وهذا يجعله هدفًا جذابًا — وإن كان صعبًا — للعلاجات الجديدة.
ضبط مركبات من الجيل الأول
بنى الباحثون واختبروا مجموعة كبيرة من الجزيئات الصغيرة، تسمى مثبطات نطاق التنشيط لمستقبل الأندروجين (ARTADIs)، مستمدة من مرشحات سريرية سابقة مثل رالانيتن وماسوفانيتن. من خلال تعديل خصائص مثل ذرات الهالوجين على الحلقات العطرية، إزالة أو إضافة مجموعات كحولية معينة، وتعديل الذوبان الدهني الجزيئي، تتبعوا بشكل منهجي كيف غيّرت تغييرات كيميائية ضئيلة الفعالية والانتقائية والسلوك في الخلايا والفئران. بعض التعديلات، مثل مجموعات تحتوي على الكلورين محددة، عززت عمومًا النشاط على الهدف وساعدت في حماية الخلايا التي لا تعتمد على مستقبل الأندروجين. عبر جولات من التصنيع والاختبار، حددوا مركبات من الجيل التالي — خاصة واحدًا اسمه BU3-12 وآخر اسمه BU170 — تفوقت على النسخ السابقة وفي بعض الحالات ضاهت أو تفوقت على الدواء القياسي إنزالوتاميد.
حجب الإشارات الكلاسيكية والمقاومة للأدوية على حد سواء
غالبًا ما تفلت أورام البروستات من العلاج عن طريق إنتاج متغيرات مستقبل قصيرة مثل AR-V7 التي تفتقد الجيب المعتاد لارتباط الدواء لكنها تظل نشطة بشكل مستمر. إنزالوتاميد لا يؤثر على هذه المتغيرات. في المقابل، كبَحت عدة من ARTADIs نشاط كل من مستقبل الأندروجين الكامل الطول وAR-V7 بفعالية في خطوط خلوية متعددة لسرطان البروستات. خفضت هذه المركبات التعبير عن الجينات التي تدفع انقسام الخلايا وبقائها، وأبطأت أو أوقفت نمو الأورام المزروعة في الفئران، بما في ذلك نماذج تعتمد على AR-V7 ومقاومة لإنزالوتاميد. في الحيوانات التي تغذت أورامها على مستويات طبيعية من التستوستيرون، احتفظت ARTADIs بنشاط قوي وفي بعض الحالات تفوقت على إنزالوتاميد، مما يشير إلى أنها قد تكون ذات قيمة خاصة في مراحل مبكرة من المرض.
كيف تمسك هذه الجزيئات بهدف متقلب الشكل
لفهم كيف تعمل هذه الأدوية على منطقة مرنة كهذه، نقّى الفريق جزء التنشيط غير المنظم من المستقبل وقاس ارتباطه مباشرة. أظهرت الاختبارات الفيزيائية الحيوية أن ARTADIs الرائدة ارتبطت بقوة ملحوظة، مع تقارب ظاهري في نطاق بيكومولار إلى نانومولار منخفض، قابل للمقارنة أو أفضل من الأدوية الراقية التي تستهدف الجيوب الصارمة. كشفت دراسات حركية مفصلة عن حالتي ارتباط على الأقل: لقاء سريع وغير دائم يتبعه ارتباط أكثر استقرارًا بكثير. على مدى أزمنة أطول، رصدت مطيافية الكتلة أن بعض ARTADIs شكلت روابط تساهمية مع حمض أميني سيستئين محدد داخل المنطقة غير المنظمة، مثبتةً فعليًا الدواء على المستقبل. من المرجح أن هذا الترسيخ الانتقائي يساعد على قفل البروتين في أشكال أقل نشاطًا ويجعل التثبيط دائمًا حتى مع تجدد جزيئات المستقبل في الخلايا.
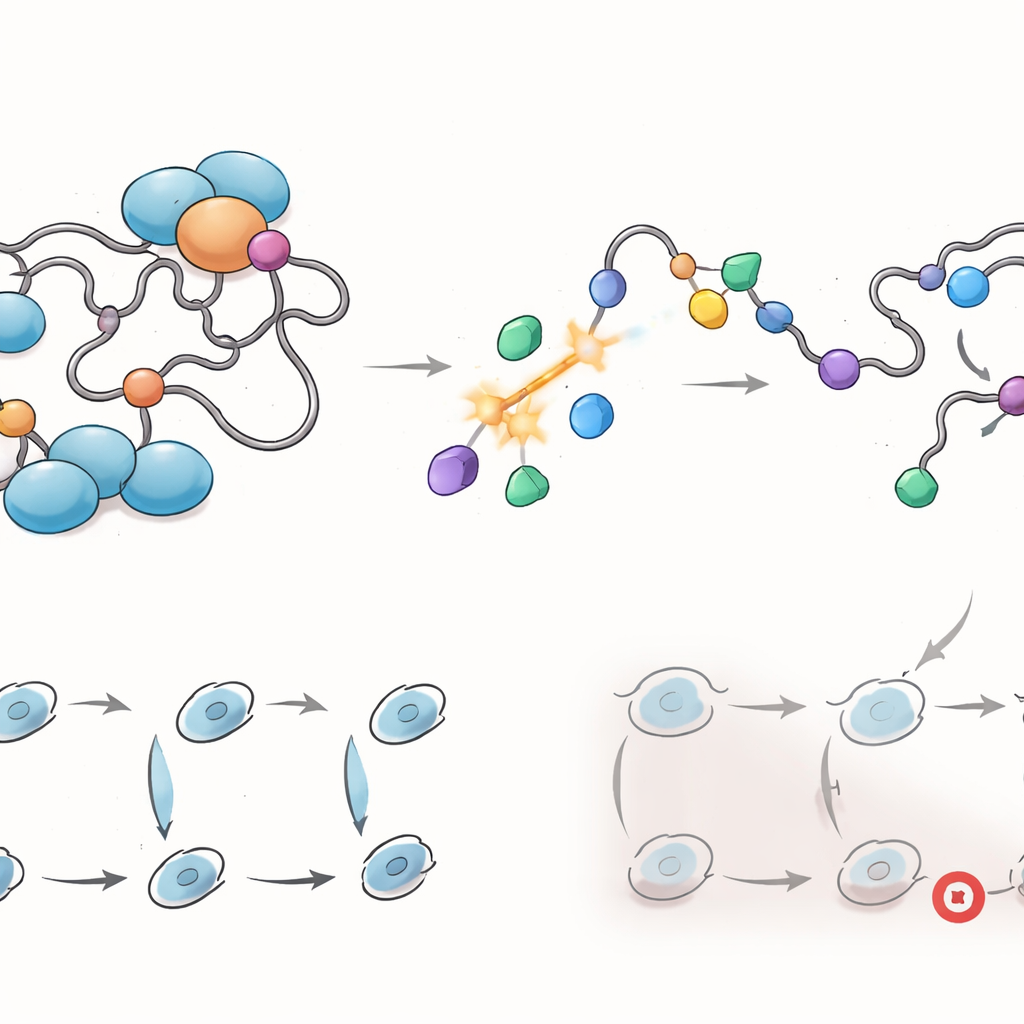
إعادة توصيل برامج الجينات وشبكات الشركاء
بما أن نطاق التنشيط ينسق العديد من الشراكات، فحص الباحثون كيف تعيد ARTADIs تشكيل شبكة المستقبل. باستخدام تسلسل الرنا على مستوى الجينوم، وجدوا أن هذه المركبات تخفض على نطاق واسع برامج جينية مرتبطة بتقدم دورة الخلية وإصلاح الحمض النووي وفصل الكروموسومات — محركات رئيسية لنمو الورم — بطرق تختلف عن إنزالوتاميد. أكدت تجارب خلوية أن ARTADIs محددة أجبرت خلايا السرطان على التوقف عند نقاط مميزة في دورة الانقسام وفي بعض الحالات أثارت إشارات تلف الحمض النووي. أظهر رسم تفاعلات البروتين أن ARTADIs قوضت اتصالات بين المستقبل والعديد من المنظمات المساعدة المعروفة، بما في ذلك عوامل تساعده على ربط الحمض النووي وإعادة تشكيل الكروماتين، والأهم من ذلك، حجبت تفاعلات تشمل AR-V7 التي لا تستطيع إنزالوتاميد الوصول إليها.
ماذا يعني هذا لعلاج مستقبل سرطان البروستات
تُظهر هذه الدراسة أن هدفًا غير منظم ومتحرك على بروتين سرطان رئيسي يمكن، في الواقع، استهدافه بدقة وقوة عاليتين. من خلال الارتباط وأحيانًا القفل التساهمي على الطرف المرن لمستقبل الأندروجين، تقلل ARTADIs من الإشارات الطبيعية والمقاومة للأدوية، وتغيّر مسارات النمو والإصلاح الحرجة، وتبطئ الأورام في نماذج حيوانية، حتى عندما تكون مستويات الهرمونات الذكرية مرتفعة. بالنسبة للمرضى، قد تكمل هذه الاستراتيجية يومًا ما العلاجات الحالية أو تحل محلها، مما يؤخر تطور المقاومة ويقدم خيارات تعمل حتى بعد فشل الأدوية التي تستهدف جيب المستقبل التقليدي.
الاستشهاد: Obst, J.K., Banuelos, C.A., Jian, K. et al. Drugging the intrinsically disordered transactivation domain of androgen receptor. Sig Transduct Target Ther 11, 157 (2026). https://doi.org/10.1038/s41392-026-02642-3
الكلمات المفتاحية: سرطان البروستات, مستقبل الأندروجين, البروتينات غير المنظمة جوهرياً, مقاومة الأدوية, تنظيم النسخ الجيني