Clear Sky Science · fr
Activation transcriptionnelle médiée par TWIST1 de SPON2 favorisant les métastases péritonéales du cancer colorectal via un réseau de signalisation du stroma
Pourquoi cette étude importe pour les personnes atteintes d’un cancer du côlon
Lorsque le cancer du côlon ou du rectum se propage dans la cavité abdominale, en recouvrant les intestins et d’autres organes, il devient l’une des formes les plus mortelles de la maladie. La chimiothérapie standard et même la chirurgie agressive la guérissent rarement. Cette étude pose une question fondamentale mais urgente : quelle conversation moléculaire cachée entre les cellules tumorales et leur environnement rend ce type de diffusion si difficile à arrêter — et cette conversation peut‑elle être interrompue ?
Une dissémination mortelle à l’intérieur de l’abdomen
Le cancer colorectal qui ensemence la paroi de l’abdomen, appelé métastase péritonéale, touche jusqu’à un tiers des patients en phase avancée et présente un pronostic sombre, avec une survie à cinq ans proche de zéro. Les chirurgiens peuvent parfois enlever les tumeurs visibles et traiter l’abdomen par chimiothérapie chauffée, mais de minuscules foyers résistants persistent presque toujours et repoussent. Les auteurs soutiennent que pour améliorer les résultats, il faut comprendre non seulement les cellules tumorales elles‑mêmes, mais aussi l’environnement unique du péritoine et la manière dont il favorise la croissance, la dissémination et l’évasion thérapeutique du cancer.
Un signal en trois étapes qui met les tumeurs en surmultiplication
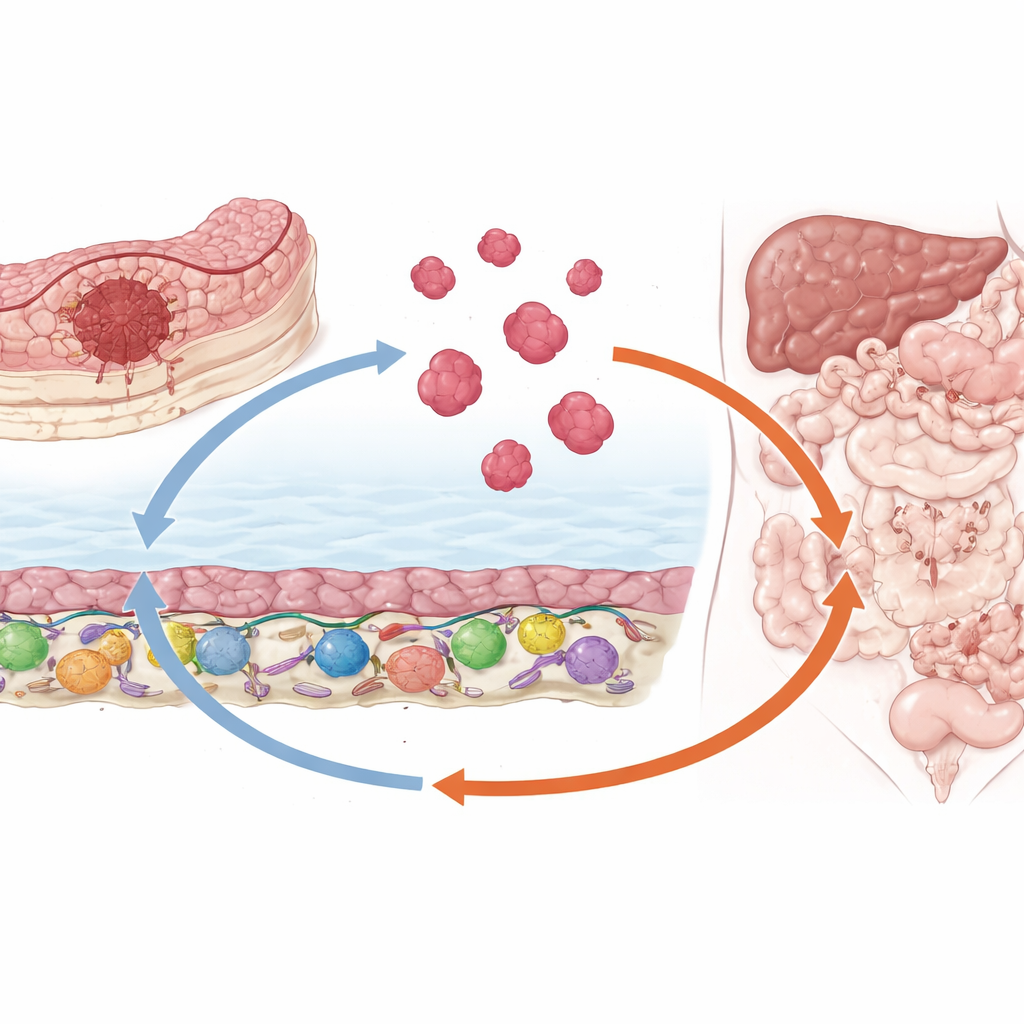
À l’aide d’échantillons de patients, de méthodes avancées de lecture des gènes et de modèles murins, les chercheurs ont mis au jour une chaîne de signalisation en trois maillons qui semble piloter ce schéma dangereux de dissémination. D’abord, des cellules du tissu de soutien qui tapisse l’abdomen libèrent un messager protéique appelé SPP1. Les cellules de cancer colorectal voisines détectent ce signal et activent un régulateur génique nommé TWIST1, connu pour aider les cellules à relâcher leurs attachements et à devenir plus mobiles. TWIST1 active à son tour la production d’une autre protéine sécrétée, SPON2. Ensemble, TWIST1 et SPON2 rendent les cellules cancéreuses plus aptes à migrer, envahir les tissus environnants et former des amas tridimensionnels qui ressemblent aux « graines » résistantes observées dans la cavité abdominale des patients.
Comment le cancer remodelle son voisinage
L’histoire ne s’arrête pas à la cellule tumorale. SPON2, une fois sécrétée par les cellules tumorales, agit en retour sur les cellules stromales environnantes — y compris les cellules mésothéliales qui forment la couche glissante de l’abdomen — et les pousse vers un état plus fibreux et favorable au cancer, semblable à des fibroblastes activés. Ces cellules stromales remodelées produisent à leur tour encore plus de SPP1, bouclant une rétroaction auto‑renforçante entre la tumeur et le stroma. Cette boucle épaissit les tissus avec du collagène et d’autres composants de la matrice et inonde l’espace de signaux pro‑croissance, des conditions qui favorisent l’expansion tumorale et l’accumulation de liquide (ascite) qui provoque souvent des symptômes sévères chez les patients.
Bloquer la boucle ralentit les tumeurs et favorise l’attaque immunitaire
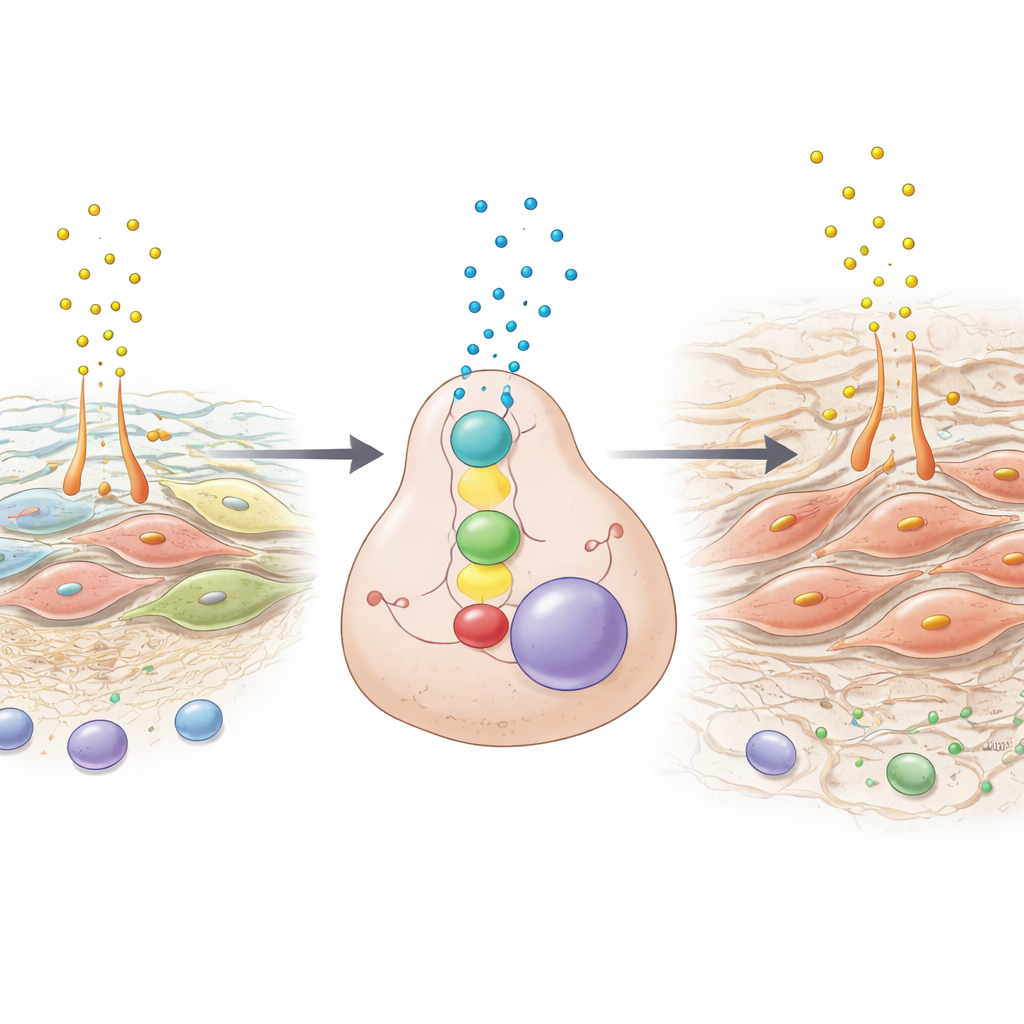
Dans des modèles murins qui reproduisent fidèlement les métastases péritonéales humaines, l’équipe a désactivé des éléments individuels de ce circuit. L’inactivation de TWIST1 ou de SPON2 dans les cellules tumorales, ou la suppression de SPP1 dans les cellules stromales hôtes, a réduit nettement le nombre et la taille des foyers tumoraux abdominaux, diminué l’accumulation de liquide et aminci le stroma fibreux. Parallèlement, les tumeurs sont devenues plus accessibles au système immunitaire : on a observé une augmentation marquée des cellules CD8 cytotoxiques infiltrant la tumeur, sans changements majeurs dans d’autres types cellulaires immunitaires. Des expériences en laboratoire ont montré que des médicaments bloquant la voie PI3K–AKT — un signal de croissance clé activé par SPP1 — pouvaient également atténuer TWIST1 et SPON2, suggérant des pistes par lesquelles des agents existants pourraient affaiblir ce dialogue malin.
Ce que cela pourrait signifier pour les traitements futurs
Pour un non‑spécialiste, l’essentiel de ce travail est que les auteurs ont cartographié une conversation spécifique en trois étapes — SPP1 vers TWIST1 vers SPON2 — entre les cellules du cancer colorectal et la paroi abdominale qui aide le cancer à se propager, à construire un tissu de soutien cicatriciel, à se protéger des attaques immunitaires et à générer des ascites. En perturbant n’importe quel maillon de cette chaîne, les tumeurs chez la souris deviennent plus petites, moins fibreuses et plus vulnérables aux cellules immunitaires. Cela suggère que la mesure de ces protéines pourrait aider à identifier les patients à haut risque, et que des thérapies ciblant SPP1, TWIST1, SPON2 ou les voies de signalisation qu’ils contrôlent pourraient un jour transformer un mode de dissémination presque intraitable en une maladie plus gérable.
Citation: Zhou, Z., La Ferlita, A., Palavalli, M.H. et al. TWIST1 mediated transcriptional activation of SPON2 drives colorectal cancer peritoneal metastasis through stromal cell signaling network. Oncogene 45, 1613–1626 (2026). https://doi.org/10.1038/s41388-026-03743-7
Mots-clés: cancer colorectal, métastases péritonéales, microenvironnement tumoral, TWIST1 SPON2 SPP1, stroma tumoral