Clear Sky Science · de
TWIST1-vermittelte transkriptionelle Aktivierung von SPON2 treibt peritoneale Metastasierung beim kolorektalen Karzinom durch ein Signalnetzwerk des Stromas voran
Warum diese Studie für Menschen mit Darmkrebs wichtig ist
Wenn sich Darm- oder Rektumkrebs in die Bauchhöhle ausbreitet und Darm und andere Organe überzieht, zählt dies zu den tödlichsten Formen der Erkrankung. Standardchemotherapie und selbst aggressive Operationen heilen sie nur selten. Diese Studie stellt eine einfache, aber dringende Frage: Welcher verborgene molekulare Dialog zwischen Tumorzellen und ihrer Umgebung macht diese Form der Ausbreitung so schwer zu stoppen — und lässt sich dieser Dialog unterbrechen?
Eine tödliche Ausbreitung im Bauchraum
Kolorektaler Krebs, der die Bauchfellschicht besiedelt (peritoneale Metastasierung), betrifft bis zu einem Drittel der Patientinnen und Patienten mit fortgeschrittener Erkrankung und hat eine düstere Prognose, mit einer Fünfjahresüberlebensrate nahe null. Chirurgen können manchmal sichtbare Tumoren entfernen und die Bauchhöhle mit erhitzter Chemotherapie behandeln, aber winzige resistente Ablagerungen verbleiben fast immer und wachsen nach. Die Autoren argumentieren, dass wir zur Verbesserung der Ergebnisse nicht nur die Tumorzellen selbst verstehen müssen, sondern auch die einzigartige Umgebung des Peritoneums und wie sie das Krebswachstum, die Ausbreitung und die Therapieumgehung fördert.
Ein dreiteiliges Signal, das Tumoren hochfährt
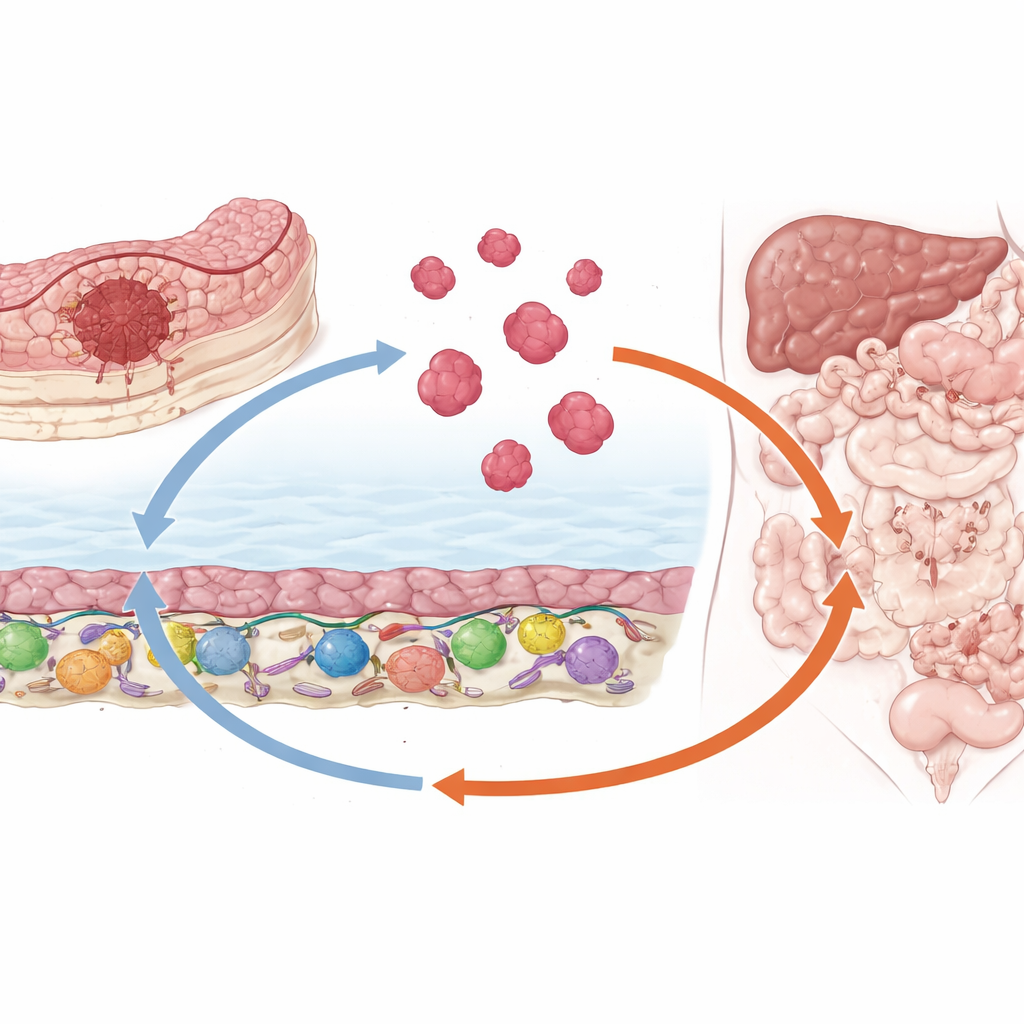
Mithilfe von Patientenproben, ausgefeilten Genexpressionsmethoden und Mausmodellen entdeckten die Forschenden eine dreigliedrige Signalkette, die offenbar dieses gefährliche Ausbreitungsmuster antreibt. Zunächst setzen Zellen des stützenden Gewebes, das die Bauchhöhle auskleidet, einen Proteinboten namens SPP1 frei. Nahegelegene kolorektale Tumorzellen nehmen dieses Signal wahr und schalten einen Genregulator namens TWIST1 ein, der dafür bekannt ist, Zellen zu lockern und beweglicher zu machen. TWIST1 aktiviert seinerseits die Produktion eines weiteren sekretierbaren Proteins, SPON2. Gemeinsam fördern TWIST1 und SPON2 die Wanderung der Tumorzellen, ihr Eindringen in umliegendes Gewebe und die Bildung dreidimensionaler Cluster, die den resistenten "Samen" ähneln, den man in der Bauchhöhle von Patientinnen und Patienten findet.
Wie der Krebs seine Nachbarschaft umgestaltet
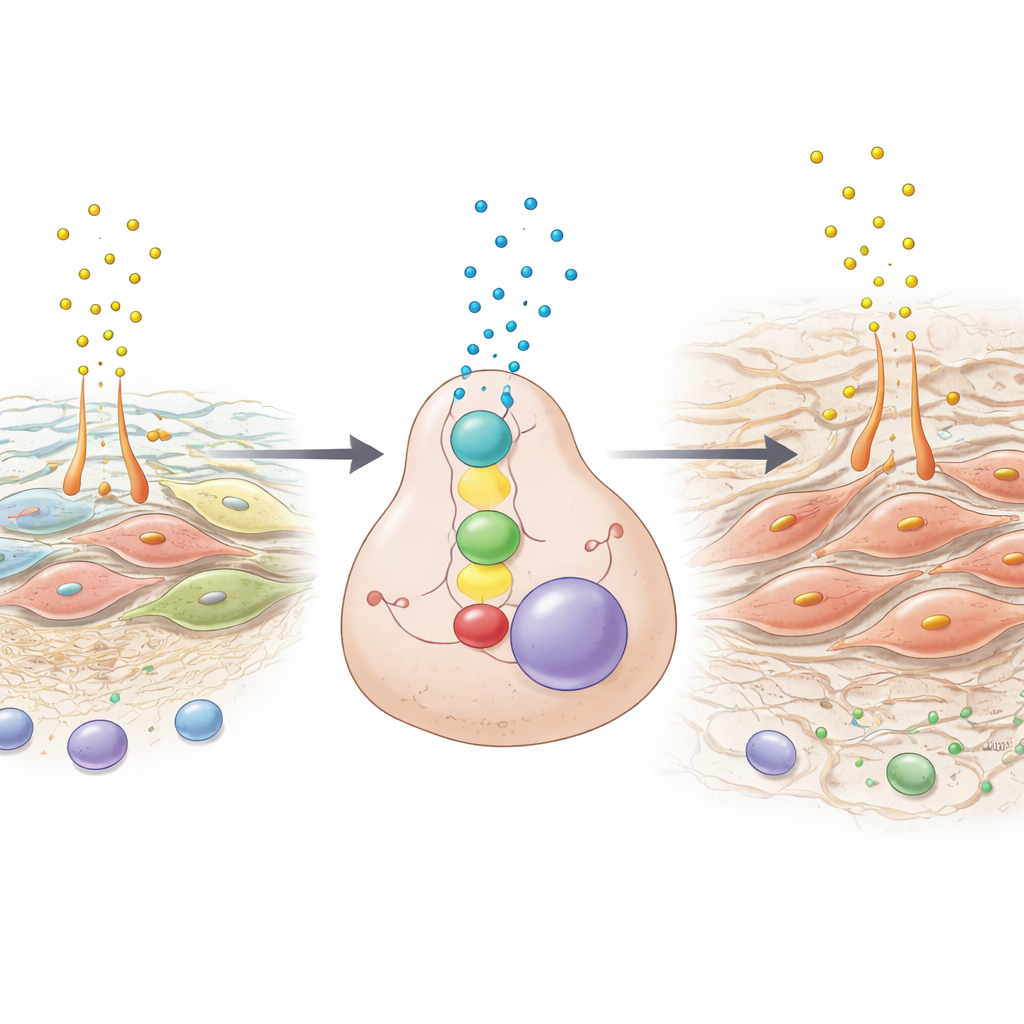
Die Geschichte endet nicht bei der Tumorzelle. SPON2, einmal von Tumorzellen ausgeschieden, wirkt zurück auf die umliegenden Stromazellen — einschließlich Mesothelzellen, die die gleitende Auskleidung der Bauchhöhle bilden — und drängt sie in einen faserigeren, krebsunterstützenden Zustand, ähnlich aktivierten Fibroblasten. Diese umgestalteten Stromazellen produzieren wiederum noch mehr SPP1 und schließen damit eine selbstverstärkende Schleife zwischen Tumor und Stroma. Die Schleife verdickt das Gewebe mit Kollagen und anderen Matrixkomponenten und flutet den Raum mit wachstumsfördernden Signalen — Bedingungen, die Tumorwachstum und die Ansammlung von Aszites begünstigen, die bei Patientinnen und Patienten oft schwere Beschwerden verursacht.
Den Kreislauf zu blockieren verlangsamt Tumoren und lädt das Immunsystem ein
In Mausmodellen, die die menschliche peritoneale Metastasierung gut nachbilden, schaltete das Team einzelne Teile dieser Schaltung aus. Die Deletion von TWIST1 oder SPON2 in Tumorzellen oder das Entfernen von SPP1 aus den stromalen Wirtszellen verringerte deutlich Anzahl und Größe der Bauchraumtumoren, reduzierte die Flüssigkeitsansammlung und dünnte das faserige Stroma aus. Gleichzeitig wurden die Tumoren für das Immunsystem zugänglicher: Es gab einen deutlichen Anstieg krebsabtötender CD8-T-Zellen im Tumor, ohne größere Veränderungen anderer Immunzelltypen. Laborexperimente zeigten, dass Medikamente, die den PI3K–AKT-Weg blockieren — ein Schlüsselsignal, das durch SPP1 aktiviert wird — auch TWIST1 und SPON2 abschwächen können, was auf mögliche Wege hinweist, wie vorhandene Wirkstoffe diesen malignen Dialog schwächen könnten.
Was das für künftige Behandlungen bedeuten könnte
Für Laien lässt sich das Wesentliche dieser Arbeit so zusammenfassen: Die Autoren haben einen spezifischen dreistufigen Dialog — SPP1 zu TWIST1 zu SPON2 — zwischen Darmkrebszellen und der Bauchfellschicht kartiert, der dem Krebs hilft, sich auszubreiten, narbenähnendes Stützgewebe aufzubauen, dem Immunsystem die Zugänge zu versperren und Aszites zu erzeugen. Wird eine Verbindung dieser Kette unterbrochen, werden Tumoren bei Mäusen kleiner, weniger fibrotisch und anfälliger für Immunzellen. Das deutet darauf hin, dass das Messen dieser Proteine helfen könnte, Hochrisikopatienten zu identifizieren, und dass Therapien, die auf SPP1, TWIST1, SPON2 oder die von ihnen gesteuerten Signalwege abzielen, eines Tages ein bisher kaum behandelbares Muster der Ausbreitung in eine besser beherrschbare Erkrankung verwandeln könnten.
Zitation: Zhou, Z., La Ferlita, A., Palavalli, M.H. et al. TWIST1 mediated transcriptional activation of SPON2 drives colorectal cancer peritoneal metastasis through stromal cell signaling network. Oncogene 45, 1613–1626 (2026). https://doi.org/10.1038/s41388-026-03743-7
Schlüsselwörter: kolorektales Karzinom, peritoneale Metastasierung, Tumormikroumgebung, TWIST1 SPON2 SPP1, Krebsstroma