Clear Sky Science · es
El impacto del óxido de grafeno en las propiedades magnéticas e hipertermia de las ferritas CoFe2O4 y MnFe2O4
Calentar tumores con imanes diminutos
Los oncólogos saben desde hace tiempo que elevar ligeramente la temperatura de un tumor puede aumentar la eficacia de tratamientos como la quimioterapia y la radioterapia. Este estudio explora una nueva forma de generar ese calor desde el interior del cuerpo usando partículas magnéticas diminutas. Al comparar dos tipos de partículas y mezclarlas con láminas de carbono ultrafinas, los investigadores buscan materiales que calienten los tumores de forma eficiente y que sigan siendo fáciles de administrar y controlar.
Por qué el calor magnético puede ayudar a tratar el cáncer
En lugar de irradiar con microondas o luz desde el exterior, la hipertermia magnética se basa en nanopartículas que se calientan cuando se sitúan en un campo magnético variable. Si estas partículas se inyectan cerca de un tumor, el campo puede activarse desde fuera del cuerpo y las partículas actúan como pequeños calentadores, elevando la temperatura local solo unos grados por encima de la normal. El reto es diseñar partículas que generen suficiente calor a intensidades y frecuencias de campo seguras para los pacientes, manteniéndose bien dispersas en los fluidos corporales y presentando toxicidad mínima.
Dos materiales magnéticos bajo el microscopio
El equipo se centró en dos compuestos a base de hierro: ferrita de manganeso (MnFe2O4) y ferrita de cobalto (CoFe2O4). Ambas son imanes diminutos, pero se comportan de forma muy distinta. La ferrita de manganeso es un imán “blando”, lo que significa que su magnetización interna puede invertirse con relativa facilidad. La ferrita de cobalto es un imán “duro”, cuya magnetización está fuertemente bloqueada. Las nanopartículas se sintetizaron en agua mediante un método hidrotermal y se examinaron con difracción de rayos X y microscopía electrónica para confirmar su estructura, forma y tamaño. Las partículas de MnFe2O4 fueron en su mayoría cubos y cuboides de unos 20 a 30 nanómetros, mientras que las de CoFe2O4 eran más pequeñas y esféricas, alrededor de 14 nanómetros.
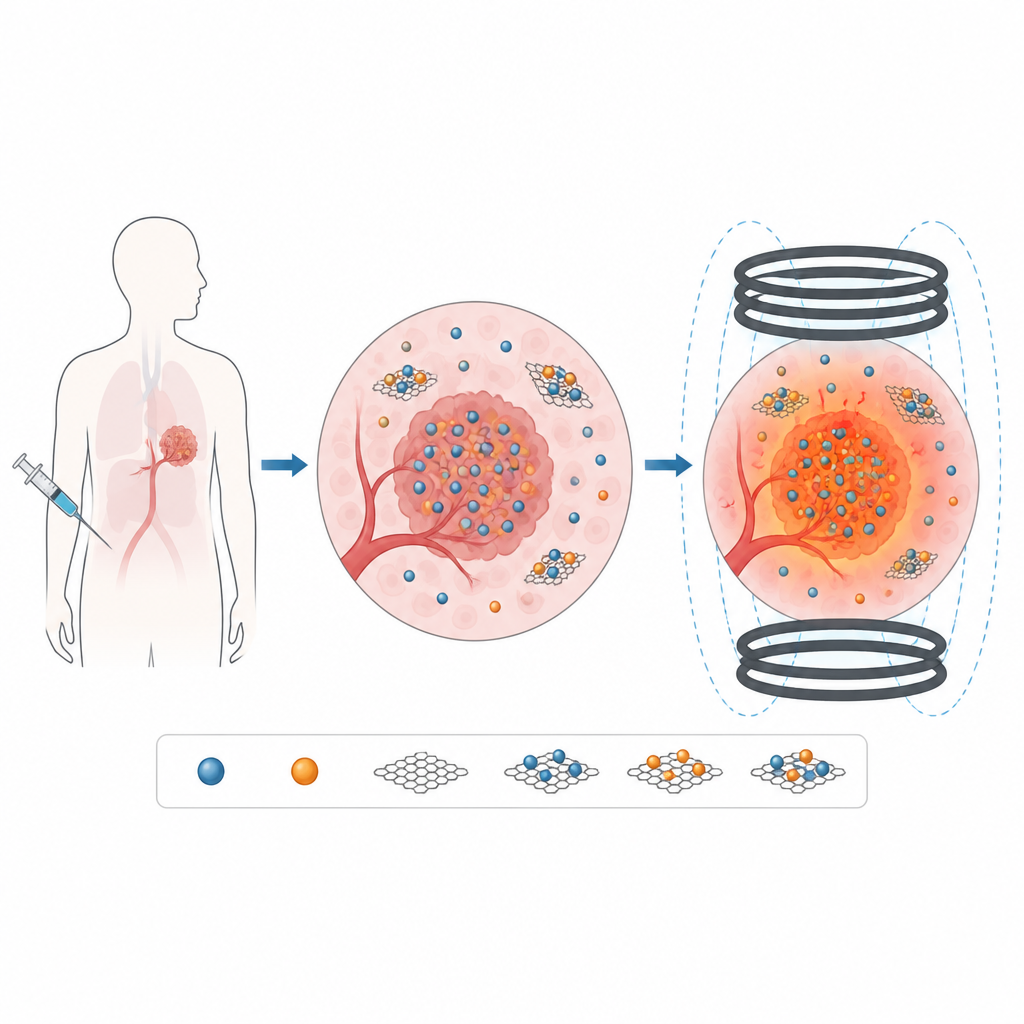
Añadir óxido de grafeno: ayuda y perjuicio
Para mejorar la estabilidad en líquido y crear una superficie que posteriormente pueda funcionalizarse con fármacos o moléculas diana, los investigadores anclaron las nanopartículas de ferrita sobre láminas de óxido de grafeno, un material de carbono plano rico en grupos oxigenados. Las imágenes mostraron partículas de MnFe2O4 y CoFe2O4 distribuidas sobre las láminas flexibles en lugar de aglomerarse. La espectroscopía confirmó que los enlaces químicos tanto en las ferritas como en el óxido de grafeno permanecían intactos en los compuestos. Sin embargo, las pruebas magnéticas revelaron que añadir óxido de grafeno reducía de forma consistente la magnetización global de las muestras, porque el carbono no magnético diluye la cantidad de material magnético activo e introduce defectos adicionales en la interfaz.
Cómo las partículas generan realmente calor
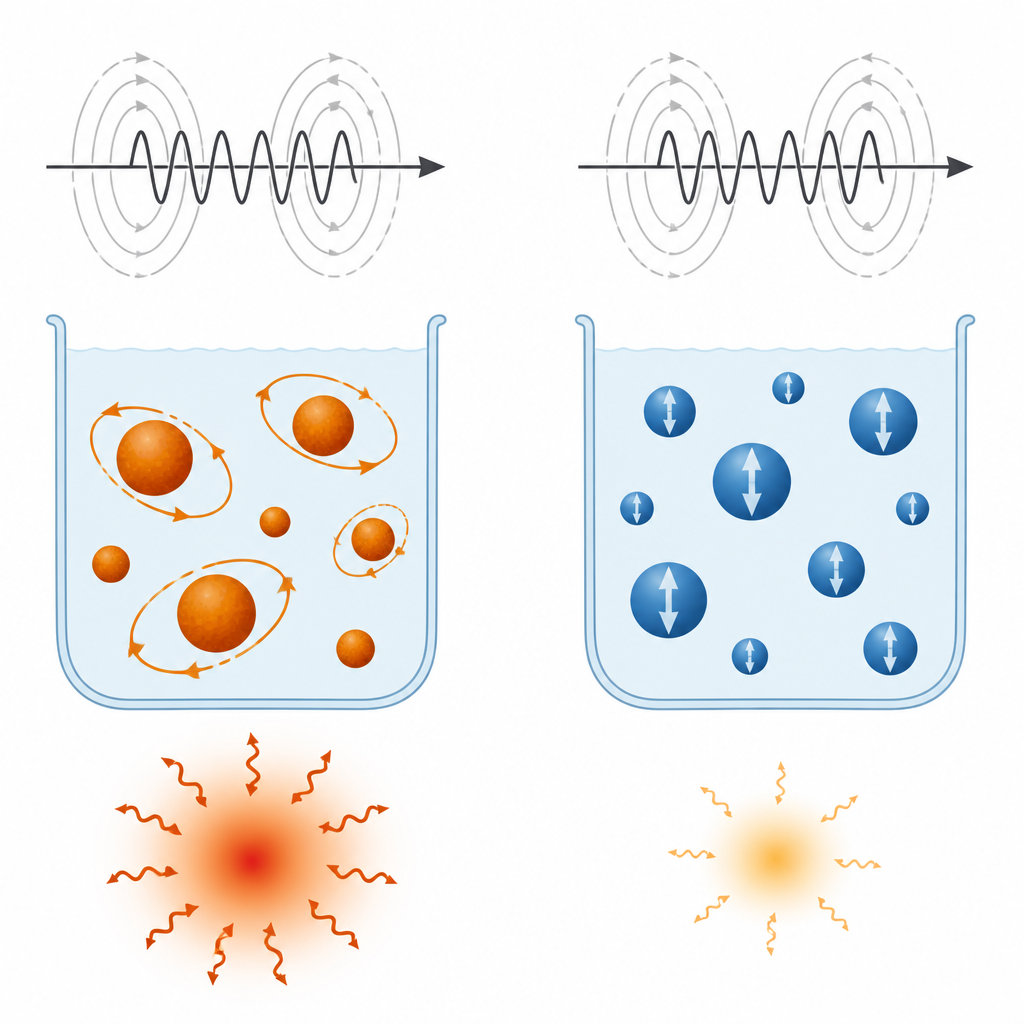
Cuando las suspensiones se sometieron a un campo magnético alterno similar al que podría usarse en tratamiento, todas las muestras se calentaron, pero no por igual. La ferrita de manganeso alcanzó una tasa de absorción específica de aproximadamente 110 vatios por gramo, mientras que la de cobalto alcanzó alrededor de 70 vatios por gramo. La clave está en cómo responden las partículas al campo variable. En MnFe2O4, la magnetización interna de cada partícula puede tanto invertirse internamente como permitir que la partícula completa rote ligeramente en el líquido. Estos dos tipos de movimiento se combinan y ocurren en una escala temporal que coincide con la velocidad del campo aplicado, haciendo el calentamiento eficiente. En CoFe2O4, la magnetización interna está efectivamente congelada por su fuerte bloqueo magnético, de modo que solo la rotación física más lenta en el fluido contribuye, lo que es menos eficaz en las condiciones probadas. Añadir óxido de grafeno redujo la capacidad de calentamiento en ambos casos, más acusadamente en MnFe2O4, porque disminuyó la magnetización y fijó algunas regiones magnéticas impidiendo que respondieran libremente.
Qué significa esto para futuros tratamientos contra el cáncer
Este trabajo muestra que elegir partículas con alta magnetización no es suficiente para lograr un calentamiento intenso para la terapia contra el cáncer. La facilidad con la que la magnetización interna puede moverse, conocida como anisotropía magnética, debe ajustarse para que las partículas respondan en la misma escala temporal que el campo aplicado. En las condiciones aquí probadas, la ferrita de manganeso ofreció el mejor equilibrio, lo que la convierte en la candidata más prometedora. El óxido de grafeno ayuda a mantener las partículas dispersas y ofrece puntos de anclaje para futuras dianas farmacológicas, pero también tiene un coste en la potencia de calentamiento. Los diseños futuros deberán equilibrar estos compromisos, ajustando el tamaño y la forma de las partículas, el recubrimiento superficial y el soporte de carbono para crear nano-calefactores seguros y eficientes que puedan dirigirse con precisión a los tumores.
Cita: Ramadan, W., Gasser, A., Ramadan, A. et al. The impact of graphene oxide on the magnetic and hyperthermia properties of CoFe2O4 and MnFe2O4 ferrites. Sci Rep 16, 14736 (2026). https://doi.org/10.1038/s41598-026-51345-w
Palabras clave: hipertermia magnética, nanopartículas de ferrita, óxido de grafeno, terapia contra el cáncer, nanomedicina