Clear Sky Science · ar
تأثير أكسيد الجرافين على الخصائص المغناطيسية وخصائص التضخيم الحراري لمغناطيسات CoFe2O4 و MnFe2O4
تسخين الأورام بواسطة مغناطيسات صغيرة
يعلم أطباء السرطان منذ زمن أن تسخين الورم بلطف يمكن أن يجعل علاجات أخرى مثل الكيميائيّة والإشعاعية أكثر فعالية. تستكشف هذه الدراسة طريقة جديدة لتوليد هذا الحرارة من داخل الجسم باستخدام جسيمات مغناطيسية نانوية. من خلال مقارنة نوعين من الجسيمات ومزجهما بألواح كربونية فائقة النحافة، يبحث الباحثون عن مواد تسخّن الأورام بكفاءة مع البقاء سهلة التوصيل والتحكم.
لماذا يمكن للحرارة المغناطيسية أن تساعد في علاج السرطان
بدلاً من تسليط الموجات الدقيقة أو الضوء من خارج الجسم، يعتمد التضخيم الحراري المغناطيسي على جسيمات نانوية تسخن عند وضعها في حقل مغناطيسي متغير. إذا حُقنت هذه الجسيمات بالقرب من ورم، يمكن تشغيل الحقل من خارج الجسم فتعمل الجسيمات كمسخّنات دقيقة، رافعةً درجة الحرارة المحلية ببضع درجات فقط فوق المعتاد. التحدّي هو تصميم جسيمات تُنتج حرارة كافية عند شدائد وترددات للحقل آمنة للمرضى، مع البقاء موزعة جيدًا في سوائل الجسم وذات سمية مُنخفضة قدر الإمكان.
مادتان مغناطيسيتان تحت المجهر
ركّز الفريق على مركبين حديديين، فيريت المنغنيز (MnFe2O4) وفيريت الكوبالت (CoFe2O4). كلاهما مغناطيسات صغيرة، لكن سلوكهما مختلف تمامًا. فيريت المنغنيز مغناطيس "ناعم"، بمعنى أن مغناطيسيته الداخلية يمكن أن تنقلب بسهولة نسبية. فيريت الكوبالت مغناطيس "قاسي"، حيث تُثبت مغناطيسيته بقوة في موضعها. صُنعت الجسيمات النانوية في الماء باستخدام طريقة هيدروحرارية وفُحصت بالأشعة السينية والمجاهر الإلكترونية لتأكيد التركيب والشكل والحجم. كانت جسيمات MnFe2O4 في الغالب مكعبة ومكعبية الشكل بحجم حوالي 20 إلى 30 نانومتر، بينما كانت جسيمات CoFe2O4 أصغر وأكثر كروية، حوالى 14 نانومتر.
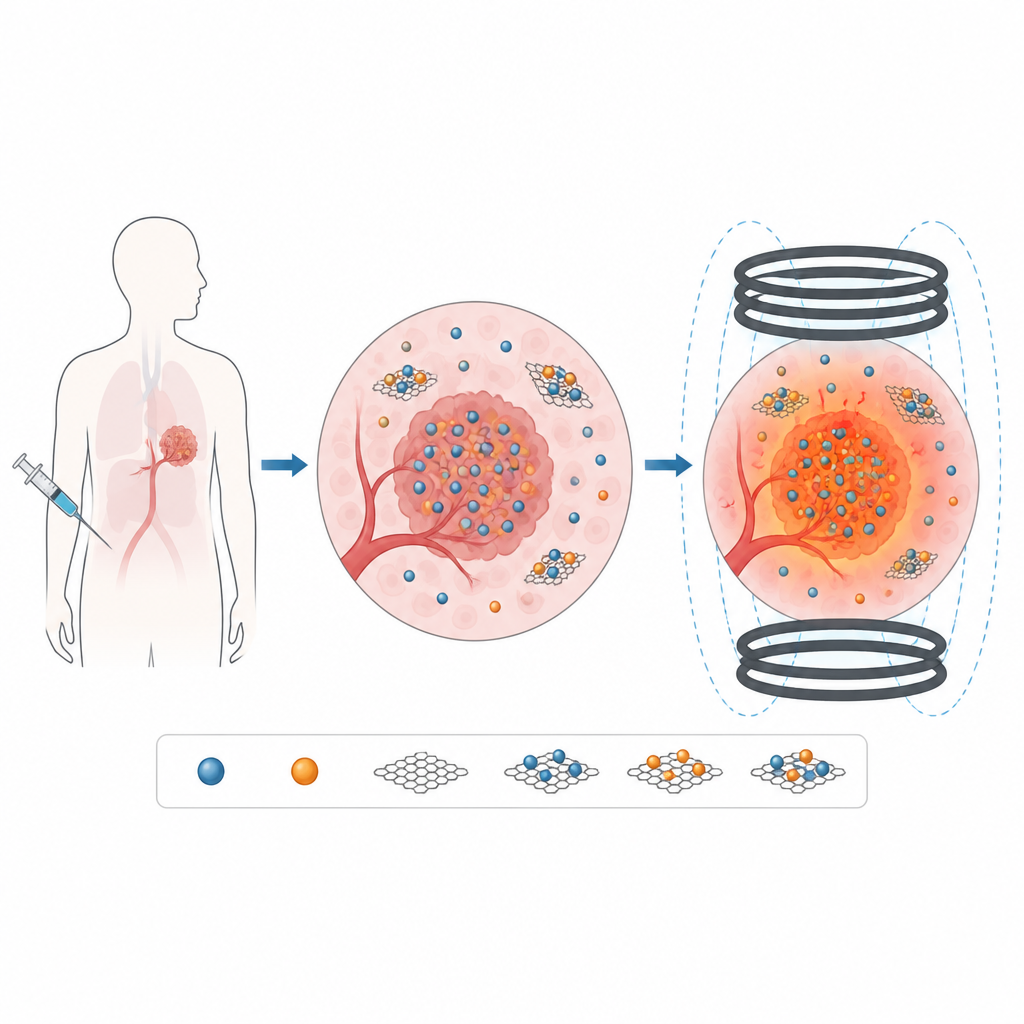
إضافة أكسيد الجرافين: مساعدة وعقبة
لتحسين الاستقرار في السائل وخلق سطح يمكن لاحقًا تزيينه بالعقاقير أو جزيئات الاستهداف، ثبت الباحثون جسيمات الفيريت على صفائح أكسيد الجرافين، وهي مادة كربونية مسطحة غنية بمجموعات أكسجينية. أظهرت الصور انتشار جسيمات MnFe2O4 و CoFe2O4 عبر الصفائح المرنة بدلًا من التكتّل. أكدت التحليلات الطيفية أن الروابط الكيميائية في كل من الفيريت وأكسيد الجرافين بقيت سليمة في المركبات. مع ذلك، كشفت الاختبارات المغناطيسية أن إضافة أكسيد الجرافين قلّلت باستمرار المغناطيسية الكلية للعينات، لأن الكربون غير المغناطيسي قلّل نسبة المادة المغناطيسية الفعالة وأدخل عيوبًا إضافية عند الواجهة.
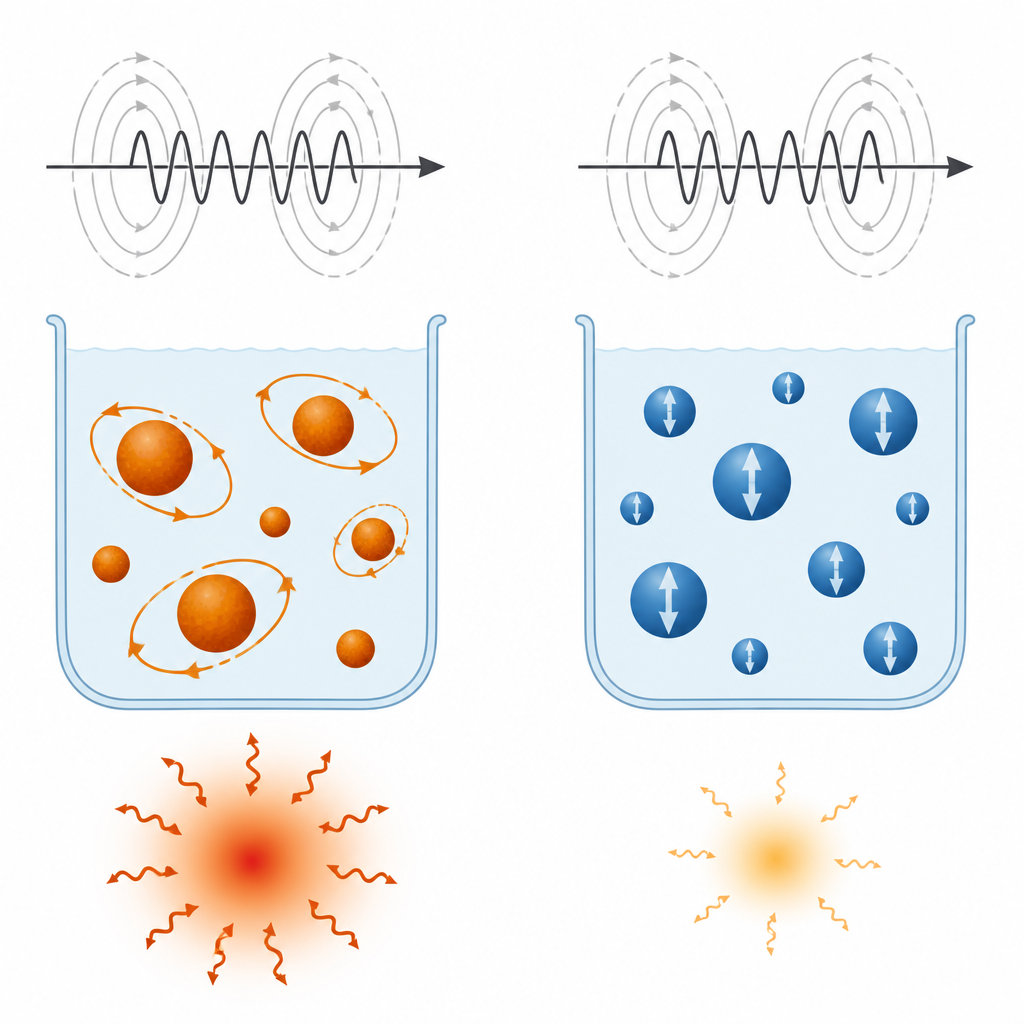
كيف تولد الجسيمات الحرارة فعليًا
عندما وُضعت المعلقات في حقل مغناطيسي متناوب شبيه بما قد يُستخدم في العلاج، سخنت كل العينات، لكن ليس بالمستوى نفسه. بلغ معدل الامتصاص النوعي لفيريت المنغنيز نحو 110 واط لكل غرام، بينما بلغ لفيريت الكوبالت نحو 70 واط لكل غرام. يكمن السبب في كيفية استجابة الجسيمات للحقل المتغير. في MnFe2O4، يمكن لمغناطيسيّة كل جسيم أن تقلب داخليًا وكذلك يسمح للجسيم كله بالدوران قليلًا في السائل. يعمل هذان النوعان من الحركة معًا ويحدثان على مقياس زمني يتطابق مع سرعة الحقل المطبق، مما يجعل التوليد الحراري فعالًا. في CoFe2O4، تكون المغناطيسيّة الداخلية مجمدة عمليًا بسبب القفل المغناطيسي القوي، لذا تساهم فقط الحركة الدورانية الفيزيائية الأبطأ في السائل، وهو أقل فاعلية تحت الظروف المختبرة. أدت إضافة أكسيد الجرافين إلى خفض التسخين في الحالتين، وبشكل أقوى لـ MnFe2O4، لأنها خفّضت المغناطيسية وربطت بعض المناطق المغناطيسية بحيث لا يمكنها الاستجابة بحرية.
ماذا يعني هذا لعلاجات السرطان المستقبلية
تُظهر هذه الدراسة أن اختيار جسيمات ذات مغناطيسية عالية وحدها لا يكفي للحصول على تسخين قوي لعلاج السرطان. يجب ضبط سهولة حركة المغناطيسية الداخلية، المعروفة بالأنزياطروبية المغناطيسية، بحيث تستجيب الجسيمات على نفس الإطار الزمني للحقل المطبق. تحت الظروف المختبرة هنا، قدّم فيريت المنغنيز أفضل توازن، مما يجعله المرشح الأكثر وعدًا. يساعد أكسيد الجرافين في الحفاظ على تشتت الجسيمات ويقدّم نقاط ربط لاستهداف الأدوية مستقبلًا، لكنه يأتي أيضًا بتكلفة في قوة التسخين. سيتعين على التصميمات المستقبلية موازنة هذه المقايضات عن طريق تعديل حجم الجسيمات وشكلها وطلائها السطحي والدعم الكربوني لصنع مسخّنات نانوية آمنة وفعالة يمكن توجيهها بدقة إلى الأورام.
الاستشهاد: Ramadan, W., Gasser, A., Ramadan, A. et al. The impact of graphene oxide on the magnetic and hyperthermia properties of CoFe2O4 and MnFe2O4 ferrites. Sci Rep 16, 14736 (2026). https://doi.org/10.1038/s41598-026-51345-w
الكلمات المفتاحية: التضخيم الحراري المغناطيسي, جسيمات فيريت نانوية, أكسيد الجرافين, علاج السرطان, الطب النانوي