Clear Sky Science · de
Die Auswirkung von Graphenoxid auf die magnetischen und Hyperthermie-Eigenschaften von CoFe2O4- und MnFe2O4-Ferriten
Tumore mit winzigen Magneten erwärmen
Krebsärzte wissen seit langem, dass eine milde Erwärmung eines Tumors andere Behandlungen wie Chemotherapie und Strahlentherapie wirksamer machen kann. Diese Studie untersucht eine neue Methode, diese Wärme von innen im Körper mithilfe winziger magnetischer Partikel zu erzeugen. Durch den Vergleich zweier Partikeltypen und deren Kombination mit ultradünnen Kohlenstofffolien suchen die Forschenden nach Materialien, die Tumore effizient erhitzen und zugleich leicht zu verabreichen und zu steuern sind.
Warum magnetische Erwärmung bei der Krebsbehandlung helfen kann
Statt Mikrowellen oder Licht von außen einzusetzen, beruht die magnetische Hyperthermie auf Nanopartikeln, die sich in einem wechselnden Magnetfeld erwärmen. Werden diese Partikel in Tumornähe injiziert, kann das Feld von außen eingeschaltet werden und die Partikel fungieren als winzige Heizquellen, die die lokale Temperatur nur um wenige Grad über den Normalwert anheben. Die Herausforderung besteht darin, Partikel zu entwerfen, die bei Feldstärken und Frequenzen, die für Patienten sicher sind, genügend Wärme erzeugen, sich gut in Körperflüssigkeiten dispergieren und nur minimale Toxizität aufweisen.
Zwei magnetische Materialien unter dem Mikroskop
Das Team konzentrierte sich auf zwei eisenbasierte Verbindungen: Manganferrit (MnFe2O4) und Kobaltferrit (CoFe2O4). Beide sind winzige Magnete, verhalten sich aber sehr unterschiedlich. Manganferrit ist ein „weicher“ Magnet, dessen interne Magnetisierung sich relativ leicht umkehren kann. Kobaltferrit ist ein „harter“ Magnet, dessen Magnetisierung stark festgelegt ist. Die Nanopartikel wurden in Wasser mittels Hydrothermalverfahren hergestellt und mit Röntgendiffraktion sowie Elektronenmikroskopen untersucht, um Struktur, Form und Größe zu bestätigen. MnFe2O4-Partikel waren überwiegend würfelförmig oder quaderähnlich mit etwa 20 bis 30 Nanometern Kantenlänge, während CoFe2O4-Partikel kleiner und eher sphärisch mit rund 14 Nanometern Durchmesser waren.
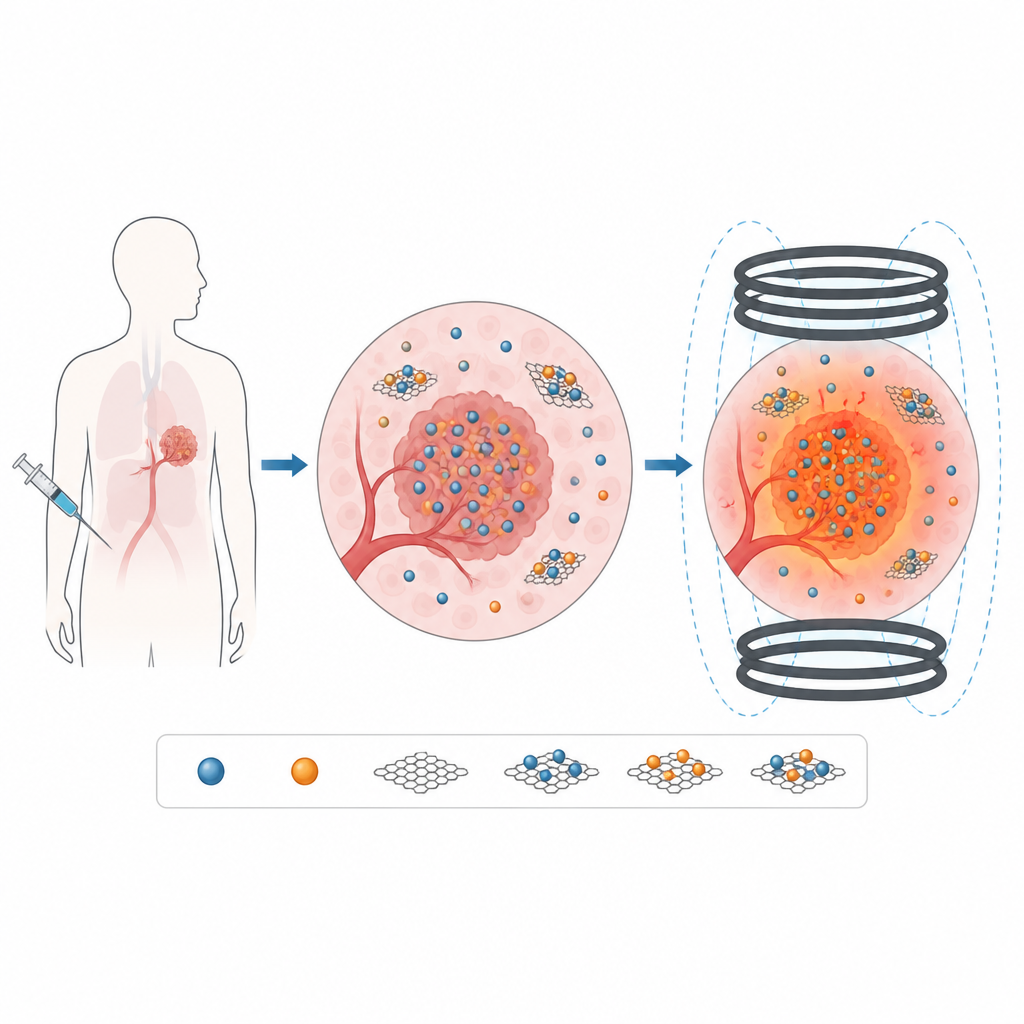
Graphenoxid hinzufügen: Hilfe und Hindernis
Um die Stabilität in Flüssigkeiten zu verbessern und eine Oberfläche zu schaffen, die später mit Wirkstoffen oder Targeting-Molekülen ausgestattet werden kann, verankerten die Forschenden die Ferrit-Nanopartikel auf Blättern aus Graphenoxid, einem flachen Kohlenstoffmaterial mit vielen Sauerstoffgruppen. Die Bildgebung zeigte, dass sich MnFe2O4- und CoFe2O4-Partikel gleichmäßig über die flexiblen Blätter verteilten, anstatt zu verklumpen. Spektroskopie bestätigte, dass die chemischen Bindungen sowohl in den Ferriten als auch im Graphenoxid in den Kompositen erhalten blieben. Magnetische Messungen zeigten jedoch, dass die Zugabe von Graphenoxid die Gesamtmagnetisierung der Proben konstant verringerte, da das nicht-magnetische Kohlenstoffmaterial den Anteil aktiven magnetischen Materials verdünnte und zusätzliche Defekte an der Grenzfläche einführte.
Wie die Partikel tatsächlich Wärme erzeugen
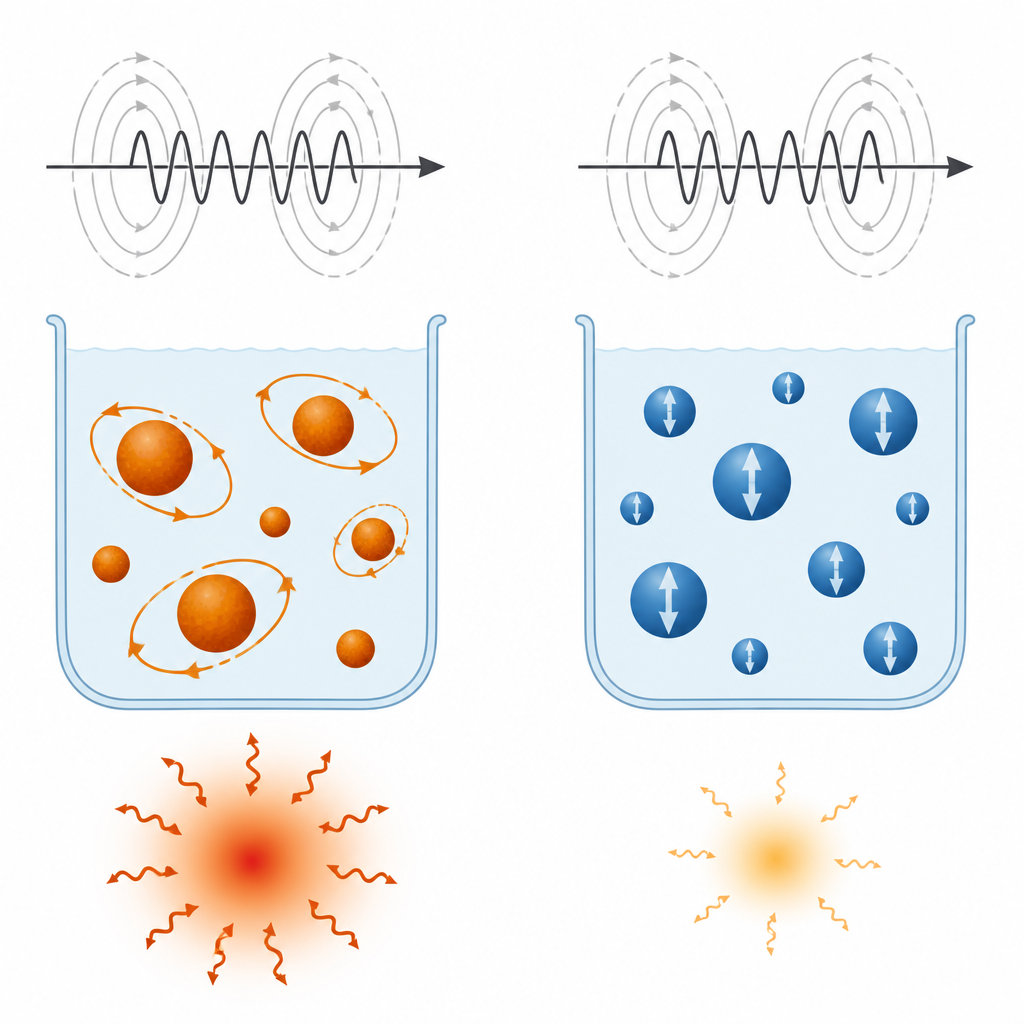
Wurden die Suspensionen einem wechselnden Magnetfeld ausgesetzt, das einem für die Behandlung verwendeten Feld ähnelt, erwärmten sich alle Proben, jedoch nicht gleich stark. Manganferrit erreichte eine spezifische Absorptionsrate von etwa 110 Watt pro Gramm, während Kobaltferrit rund 70 Watt pro Gramm erreichte. Entscheidend ist, wie die Partikel auf das wechselnde Feld reagieren. Bei MnFe2O4 kann sich die Magnetisierung innerhalb jedes Partikels sowohl intern umkehren als auch die ganze Partikelstruktur sich leicht in der Flüssigkeit drehen. Diese beiden Bewegungsarten wirken zusammen und erfolgen in einem Zeitmaßstab, der zur Frequenz des angelegten Feldes passt, wodurch die Erwärmung effizient ist. Bei CoFe2O4 ist die interne Magnetisierung durch die starke magnetische Fixierung praktisch eingefroren, sodass nur die langsamere physikalische Rotation in der Flüssigkeit beiträgt, was unter den getesteten Bedingungen weniger effektiv ist. Die Zugabe von Graphenoxid verringerte die Erwärmung in beiden Fällen, stärker bei MnFe2O4, weil sie die Magnetisierung reduzierte und einige magnetische Bereiche blockierte, sodass sie sich nicht frei anpassen konnten.
Was das für künftige Krebstherapien bedeutet
Diese Arbeit zeigt, dass es nicht genügt, Partikel mit hoher Magnetisierung zu wählen, um starke Erwärmung für die Krebstherapie zu erreichen. Die Leichtigkeit, mit der sich die interne Magnetisierung bewegen kann — bekannt als magnetische Anisotropie — muss so abgestimmt werden, dass die Partikel im gleichen Zeitmaßstab wie das angelegte Feld reagieren. Unter den hier getesteten Bedingungen bot Manganferrit das beste Gleichgewicht und ist damit der vielversprechendere Kandidat. Graphenoxid hilft, Partikel zu dispergieren und bietet Ansätze für künftiges Wirkstoff-Targeting, bringt jedoch auch einen Verlust an Heizleistung mit sich. Zukünftige Designs müssen diese Kompromisse ausbalancieren und Partikelgröße, -form, Oberflächenbeschichtung und die Kohlenstoffunterlage so anpassen, dass sichere, effiziente Nanoheizer entstehen, die präzise zu Tumoren geführt werden können.
Zitation: Ramadan, W., Gasser, A., Ramadan, A. et al. The impact of graphene oxide on the magnetic and hyperthermia properties of CoFe2O4 and MnFe2O4 ferrites. Sci Rep 16, 14736 (2026). https://doi.org/10.1038/s41598-026-51345-w
Schlüsselwörter: magnetische Hyperthermie, Ferrit-Nanopartikel, Graphenoxid, Krebstherapie, Nanomedizin