Clear Sky Science · de
Ramulus Mori (Sangzhi)-Alkaloide dämpfen ernährungsbedingte Adipositas durch Modulation metabolischer Programme im Fettgewebe
Warum diese Forschung für die alltägliche Gesundheit wichtig ist
Adipositas ist mehr als nur zusätzliches Körpergewicht; sie verändert Organe und erhöht das Risiko für Diabetes, Herzkrankheiten und Fettleber. Diese Studie untersucht, ob ein natürlicher Extrakt aus Maulbeerzweigen, der in China bereits zur Behandlung von Typ‑2‑Diabetes verwendet wird, den Körper auch dazu bringen kann, mehr Fett zu verbrennen, indem er das Verhalten verschiedener Fettgewebearten verändert. Wenn dieser Ansatz funktioniert, könnte er den Weg zu sicheren Therapien ebnen, die unsere eigenen Fettzellen dazu bringen, Energie zu vergeuden statt sie zu speichern.
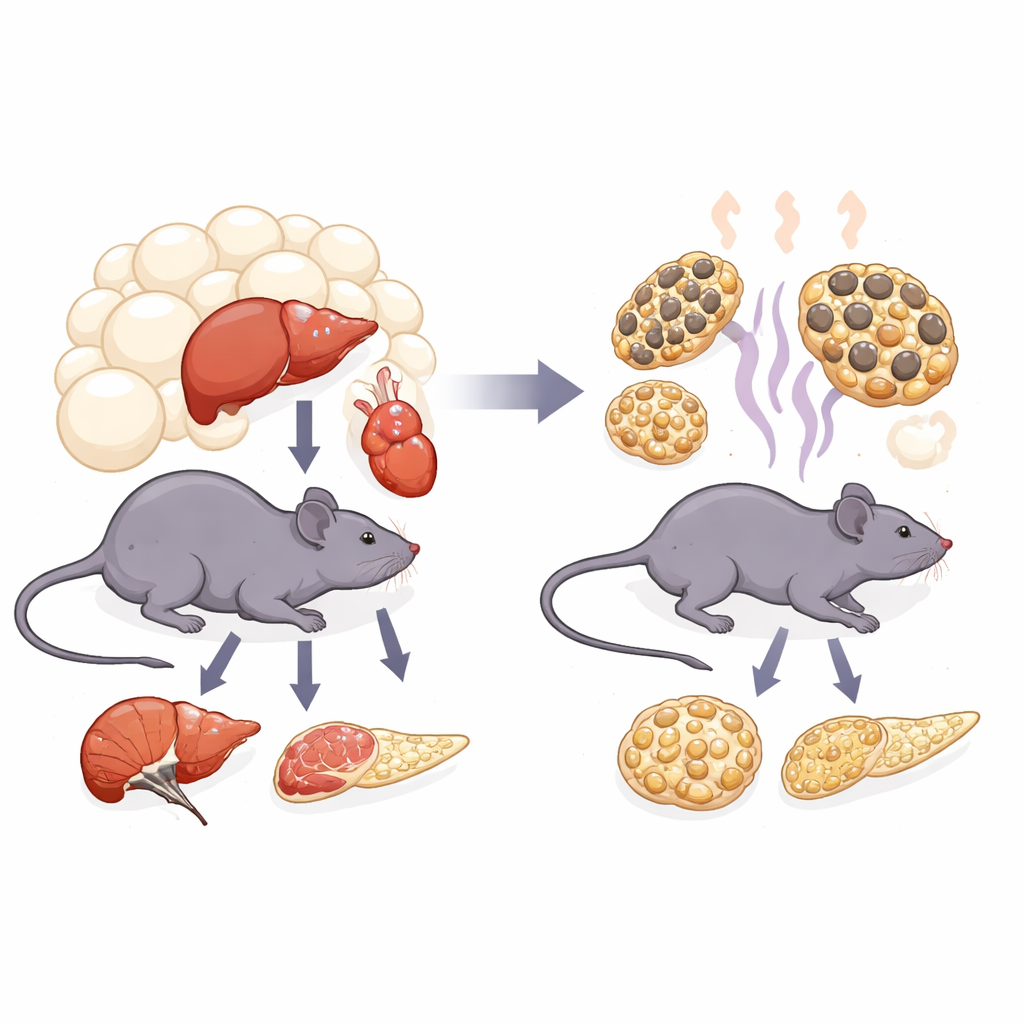
Speicherfett in Brennfett verwandeln
Unser Körper enthält mehrere Arten von Fett. Weißes Fett ist das hauptsächliche Speicherdepot und packt Energie in große, einzelne Tropfen in jeder Zelle. Braunes Fett dagegen ist voller kleiner Tropfen und Energiezentralen, den Mitochondrien, die Energie als Wärme freisetzen. Unter bestimmten Bedingungen kann weißes Fett braunähnliche Eigenschaften annehmen – ein Prozess, der als „Browning“ bezeichnet wird und sogenanntes beige Fett erzeugt. Bei Adipositas versagt dieses System: Braunes Fett wird träger und nimmt weiße Züge an, während weiße Fettzellen anschwellen und nicht mehr richtig funktionieren. Die Forschenden wollten wissen, ob Ramulus Mori (Sangzhi)-Alkaloide (SZ‑A), eine Mischung natürlicher Verbindungen aus Maulbeerzweigen, das Fett wieder in einen aktiveren, kalorienverbrennenden Zustand zurückdrängen können.
Test eines Maulbeerextrakts bei adipösen Mäusen
Das Team fütterte männliche Mäuse 14 Wochen lang mit einer fettreichen Diät, um ernährungsbedingte Adipositas zu modellieren, und behandelte sie anschließend sechs Wochen lang entweder mit einer niedrigen oder einer hohen Dosis SZ‑A. Trotz ähnlicher Nahrungsaufnahme nahmen die behandelten Mäuse deutlich weniger Gewicht zu als unbehandelte fettleibige Tiere. Sie hatten weniger Fett in mehreren wichtigen Depots unter der Haut und um die Organe herum, und in ihren Lebern fanden sich weniger Fetttröpfchen, was auf einen Schutz gegen Fettleber hindeutet. Auf Ebene des gesamten Organismus verbesserte SZ‑A die Blutzuckerkontrolle, machte die Tiere insulinempfindlicher und senkte schädliche Blutfette wie Cholesterin und Triglyzeride – Hinweise auf eine umfassende Verbesserung der metabolischen Gesundheit.
Die körpereigenen Fettverbrennungsmaschinen verjüngen
Bei genauerer Betrachtung des Fettgewebes stellten die Forschenden fest, dass SZ‑A sowohl die Größe als auch das Verhalten der Fettzellen veränderte. Im subkutanen weißen Fett schrumpften vergrößerte Zellen und begannen, beige‑ähnliche Eigenschaften anzunehmen; molekulare Marker für Wärmeerzeugung und gesteigerte mitochondriale Aktivität traten auf. Im viszeralen Fett, das normalerweise schädlicher und weniger flexibel ist, bewirkte SZ‑A keinen dramatischen Übergang zu klassischem braunen Fett. Stattdessen verschob sich die Genaktivität hin zu besserem Fettabbau und effizienterer Verbrennung von Fettsäuren – Veränderungen, die die Belastung der Leber mildern und die Insulinsensitivität verbessern können. Im braunen Fett, das bei adipösen Mäusen „verweißt“ und mit großen Tropfen durchsetzt war, reduzierte SZ‑A die angesammelten Lipidtropfen und stellte Marker für Wärmeerzeugung teilweise wieder her, was auf eine teilweises Wiederherstellung dieses natürlichen kalorienverbrennenden Gewebes hindeutet.
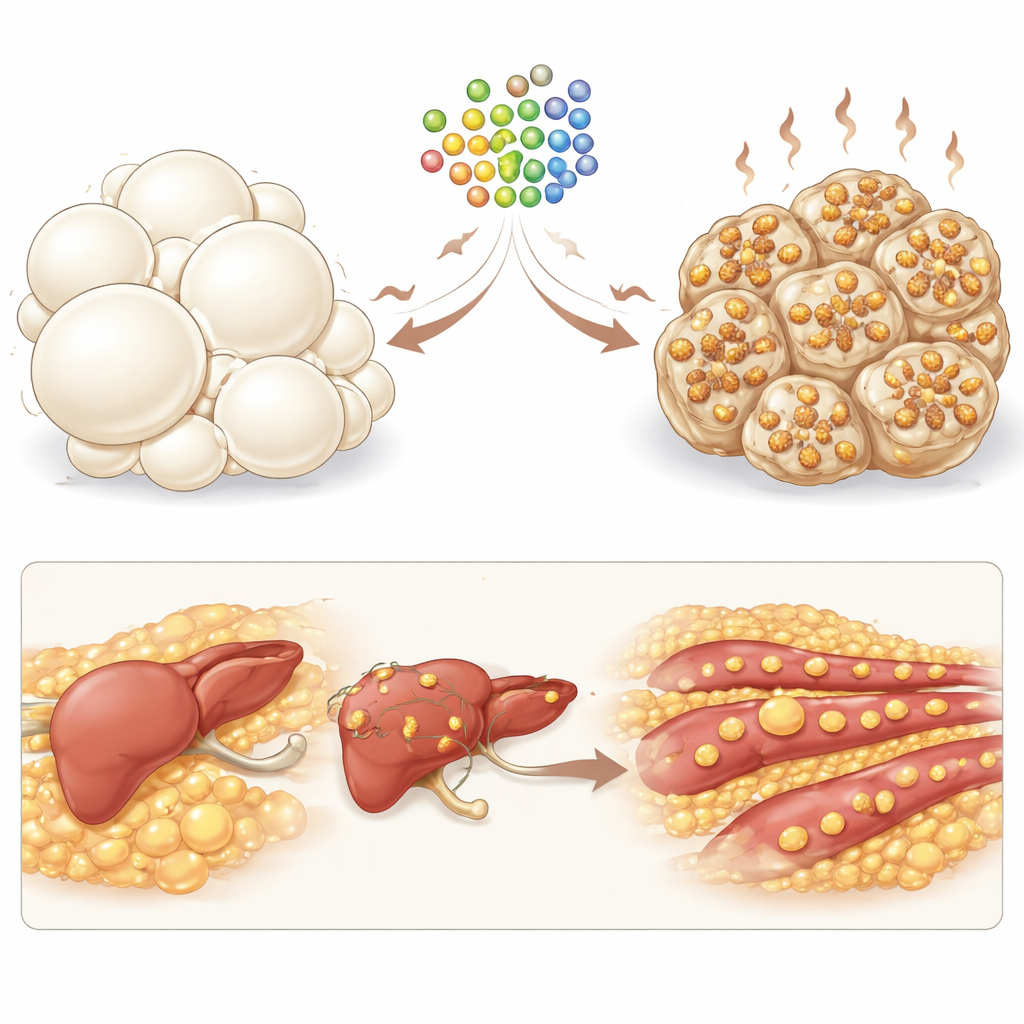
Fettzellen und Genprogramme im Labor untersuchen
Um zu prüfen, ob diese Effekte vom ganzen Organismus abhängen oder direkt in Fettzellen auftreten können, setzten die Forschenden kultivierte Maus-Fettzellen SZ‑A aus. In Dosen, die die Zellen nicht schädigten, regte der Extrakt sie an, viele der gleichen Browning‑ und Thermogenese‑verwandten Gene hochzufahren, die auch in den behandelten Mäusen zu sehen waren – selbst ohne externe Nerven‑ oder Hormonsignale. Parallel dazu zeigte eine breit angelegte Analyse der Genaktivität im viszeralen Fett behandelter Tiere eine großflächige Umprogrammierung metabolischer Wege: Gene, die am Fettsäureabbau, an der Oxidation und an mitochondrialer Funktion beteiligt sind, waren stark angereichert. Dieses Muster stützt die Idee, dass SZ‑A das Fett in einen oxidativeren, energieverbrauchenden Zustand drängt statt in einen reinen Speicherzustand, obwohl die Autor*innen anmerken, dass direkte Messungen von Wärmeausgabe und Energieverbrauch erforderlich sind, um dies zu bestätigen.
Was das für zukünftige Therapien bedeuten könnte
Insgesamt legt die Studie nahe, dass Ramulus Mori (Sangzhi)-Alkaloide ernährungsbedingter Adipositas bei Mäusen entgegenwirken können, indem sie mehrere Fettdepots koordinieren: das subkutane weiße Fett schlanker machen und „umtrainieren“, die Wärmeerzeugung des braunen Fettes wiederbeleben und das tiefe Bauchfett so umrüsten, dass es Fette verbrennt statt sie anzusammeln. Da SZ‑A in China bereits für Menschen mit Typ‑2‑Diabetes zugelassen und als sicher gilt, sticht es unter natürlichen Verbindungen als realistischer Kandidat für weitere Tests hervor. Zwar sind weitere Arbeiten nötig – insbesondere direkte Messungen des Energieverbrauchs und Studien in unterschiedlichen Tiermodellen sowie beim Menschen – doch deuten diese Befunde darauf hin, dass ein sanftes Umprogrammieren des Fettstoffwechsels zu einem kraftvollen, multi‑zieligen Ansatz gegen Adipositas und ihre Begleiterkrankungen werden könnte.
Zitation: Zhang, R., Peng, G., Pan, X. et al. Ramulus Mori (Sangzhi) alkaloids attenuate diet-induced obesity by modulating adipose tissue metabolic programs. Sci Rep 16, 10846 (2026). https://doi.org/10.1038/s41598-026-45462-9
Schlüsselwörter: Adipositas, braunes Fett, Maulbeer-Alkaloide, Fettbraunung, metabolische Gesundheit