Clear Sky Science · de
Computergestützte Identifikation konservierter Epitope des Dengue‑Virus-Hüllproteins für Impfstoffentwicklung und immunodiagnostische Plattform
Warum diese Forschung wichtig ist
Denguefieber ist eine von Mücken übertragene Krankheit, die inzwischen fast die Hälfte der Weltbevölkerung bedroht. Dennoch fehlt Ärzten nach wie vor ein Impfstoff, der sicher gegen alle vier Virusvarianten schützt, ebenso wie verlässliche Bluttests, die eindeutig zeigen, welche Variante eine Infektion verursacht. Diese Studie nutzt fortgeschrittene Computerwerkzeuge, um das Virus im Detail zu durchkämmen und winzige Bausteine zu finden, die die Grundlage für einen sichereren, breiter wirksamen Impfstoff und präzisere diagnostische Tests bilden könnten.
Vier verwandte Viren, ein großes Problem
Das Dengue‑Virus tritt in vier eng verwandten Formen, sogenannten Serotypen, auf, von denen jede Erkrankungen von mildem Fieber bis hin zu lebensbedrohlichen Zuständen verursachen kann. Eine Infektion mit einem Serotyp schützt nur gegen diesen einen und kann das Krankheitsbild verschlimmern, wenn man später mit einem anderen Serotyp infiziert wird. Bestehende Impfstoffe haben deshalb Schwierigkeiten, weil sie gleichzeitig eine starke, ausgewogene Immunität gegen alle vier Serotypen auslösen müssen, ohne das Immunsystem zu einer schädlichen Überreaktion zu verleiten. Hinzu kommt, dass aktuelle Bluttests Dengue mit verwandten Viren wie Zika verwechseln können, was die genaue Nachverfolgung von Ausbrüchen erschwert.
Heranzoom auf die Virusoberfläche
Die Forschenden konzentrierten sich auf das Hüllprotein des Virus, einen Hauptbestandteil der äußeren Schicht, den das Immunsystem als erstes „sieht“. Sie sammelten Tausende von Hüllproteinsequenzen aus allen vier Serotypen und richteten sie aus, um Regionen zu finden, die entweder hochgradig konserviert (ähnlich über alle Typen hinweg) oder klar unterschiedlich von Serotyp zu Serotyp sind. Das Ziel war zweigeteilt: Konservierte Regionen könnten als Rückgrat eines universellen Impfstoffs dienen, während einzigartige Regionen als Fingerabdrücke für Tests fungieren könnten, die zwischen Serotypen unterscheiden.
Mit Computern vielversprechende Ziele finden
Mithilfe einer Suite von Immunoinformatik‑Tools sagte das Team vorher, welche kurzen Abschnitte des Hüllproteins wahrscheinlich von den T‑Zellen und B‑Zellen des Körpers erkannt werden — den weißen Blutkörperchen, die Immunangriffe koordinieren und ausführen. Sie bewerteten jedes Kandidatenfragment danach, wie stark es eine Immunantwort auslösen könnte, ob es Ähnlichkeit zu menschlichen Proteinen aufweist (was Autoimmunität verursachen könnte) und ob es wahrscheinlich toxisch oder allergen ist. Mehrere Fragmente zeichneten sich als sowohl sicher als auch gut für das Immunsystem sichtbar aus, darunter ein Satz, der in allen Serotypen vorkommt und ein „tetravalenter“ Dengue‑Impfstoffkonzept stützen könnte, sowie weitere Sätze, die für die Dengue‑Typen 2, 3 bzw. 4 einzigartig sind und sich ideal für hochspezifische Diagnostiktests eignen.
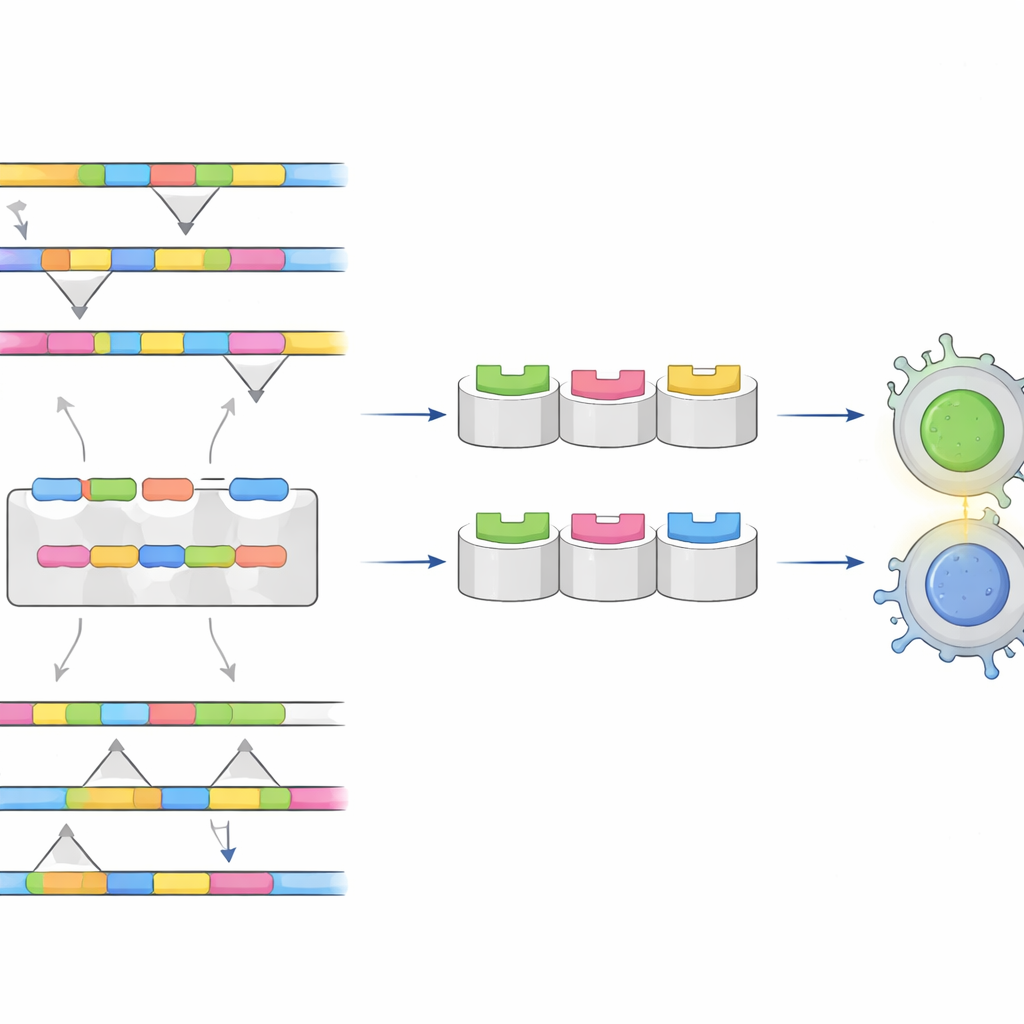
Prüfung der Passform in 3D
Um über Sequenzmuster hinauszugehen, erstellten die Forschenden dreidimensionale Modelle, wie sich diese viralen Fragmente in menschliche Immunmoleküle einfügen würden, die sie T‑Zellen präsentieren. Sie verwendeten Molekulardocking, um die physische Passform zwischen Peptid und Immunrezeptor zu simulieren, und Normalmodenanalyse, um zu untersuchen, wie stabil diese Komplexe beim Bewegen und Nachgeben sind. Einige Peptid‑Rezeptor‑Paare bildeten besonders enge, stabile Bindungen, was darauf hindeutet, dass sie T‑Zellen verlässlich bei vielen Menschen weltweit alarmieren könnten. Eine Populationsanalyse, basierend darauf, wie häufig verschiedene Varianten von Immunrezeptoren in verschiedenen Regionen vorkommen, zeigte, dass das beste Kandidatenset theoretisch etwa zwei Drittel der Weltbevölkerung abdecken könnte, mit besonders starker Abdeckung in Ostasien, Europa und den Amerikas.
Was das für zukünftige Werkzeuge bedeutet
Einfach gesagt liefert diese Arbeit eine sorgfältig gefilterte Kurzliste viraler „Bausteine“, die besonders vielversprechend für die nächste Generation von Dengue‑Impfstoffen und Bluttests erscheinen. Die konservierten Fragmente könnten helfen, einen einzelnen Impfstoff zu entwickeln, der gegen alle vier Dengue‑Typen wirkt, während die einzigartigen Fragmente Ärzten erlauben könnten, genau zu bestimmen, welcher Typ die Erkrankung eines Patienten verursacht. Obwohl diese Vorhersagen noch im Labor und in klinischen Studien bestätigt werden müssen, zeigt die Studie, wie computergestützte Analysen die Suche nach Impfstoff‑ und Diagnostikzielen gegen eine sich rasch ausbreitende Tropenkrankheit deutlich beschleunigen und schärfen können.
Zitation: da Silva, M.K., Fulco, U.L., Alqahtani, T. et al. Computational identification of conserved dengue virus envelope protein epitopes for vaccine design and immunodiagnostic platform. Sci Rep 16, 14167 (2026). https://doi.org/10.1038/s41598-026-37744-z
Schlüsselwörter: Dengue-Impfstoff, Epitop-Kartierung, Hüllprotein, Immunoinformatik, serotyp-spezifische Diagnostik