Clear Sky Science · de
Herz-Kreislauf-Alterung: Kennzeichen, Signalwege, Erkrankungen und therapeutische Angriffspunkte
Warum unser Herz altert, bevor wir uns alt fühlen
Viele Menschen verbinden Altern mit grauen Haaren und langsameren Schritten, doch tief im Körper vollzieht sich eine leisere Form des Alterns. Unsere Herzen und Blutgefäße versteifen und verlieren nach und nach ihre Elastizität, und dieser verborgene Prozess ist der wichtigste Treiber für Herzinfarkte, Schlaganfälle und Herzinsuffizienz weltweit. Dieser Übersichtsartikel fasst Jahrzehnte der Forschung zusammen, um zu erklären, warum das kardiovaskuläre System altert, wie dieses Altern zahlreiche schwere Erkrankungen auslöst und was die Wissenschaft bereits dagegen unternimmt — von Lebensstiländerungen bis hin zu experimentellen „Verjüngungs“-Therapien.
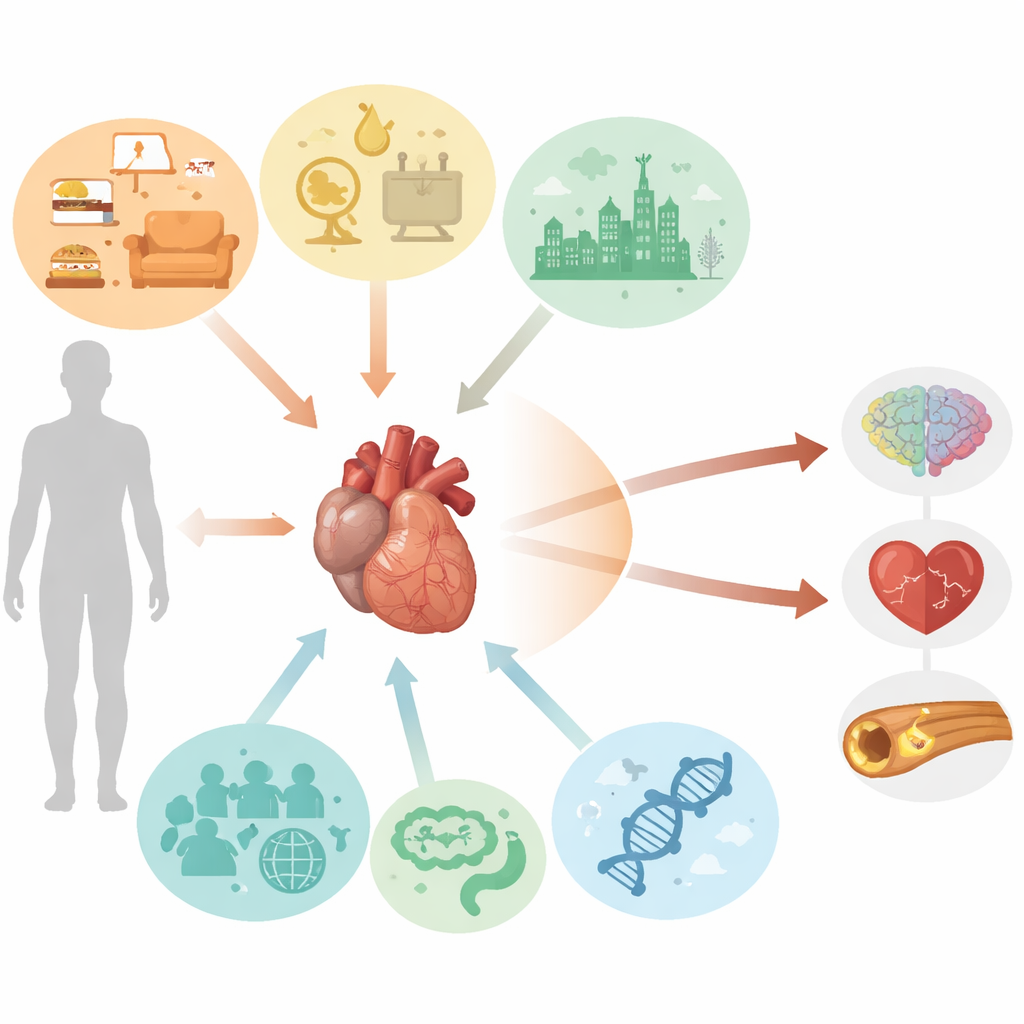
Alltägliche Einflüsse, die das Herz altern lassen
Die Autoren beschreiben kardiovaskuläres Altern nicht nur als bloßen Zeitverlauf. Fünf große Einflussbereiche wirken zusammen, um den Prozess zu beschleunigen oder zu verlangsamen: Lebensgewohnheiten, Stoffwechsel- und Hormonbalance, Umweltbelastungen, genetische und epigenetische Ausstattung sowie Merkmale unserer biologischen und sozialen Umwelt. Rauchen, Bewegungsmangel, zu viele Kalorien und chronischer Stress beschleunigen die Schädigung von Blutgefäßen. Adipositas, Bluthochdruck, Diabetes, Nierenerkrankungen und das metabolische Syndrom schaffen ein biochemisches Milieu, das die Gefäßwände angreift. Luftverschmutzung, Schwermetalle, Strahlung, bestimmte Chemotherapien und sogar Raumflug können das kardiovaskuläre System in Richtung vorzeitigen Verschleiß treiben. Zugleich beeinflussen vererbte Genvarianten, altersbedingte Verschiebungen in der Genregulation, Darmmikroben, chronische Virusinfektionen, Sexualhormone sowie ethnische und soziale Ungleichheiten, wer schneller altert und auf welche Weise.
Wie ein alterndes Herz und Gefäße im Inneren aussehen
Mit zunehmendem Alter erfahren Herz und Blutgefäße markante strukturelle und funktionelle Veränderungen. Der Herzmuskel lagert narbenähnliche Fibrose und abnorme Proteine ein, die Herzkammern vergrößern sich oder verdicken, und die Fähigkeit zu entspannen und effizient zu pumpen nimmt ab. Kleine Koronargefäße verlieren Elastizität und Dichte, wodurch die Durchblutung bei gesteigertem Bedarf eingeschränkt wird. In den Arterien werden die einst geschmeidigen Wände dicker, steifer und stärker verkalkt. Die Zellen der Innenauskleidung, die normalerweise gefäßerweiternde Signale freisetzen, werden seltener und dysfunktionaler, während Muskelzellen in der Gefäßwand ihre Identität verändern und sich weg von Kontraktion hin zu Wachstums- und Narbenbildungsprozessen entwickeln. Diese Veränderungen untergraben die Fähigkeit des kardiovaskulären Systems, sich an Stress anzupassen, und bereiten so den Boden für typische Spätprobleme wie Vorhofflimmern, Herzinsuffizienz mit erhaltener Ejektionsfraktion und schwer behandelbaren Bluthochdruck.
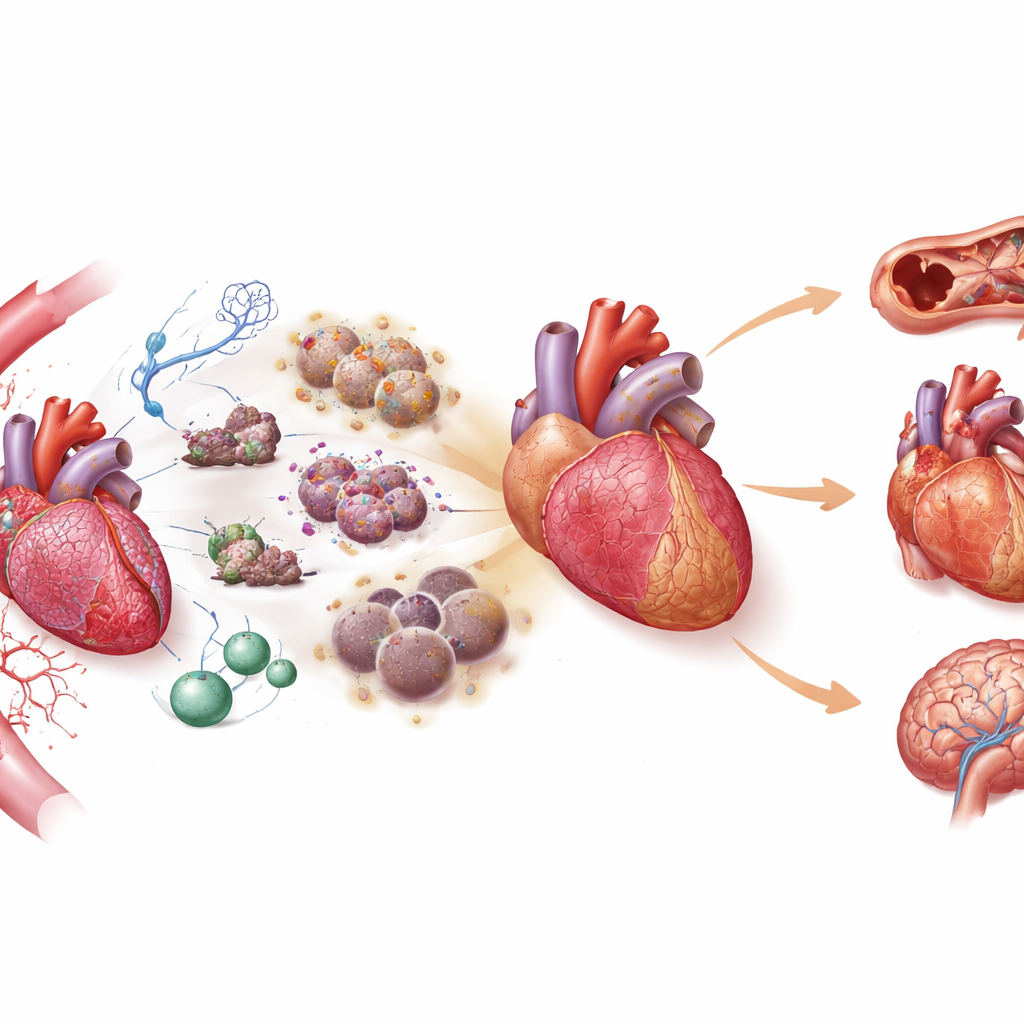
Die inneren Kennzeichen des kardiovaskulären Alterns
Um die Komplexität zu ordnen, gliedert das Papier zwölf „Kennzeichen“ des kardiovaskulären Alterns in drei Ebenen: molekular, zellulär und systemisch. Auf molekularer Ebene schwächen DNA-Schäden, epigenetische Drift, Versagen der Proteinqualitätskontrolle, geschwächte Mitochondrien und chronische niedriggradige Entzündung nach und nach die Zellgesundheit. Auf zellulärer Ebene verlieren zentrale Akteure wie Herzmuskelzellen, gefäßauskleidende Zellen, Immunzellen und Stammzellen ihre Fähigkeit zur Reparatur, zum Recycling und zur Erneuerung; viele treten in einen Zustand namens Seneszenz ein, in dem sie sich nicht mehr teilen, aber entzündungs- und gewebeumgestaltende Substanzen freisetzen. Auf systemischer Ebene werden wichtige Signalwege, die dem Körper normalerweise helfen, auf Stress zu reagieren — etwa das Hormonnetzwerk zur Regulierung von Blutdruck und Salzhaushalt, die „Kampf-oder-Flucht“-Stressantwort, Wachstumsfaktorwege und die Mechanosensibilität der Zellen — chronisch überaktiviert oder falsch abgestimmt. Diese Kennzeichen interagieren ständig, sodass eine Störung in einem Bereich, etwa mitochondriale Schäden, nach außen wirken und Entzündung, Seneszenz und Gewebeversteifung verstärken kann.
Wie ein altes Herz viele verschiedene Krankheiten antreibt
Kardiovaskuläres Altern beschränkt sich nicht auf den Brustkorb. Es bildet einen gemeinsamen Nährboden für Atherosklerose, Aneurysmen und Herzinsuffizienz und trägt auch zu Erkrankungen fernab des Herzens bei. Seneszente und dysfunktionale Gefäßzellen begünstigen fettige Plaques, schwächen die Aortenwand und machen Plaques fragiler. Verlust der Proteinqualitätskontrolle und mitochondriale Dysfunktion im Herzmuskel fördern Herzinsuffizienz. Im Gehirn tragen steife Arterien, undichte Gefäßbarrieren und verlangsamte Flüssigkeitsräumung zu kognitivem Abbau und neurodegenerativen Erkrankungen wie Alzheimer und Parkinson bei. Bei Diabetes verschlechtern gealterte Endothelzellen mikrovaskuläre Komplikationen, während hoher Blutzucker wiederum die Gefäßalterung beschleunigt und einen Teufelskreis schafft. Ähnliche Rückkopplungsschleifen verbinden wahrscheinlich Adipositas und gestörte Blutfettwerte mit fortschreitenden Schäden an Gefäßen und Organen.
Können wir die kardiovaskuläre Uhr zurückdrehen?
Der Übersichtsartikel hebt einen wachsenden Werkzeugkasten potenzieller „Verjüngungs“-Strategien hervor. Einige sind vertraut: Mit dem Rauchen aufzuhören, die Ernährungsqualität zu verbessern, ein gesundes Gewicht zu halten und regelmäßige körperliche Aktivität verlangsamen die Gefäßversteifung und verbessern die Herzfunktion in jedem Alter. Andere Ansätze sind experimenteller. Wirkstoffe, die seneszente Zellen eliminieren oder umprogrammieren, Substanzen, die Energiesensorwege wie mTOR, AMPK und Sirtuine modulieren, sowie gezielte antiinflammatorische Therapien werden in Tiermodellen und frühen klinischen Studien geprüft. Forschende untersuchen auch Nerven‑Herz-Verbindungen und zeigen, dass Schlaf, Stress und psychische Gesundheit die Gefäßalterung direkt beeinflussen, ebenso wie Stammzell‑ und extrazelluläre‑Vesikel-Ansätze zur Reparatur geschädigter Gefäße. Zugleich zielen neue „Alterungsuhren“ auf DNA‑Marken oder Blutproteine ab, um zu messen, wie alt das kardiovaskuläre System eines Menschen tatsächlich ist, und um nachzuverfolgen, ob Interventionen dessen Abbau wirklich verlangsamen oder umkehren.
Was das für gesundes Altern bedeutet
Die zentrale Botschaft für Laien lautet, dass kardiovaskuläres Altern kein einfacher, automatischer Countdown ist, der nur an Geburtstagen abgelesen werden kann. Es ist ein dynamischer Prozess, angetrieben von wechselwirkenden molekularen Schäden, zellulärem Verschleiß und systemweiter Fehlkommunikation — dennoch sind viele seiner Hebel beeinflussbar. Durch das Verständnis der Kennzeichen und Auslöser des kardiovaskulären Alterns beginnen Wissenschaftler, Therapien zu entwickeln, die das Fortschreiten verzögern, abschwächen oder teilweise umkehren könnten und so Herzinfarkte, Schlaganfälle, Herzinsuffizienz und sogar manche Formen der Demenz verhindern. Auch wenn noch viel Arbeit vor uns liegt, argumentiert die Übersicht, dass der Schutz des „Alters“ unserer Arterien und unseres Herzens eine der wirkungsvollsten Strategien sein könnte, nicht nur die Lebensspanne, sondern vor allem die Jahre gesunden, selbstständigen Lebens zu verlängern.
Zitation: Zheng, P., Yan, W., Ding, Y. et al. Cardiovascular ageing: hallmarks, signaling pathways, diseases and therapeutic targets. Sig Transduct Target Ther 11, 142 (2026). https://doi.org/10.1038/s41392-026-02630-7
Schlüsselwörter: kardiovaskuläres Altern, Gefäßgesundheit, zelluläre Seneszenz, Herzinsuffizienz, Atherosklerose