Clear Sky Science · de
Künstliche Intelligenz unterscheidet prä-fibrotische primäre Myelofibrose mit Thrombozytose von essentieller Thrombozythämie anhand digitalisierter Knochenmarkbiopsiebilder
Warum das für Menschen mit Blutkrankheiten wichtig ist
Ärztinnen und Ärzte haben oft Schwierigkeiten, zwei sich sehr ähnlich sehende Blutkrankheiten zu unterscheiden, die langfristig aber ganz unterschiedliche Risiken bergen. Diese Studie zeigt, wie künstliche Intelligenz Knochenmarkbilder am Bildschirm lesen kann, um diese Erkrankungen genauer zu trennen, und weist sogar auf subtile Gewebemerkmale hin, die Menschen möglicherweise übersehen. Für Patientinnen und Patienten könnte das schließlich bedeuten: bessere Diagnosen, klarere Risikoinformationen und individuellere Therapieansätze.
Zwei ähnliche Erkrankungen mit sehr unterschiedlicher Prognose
Essentielle Thrombozythämie und prä-fibrotische primäre Myelofibrose sind beides seltene Knochenmarkerkrankungen, die zu zu vielen Thrombozyten — den blutgerinnungsunterstützenden Zellen — führen. Unter dem Mikroskop können ihre Knochenmarkproben sehr ähnlich aussehen, sodass selbst erfahrene Pathologinnen und Pathologen manchmal uneinig sind, welche Diagnose zu stellen ist. Die Unterscheidung ist wichtig, weil Menschen mit der prä-fibrotischen Form eher schwere Vernarbungen des Markes, Leukämie und lebensbedrohliche Komplikationen entwickeln als solche mit essentieller Thrombozythämie. Aktuelle Leitlinien stützen sich auf das visuelle Urteil von Expertinnen und Experten zu Zellformen und feinen Narbenbildungen — ein Vorgehen, das sowohl subjektiv als auch zeitaufwendig ist.
Ein Computer lernt, Knochenmarkpräparate zu lesen
Die Forschenden entwickelten ein zweiteiliges KI-System, das direkt mit routinemäßig gefärbten Knochenmarkbiopsiebildern arbeitet. Zunächst nutzten sie ein leistungsfähiges vortrainiertes Modell, das ursprünglich mit Zehntausenden Krebspräparaten konfrontiert worden war, um detaillierte visuelle Muster aus jeder kleinen Region der Biopsie zu extrahieren. Danach wendeten sie eine „Attention“-Methode an, die es dem Algorithmus erlaubt, Regionen höher zu gewichten, die eine Diagnose stärker stützen. Trainiert an 200 italienischen Patientinnen und Patienten mit sorgfältig bestätigten Diagnosen und anschließend getestet an einer unabhängigen Kohorte eines US-amerikanischen Krebszentrums, unterschied das System die beiden Erkrankungen mit hoher Genauigkeit. In der Validierungsgruppe trennte es die prä-fibrotische primäre Myelofibrose korrekt von der essentiellen Thrombozythämie bei mehr als neun von zehn Patientinnen und Patienten und zeigte dabei eine besonders starke Fähigkeit, fälschlicherweise die riskantere Erkrankung zuzuordnen zu vermeiden. 
Mit synthetischen Bildern sehen, was die KI wahrnimmt
Um zu verstehen, auf welche visuellen Hinweise das Modell setzte, ergänzte das Team das System um eine generative Komponente, die realistisch wirkende Knochenmark-Patches erzeugen kann, wie sie typisch für jede Erkrankung sind. Sie wählten sowohl reale als auch computererzeugte Bildkacheln aus, die der Klassifikator mit hoher Sicherheit einordnete, und baten drei expertische Hämatopathologinnen und -pathologen, diese blind zu beurteilen. Bei realen Bildern stimmten die menschlichen Expertinnen und Experten meist mit der KI-Diagnose überein, wenn sie sich zu einer Entscheidung durchringen konnten. Bei vielen synthetischen Bildern — besonders solchen, die die essentielle Thrombozythämie nachahmten — widersprachen Pathologinnen und Pathologen jedoch häufig dem Algorithmus oder fühlten sich unsicher, eine sichere Diagnose zu treffen, obwohl die KI diese Kacheln entsprechend den bekannten Patientendaten korrekt klassifizierte.
Eine überraschende Rolle von Fett versus Zellen im Mark
Der Kontrast zwischen Mensch und Maschine veranlasste eine genauere Untersuchung der Gewebezusammensetzung in realen und generierten Bildern. Mit einem weiteren Bildanalysetool bestimmten die Forschenden, wieviel jeder Kachel von Fettarealen gegenüber blutbildenden Zellen eingenommen wurde. Über alle Proben hinweg enthielten mit essentieller Thrombozythämie assoziierte Bilder mehr Fett, während jene mit prä-fibrotischer primärer Myelofibrose dichter mit Zellen gefüllt waren. Dieses Muster zeigte sich sowohl in realen Patientenbildern als auch in den computergenerierten Bildern und war in den synthetischen essentiellen-Thrombozythämie-Slides sogar noch ausgeprägter. Heatmaps der Modell-"Attention" zeigten außerdem, dass der Algorithmus natürlicherweise aktive blutbildende Bereiche statt Knochen oder Artefakte fokussierte, was darauf hindeutet, dass er biologisch sinnvolle Hinweise gelernt hat und nicht nur Abkürzungen nutzt. 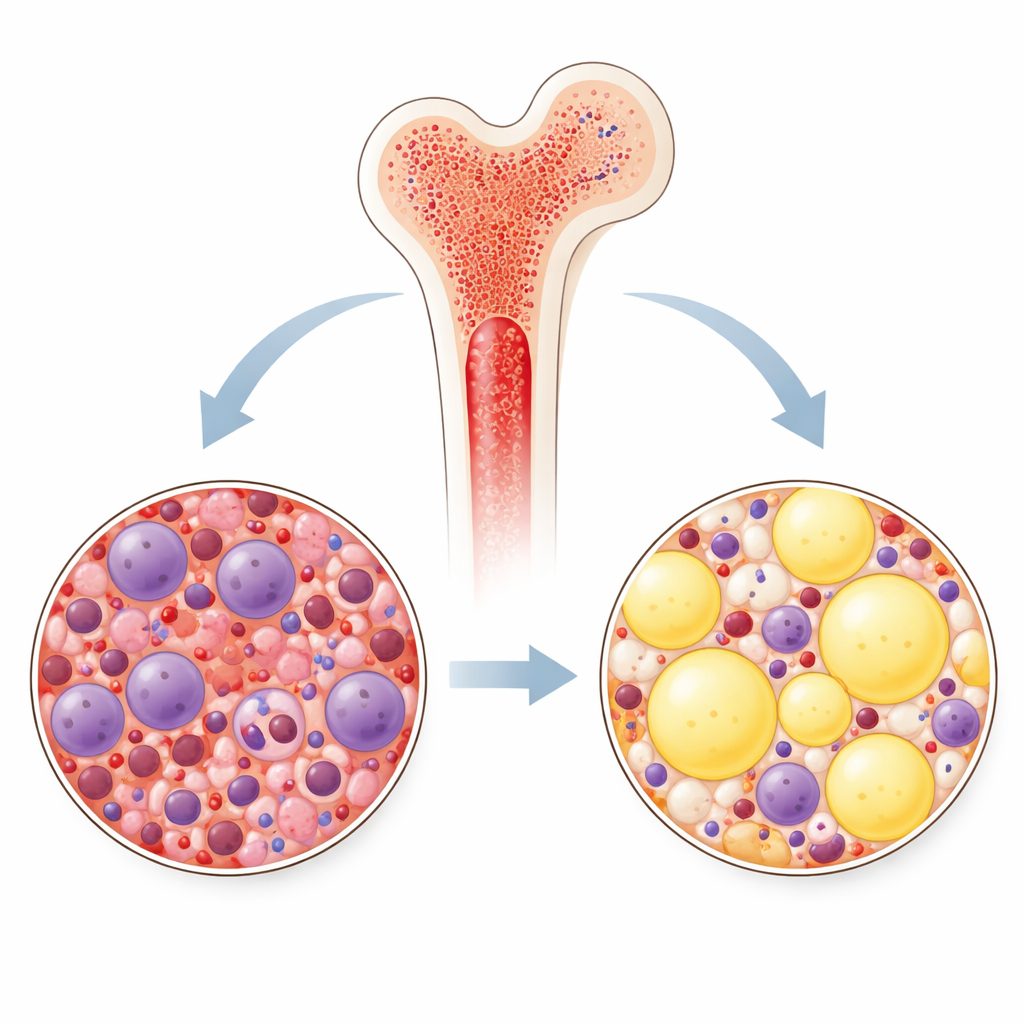
Was das für Diagnose und Behandlung bedeuten könnte
Praktisch betrachtet legt die Studie nahe, dass ein sorgfältig trainiertes KI-System Pathologinnen und Pathologen dabei unterstützen kann, diese zwei ähnlich erscheinenden Markskrankheiten anhand standardisierter Präparate zu unterscheiden, und dass es nützliche Gewebemerkmale wie das Verhältnis von Fett zu Zellen aufdecken kann, die derzeit nicht Teil der Checklisten sind. Die Autorinnen und Autoren betonen, dass ihr Tool nicht dazu bestimmt ist, die Expertise von Fachleuten zu ersetzen — insbesondere angesichts der bisher vergleichsweise geringen Patientenzahl. Stattdessen könnte es als zweites Beurteilungsinstrument dienen, vor allem in Zentren mit wenigen Fällen, und dazu beitragen, welche Patientinnen und Patienten in klinische Studien aufgenommen werden, indem solche mit der aggressiveren prä-fibrotischen Erkrankung ausgeschlossen werden. Langfristig könnte die Kombination dieser bildbasierten KI mit klinischen und genetischen Daten zu sichereren, personalisierteren Behandlungsentscheidungen für Menschen mit diesen seltenen Blutkrankheiten beitragen.
Zitation: Srisuwananukorn, A., Loscocco, G.G., Dolezal, J.M. et al. Artificial intelligence differentiates prefibrotic primary myelofibrosis with thrombocytosis from essential thrombocythemia using digitized bone marrow biopsy images. Leukemia 40, 1018–1026 (2026). https://doi.org/10.1038/s41375-026-02893-7
Schlüsselwörter: künstliche Intelligenz, Knochenmarkbiopsie, myeloproliferative Neoplasien, essentielle Thrombozythämie, prä-fibrotische Myelofibrose