Clear Sky Science · ar
ZFP148 هو كابح نسخي لتمايز الخلايا التائية CD8 القاتلة الخلوية
مساعدة القتلة داخل الجسم على أداء وظيفتهم
يعتمد جهازنا المناعي على خلايا T المتخصصة «القاتلة» لمطاردة الخلايا المصابة بالفيروسات والخلايا السرطانية. ومع ذلك، في المعارك الطويلة ضد العدوى المزمنة أو الأورام، غالبًا ما تتعب هذه الخلايا وتفقد فعاليتها. تكشف هذه الدراسة عن فرملة جزيئية، بروتين يُدعى ZFP148، يضعف قدرة هذه الخلايا على القتل. عبر رفع هذه الفرملة في الفئران وفحص الأورام البشرية، يُظهر الباحثون طريقة لتعزيز قدرة الجهاز المناعي الطبيعية على السيطرة على المرض وتحسين الاستجابة للعلاجات المناعية الحديثة للسرطان.
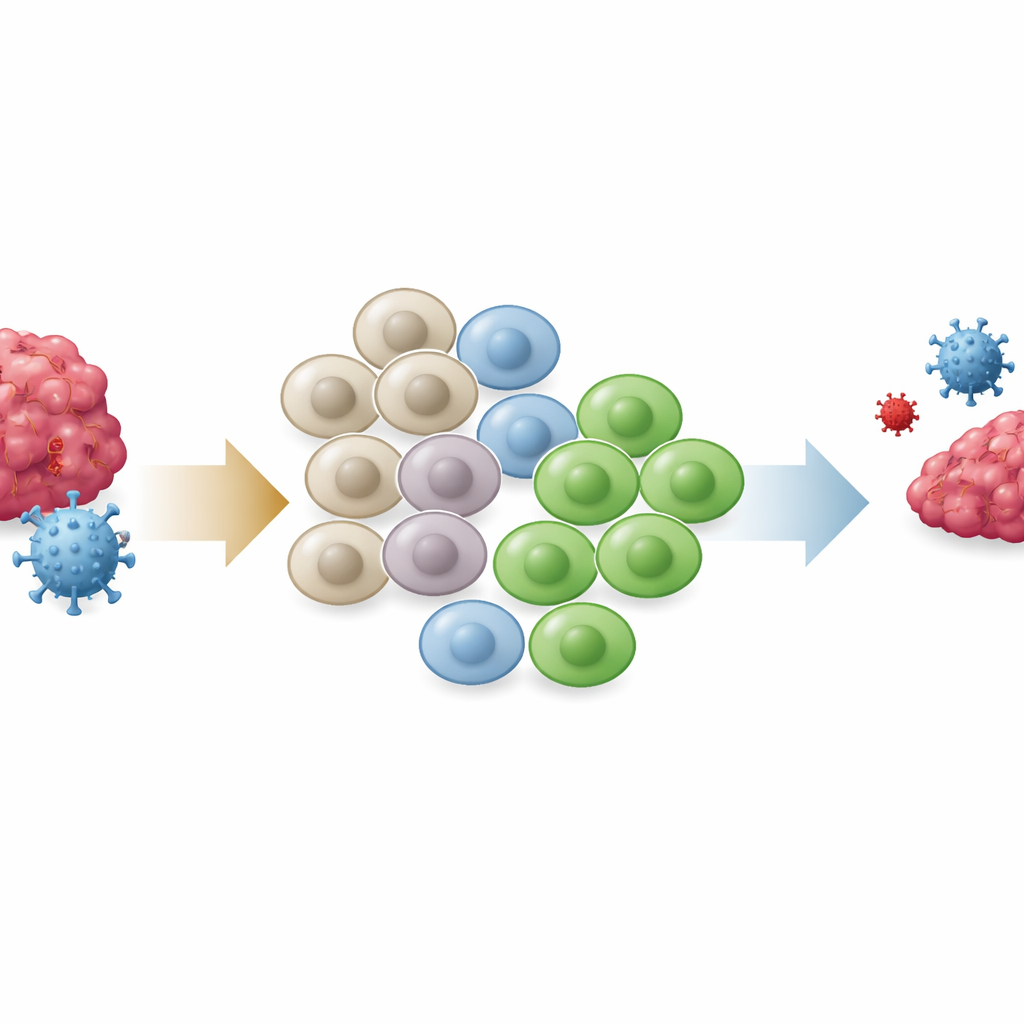
عندما ينهكه القتلة
في حالات العدوى المزمنة والسرطان، تواجه خلايا CD8 القاتلة تعرضًا مستمرًا لأهدافها. بمرور الوقت، يدخل كثير منها حالة تُعرف بالإرهاق، حيث تعبر عن جزيئات مثبطة وتفقد تدريجيًا قدرتها على الانقسام والقتل. مجموعة أصغر من الخلايا «السلفية» لا تزال قادرة على تجديد نفسها وإما أن تولد خلايا مرهقة أو خلايا قاتلة فعّالة عالية التدمير تتفوق في تدمير الخلايا المصابة أو الخبيثة. فهم ما يوجه هذا الانقسام—نحو مؤثرات قوية أم نحو الإرهاق—هو سؤال محوري لتحسين اللقاحات والعلاج المناعي.
فرملة جزيئية جديدة تظهر في الأفق
ركز الفريق على ZFP148، بروتين رابط للحمض النووي دُرس سابقًا في أنواع خلوية أخرى لكنه لم يُفهم جيدًا في خلايا T القاتلة. وجدوا أن ZFP148 أكثر وفرة في خلايا CD8 السلفية وينخفض مع تحول الخلايا إلى مؤثرات قصيرة العمر أو إلى حالة الإرهاق. باستخدام نموذج فئران للعدوى الفيروسية المزمنة، أزالوا ZFP148 بشكل انتقائي من خلايا CD8 فقط. من دون هذا الجزيء، أنتجت الحيوانات تجمعًا أكبر من الخلايا القاتلة الخلوية—المليئة بالإنزيمات المدمرة للخلايا—وتجمعًا أصغر من الخلايا المرهقة. كما تجولت هذه الخلايا المؤثرة في الجسم بشكل أوسع وأظهرت قدرة أعلى على قتل خلايا الورم في الاختبارات المخبرية.
إعادة توصيل لوحة التحكم الجينية
لرؤية كيف يعيد ZFP148 تشكيل سلوك الخلايا التائية، جمع الباحثون بين تسلسل RNA أحادي الخلية (أي الجينات النشطة) مع تحليل الكروماتين أحادي الخلية (أي مناطق الحمض النووي المفتوحة). في الفئران الطبيعية، ساعد ZFP148 في إبقاء المناطق التي تشغّل برامج المؤثرات مغلقة نسبيًا، بينما فضل أنماطًا مرتبطة بالحالات الشبيهة بالجذور أو بالإرهاق. في غياب ZFP148، أصبحت مناطق الحمض النووي التي تتحكم في جزيئات المؤثرات والسمات الشبيهة بالخلايا القاتلة الطبيعية أكثر وصولًا، وتحولت نشاطات الجينات نحو هوية شديدة السمية الخلوية. برز هدف محوري: بروتين آخر، KLF2، الذي يدعم توليد وحركة خلايا المؤثرات. ارتبط ZFP148 فعليًا بمقطع تنظيمي قرب جين Klf2 وكبح نشاطه. إزالة إما KLF2 أو ذاك العنصر DNA المحدد ألغت فوائد تعزيز المؤثرات الناجمة عن فقدان ZFP148، مما يظهر أن محور ZFP148–KLF2 يعمل كمفتاح مركزي لمصير الخلية التائية.
تعزيز العلاج المناعي
انتقل الباحثون بعد ذلك إلى نماذج سرطانية. في الفئران الحاملة لأورام القولون، أظهرت خلايا CD8 التي تفتقر إلى ZFP148 داخل الورم علامات تنشيط أقوى ومزيدًا من خلايا المؤثرات المملوءة بالحبيبات والفعالة. بمفردها، حسنت هذه التغيرات السيطرة على الورم بشكل معتدل. لكن عند دمجها مع جسم مضاد يعيق نقطة التفتيش المناعي PD-1—وهو علاج مناعي شائع للسرطان—كانت الفوائد ملحوظة. تقلصت الأورام أكثر وعاشت الفئران لفترة أطول عندما كانت خلايا CD8 تفتقر إلى ZFP148، مقارنة بعلاج حجب PD-1 وحده. وكان التحسن مرتبطًا بتوسع مجموعة من الخلايا التائية السريعة الانقسام والشديدة السمية داخل بيئة الورم.
دلائل من أورام بشرية
لاختبار ما إذا كانت المبادئ نفسها تنطبق على البشر، أعاد المؤلفون تحليل مجموعات كبيرة من بيانات الخلية الواحدة من أورام بشرية وأجروا تحريرًا جينيًا في خلايا T بشرية في المختبر. عبرت خلايا CD8 النازحة إلى الورم ذات المستويات المنخفضة من النظير البشري، ZNF148، عن المزيد من جزيئات المؤثرات ومستقبلات شبيهة بالخلايا القاتلة الطبيعية، وسجلت درجات أعلى في تواقيع النشاط السمي وخبرة مستقبل الخلية التائية. أدى خفض ZNF148 تجريبيًا في خلايا CD8 بشرية إلى زيادة إنتاج عوامل التهابية وقاتلة رئيسية. عبر عدة مجموعات مرضى سرطانية، بدا أن المرضى الذين تحملت أورامهم مستويات أقل من ZNF148، أو الذين كانت خلايا T لديهم تحمل نمطًا جينيًا «شبيهًا بفقدان ZFP148»، عاشوا لفترة أطول واستجابوا بشكل أفضل للعلاجات التي تعيق نقاط التفتيش مثل حجب PD-1 أو CTLA-4.
لماذا يهم هذا لعلاجات المستقبل
تضع هذه الدراسة ZFP148 كآلية فرملية جزيئية محفوظة توجه خلايا T القاتلة بعيدًا عن أن تصبح مهاجمين مكتملين. من خلال قمع KLF2 والحفاظ على إغلاق مناطق DNA الرئيسية، يحد ZFP148 من تكوّن وتوسع أكثر الخلايا فعالية في مكافحة السرطان والفيروسات. في الفئران، يؤدي تعطيل هذه الفرملة إلى تضخيم فوائد العلاجات المناعية القائمة على PD-1، وتشير الأنماط المرصودة في الأورام البشرية إلى أن نفس الاستراتيجية قد تساعد في تحديد المرضى الأرجح استجابتهم—أو أن تكون هدفًا دوائيًا جديدًا لتعزيز المناعة. ببساطة، تقليل نشاط ZFP148 قد يساعد قتلتنا الداخلية على البقاء أكثر نشاطًا وضرب أهدافهم بقوة أكبر.
الاستشهاد: Xiao, T., Chen, X., Song, NJ. et al. ZFP148 is a transcriptional repressor of cytolytic effector CD8+ T cell differentiation. Nat Immunol 27, 827–840 (2026). https://doi.org/10.1038/s41590-026-02461-2
الكلمات المفتاحية: خلايا T CD8, إرهاق الخلايا التائية, المناعة ضد السرطان, عوامل النسخ, العدوى المزمنة