Clear Sky Science · ar
من النيكوتين إلى مضادات فيروسات SARS-CoV-2 بفعالية قوية في الكائن الحي وطيف واسع مضاد للفيروسات التاجية
لماذا تهم هذه الدراسة للحياة اليومية
مع استمرار دوران COVID-19 وظهور متحوِّرات جديدة، لا نزال بحاجة إلى حبوب مضادة للفيروسات أفضل تعمل بشكل موثوق، وسهلة الاستخدام، وتظل فعالة عندما يتحور الفيروس. تصف هذه الدراسة رحلة غير متوقعة تبدأ بمكوّن في دخان السجائر وتنتهي بمركبين تجريبيين قويين يمكنهما إيقاف مجموعة واسعة من الفيروسات التاجية في الحيوانات. للقراء غير المتخصصين، الرسالة الأساسية هي أن الباحثين يتعلمون كيف يصممون أدوية أذكى قد تحمينا ليس فقط من فيروس كورونا الحالي، بل من الفيروسات التاجية المستقبلية أيضاً.
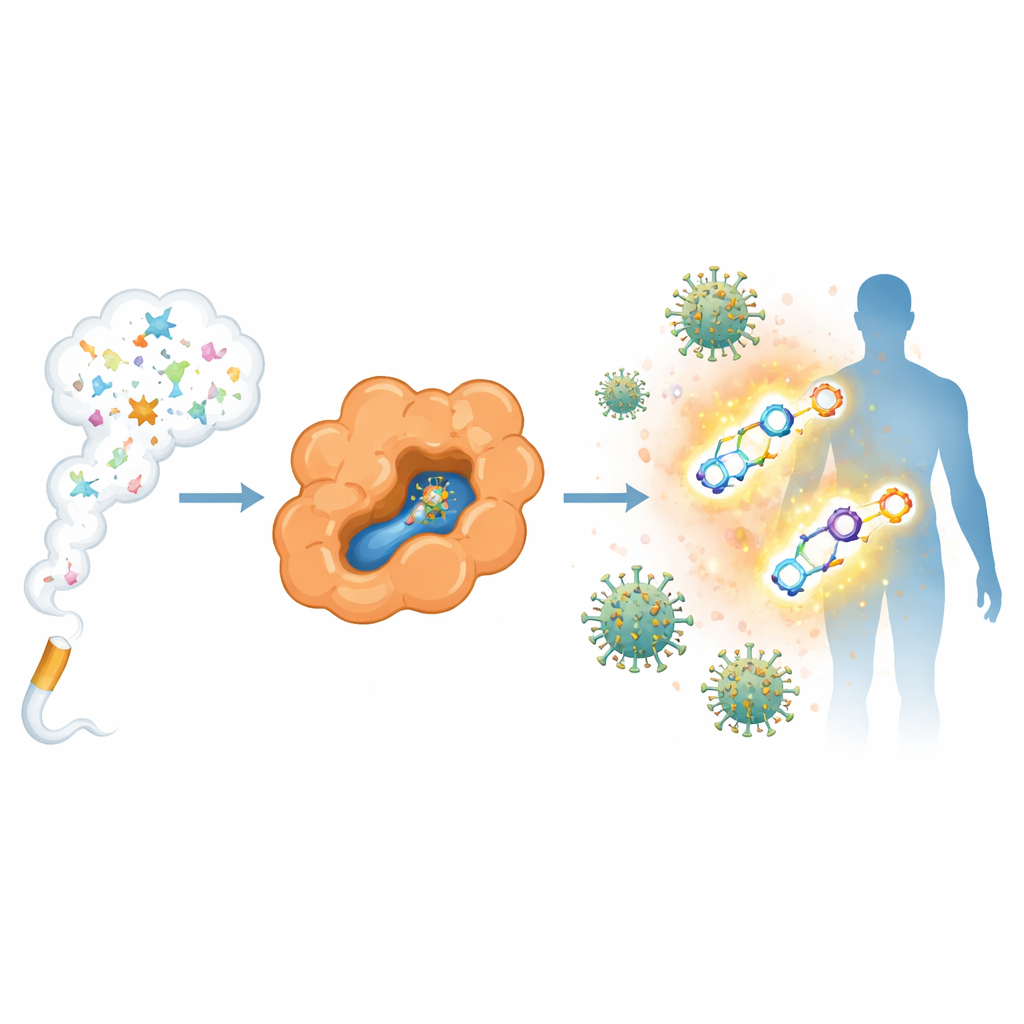
من إشارة دخان محيرة إلى دليل مخبري
في المراحل المبكرة من الجائحة، أشارت سجلات المستشفيات إلى وجود مدخنين نشطين أقل بين مرضى COVID-19 مما كان متوقعاً. لم تؤيد الأعمال اللاحقة فكرة أن التدخين يحمي، ومن الواضح أن التدخين ضار بالصحة. مع ذلك، دفعت هذه الظاهرة الغريبة الباحثين لطرح سؤال أضيق: هل يمكن لأي جزيئات مرتبطة بالنيكوتين أن تتفاعل مع آليات فيروس كورونا؟ ركز الفريق على البروتيز الرئيسي للفيروس، وهو إنزيم يقص البروتينات يحتاجه الفيروس للتكاثر. نقعوا بلورات هذا البروتيز في تركيزات عالية من جزيئات مرتبطة بالنيكوتين وفحصوها بواسطة حيود الأشعة السينية، وهي طريقة تكشف كيف تستقر الجزيئات الصغيرة داخل تجاويف البروتين.
العثور على قطعة بداية صغيرة لدواء جديد
من بين جميع المركبات ذات الصلة بالتبغ التي اختبروها، كان هناك واحد فقط—3-فينيلبيريدين—يظهر بوضوح وهو يمسك بتجويف رئيسي في بروتيز الفيروس. بمفرده، كان هذا الجزيء الصغير مثبطاً ضعيفاً، لكنه ارتبط تقريباً في نفس المكان والاتجاه كجزء من نيرماتريلڤير، مثبط البروتيز المستخدم في دواء COVID-19 باكسلوفيد. والأهم أن 3-فينيلبيريدين لم يعتمد على تلامس محدد مع بقاعدة في البروتيز تُسمى E166. العديد من الأدوية الحالية تحتاج ذلك الاتصال، وعندما يتحور الفيروس في الموضع E166 قد يصبح أقل حساسية للعلاج. طرح هذا فكرة واعدة: عبر مزج خصائص 3-فينيلبيريدين مع خصائص نيرماتريلڤير، قد يكون من الممكن بناء أدوية جديدة ترتبط بقوة دون أن تكون عرضة بشدة لتحولات المقاومة تلك.
تصميم مثبطات بروتيز أقوى وأذكى
دخل العلماء بعد ذلك مرحلة «ضبط» في كيمياء الأدوية. بنوا أولاً جزيئات هجينة جمعت النواة التفاعلية لنيرماتريلڤير مع حلقة بيريدين موضوعة في المكان الذي شوهدت فيه 3-فينيلبيريدين. خطوة بخطوة، بدّلوا عدة مناطق من الجزيئات—غيروا أنواع الحلقات، أضافوا مجموعات صغيرة مثل الفلوراين، واستبدلوا سلاسل جانبية—لتحسين مدى احكام المركبات في تجويف البروتيز وكيفية دخولها وبقائها داخل الخلايا. فحصوا كل مرشح في سلسلة من الاختبارات: مدى قدرته على حجب الإنزيم المنقى، مدى حمايته للخلايا البشرية من الضرر الناتج عن نشاط البروتيز، ومدى فعاليته في إيقاف تكاثر فيروس كورونا حي في مزروعات خلوية. ومن خلال هذه العملية برزا مركبان متميزان، أطلق عليهما YR-C-136 وSR-B-103، وكلاهما أقوى في الاختبارات المخبرية من نيرماتريلڤير وأقل تأثراً بمضخات الأدوية الخلوية التي قد تضعف بعض الأدوية.
اختبار المرشحين الجدد في الحيوانات
بعد ذلك، تساءل الفريق عما إذا كانت هذه المركبات تتصرف كأدوية فعلية داخل أجسام حية. في الفئران، أظهرت مركبات YR-C-136 وSR-B-103 «حرائك دوائية» مواتية: بقيت في مجرى الدم بمستويات مفيدة لفترة أطول وبتركيزات ذروة مماثلة مقارنة بنيرماتريلڤير عند إعطائها عن طريق الفم. عندما أُصيبت فئران إناث بسلالة SARS-CoV-2 معدلة لتناسب الفئران وعولجت عن طريق الفم، خفض كلا المركبين الجديدين كمية الفيروس في الرئتين بشكل دراماتيكي—بنحو 70 إلى 120 ضعفاً—أكثر بكثير من نيرماتريلڤير عند نفس الجرعة. أظهرت أنسجة الرئة من الحيوانات المعالجة أضراراً واحتقانات أقل بكثير، مما يشير إلى أن الأدوية لم تقلل مستوى الفيروس فقط، بل ساعدت أيضاً في الوقاية من التغيّرات المرضية الشديدة.
مواجهة المقاومة والفيروسات التاجية المستقبلية
القلق الرئيسي مع أي مضاد فيروسات هو أن الفيروس قد يتطور ليهرب منه. اختبر المؤلفون مركباتهم ضد نسخة من البروتيز تحمل تغييرين (E166V وL50F) معروفين بتقليل حساسية SARS-CoV-2 لنيرماتريلڤير. لا تزال كل من YR-C-136 وSR-B-103 تثبطان هذا الطفر جيداً، مع فقدان في الفاعلية بمقدار ضعفين إلى ثلاثة أضعاف فقط، وهو انخفاض معتدل مقارنة بالخسارة التي تُرى مع نيرماتريلڤير. كما تحدى الفريق مجموعة من فيروسات تاجية مختلفة—بما في ذلك عدة متغيرات من SARS-CoV-2 مثل دلتا وأوميكرون، فضلاً عن فيروسات تاجية بشرية أقدم مثل OC43 و229E وSARS-CoV وMERS-CoV. في المزروعات الخلوية، منعت المركبات الجديدة جميعها، غالباً عند تركيزات منخفضة جداً، مما يظهر إمكانات واسعة بطيف «كاسح للفيروسات التاجية».
ماذا يعني هذا العمل للمستقبل
لا تشير هذه الأبحاث إلى أن التدخين مفيد؛ بل تُظهر كيف يمكن لقطعة كيميائية صغيرة مرتبطة بالنيكوتين، اكتشفت في بيئة مختبرية محكومة للغاية، أن تلهم أدوية أكثر فعالية. عبر رسم خرائط دقيقة لكيفية جلوس تلك القطعة والأدوية القائمة في بروتيز الفيروس، بنى العلماء مركبات هجينة أقوى، وأقل عرضة لطرق المقاومة المعروفة، ومفعولها ضد العديد من الفيروسات التاجية في نماذج ما قبل السريرية. بينما لا يزال يتعين على YR-C-136 وSR-B-103 اجتياز اختبارات صارمة للسلامة والفعالية في البشر، فإنهما يمثلان نماذج واعدة لأقراص مضادة للفيروسات من الجيل التالي قد تساعد في علاج عدوى COVID-19 الحالية وتكون أدوات مهمة عند ظهور تهديد فيروس تاجي جديد.
الاستشهاد: Khatua, K., Atla, S., Coleman, D. et al. From nicotine to SARS-CoV-2 antivirals with potent in vivo efficacy and a broad anti-coronavirus spectrum. Nat Commun 17, 2782 (2026). https://doi.org/10.1038/s41467-026-69527-5
الكلمات المفتاحية: البروتيز الرئيسي لـ SARS-CoV-2, تصميم أدوية مضادة للفيروسات, مقاومة الفيروسات التاجية, الاكتشاف القائم على الشظايا, مضادات فيروسات واسعة الطيف