Clear Sky Science · ar
اللايسين يخفف إصابة الرئتين الحادة عبر استعادة أسيتلة α‑تيوبولين ونشاط الأهداب
لماذا هذا مهم لصحة الرئة
يمكن أن تحول إصابة الرئة الشديدة عدوى أو تعرضًا سامًا إلى أزمة تهدد الحياة، ما يجعل المرضى يعتمدون على أجهزة التنفس وإذا نجاوا فمعرضين لاحتمال تشكل تندب دائم. تستكشف هذه الدراسة مساعدًا بسيطًا مفاجئًا: الحمض الأميني الشائع اللايسين. يظهر الباحثون أن اللايسين يمكن أن يساعد الرئتين المصابة على إصلاح نفسها في نماذج حيوانية عبر دعم هياكل شعرية دقيقة على خلايا المجرى الهوائي وتثبيت الحاجز الذي يحافظ على سلامة الحويصلات الهوائية.
عندما ينحرف إصلاح الرئة عن مساره
تنشأ إصابة الرئة الحادة وصيغتها الشديدة متلازمة الضائقة التنفسية الحادة من إهانات كبيرة مثل الالتهاب الرئوي الفيروسي، أو مواد كيميائية سامة مثل الباراكووات، أو الإشعاع، أو العلاج الكيميائي. في هذه الحالات يُتلف البطانة الرقيقة للحويصلات الهوائية، ويتراكم السائل والخلايا الالتهابية، ويتقدم بعض المرضى إلى تندب دائم يُسمى التليف الرئوي. خلايا الإصلاح الرئيسية في الرئة، المعروفة بالخلايا السنخية من النوع الثاني، يمكن أن تتجدد لتعطي سطح الحويصلة الطبيعي أو تنزلق إلى حالات مكونة للندب. استخدم المؤلفون عينات بشرية ونماذج حيوانية لتسمم الباراكووات، وهو سبب معروف لضرر رئوي كارثي، لفهم ما الذي يميل بهذا التوازن نحو الشفاء أو نحو التليف.
عجز طاقة خفي في الخلايا الرئوية المصابة
من خلال تحليل بيانات تسلسل RNA للخلايا المفردة من مرضى وقياس المستقلبات في الدم، وجد الفريق أن خلايا الظهارة الرئوية تخضع لتحول أيضي عميق أثناء الإصابة الشديدة. تُجهد المسارات الميتوكوندرية التي تولد الطاقة عادة إلى أقصاها، وتبدأ الخلايا باستهلاك الأحماض الأمينية بشدة، لا سيما اللايسين. في كل من المرضى والفئران، انخفضت مستويات اللايسين وعدد من الأحماض الأمينية الأساسية في الدم، مما يشير إلى أنها تُحرق كوقود احتياطي. وفي الوقت نفسه، صعدت التعبيرات الجينية المرتبطة بتفكيك اللايسين إلى أسيتيل‑CoA، وهو مركب محوري في الأيض. هذا أشار إلى استقلاب اللايسين كمسار «إنقاذ» رئيسي يساعد الخلايا المنهكة على الاستمرار عندما تتعطل مسارات السكر والدهون.
اللايسين يساعد الرئات التالفة على التعافي
لاختبار ما إذا كان يمكن تحويل هذه الدلالة الأيضية إلى علاج، أعطى الباحثون مكملات اللايسين لفئران ورئيسيات غير بشرية مصابة بتسمم الباراكووات. وكانت النتائج لافتة: في الفئران تحسنت البقاء على قيد الحياة من عدم وجود أي ناجين في المجموعة غير المعالجة إلى ما يقرب من ثلثي الحيوانات المعطاة اللايسين. أظهرت رئات الحيوانات المُكمّلة ترسبات أقل للكولاجين وسمكًا أقل في الأنسجة، مما يدل على تقليل التليف، وكانت علامات التهاب الحويصلات التقليدية مخففة بشكل ملحوظ. عادت ملفات التعبير الجيني، التي كانت مضطربة بشدة بفعل الباراكووات، إلى أقرب ما يكون إلى الوضع الطبيعي مع علاج اللايسين. تعافت مؤشرات أنواع الخلايا الظهارية الرئيسية التي تشكل الحاجز بين الهواء والدم، لا سيما الخلايا السنخية من النوع الثاني والنوع الأول. وفي الوقت نفسه، انخفض استقدام الخلايا المناعية وعلامات الالتهاب الجهازية، بما يتوافق مع فائدة ثانوية ناجمة عن حفاظ أفضل على حاجز الظهارة.
«فرش» خلوية دقيقة والتحكم بالكالسيوم
بالتعمق أكثر، اكتشف المؤلفون أن الفعل الرئيسي للايسين كان بنيويًا قدر ما هو أيضي. قلل إصابة الباراكووات من بروتينات التصاق ظهارية مهمة مثل E‑cadherin وZO‑1، مما أضعف الختم بين الخلايا المجاورة، وكبح نمو وعمل الأهداب الأولية — بروزات مجهرية تستشعر بيئة الخلية. أعادت مكملات اللايسين الأسيتلة على α‑تيوبولين، وهي تعديلة لازمة لبناء أهداب مستقرة، وأعادت أعداد وطول الأهداب نحو الوضع الطبيعي. ساعدت هذه الأهداب المستعادة على إعادة تموضع بروتين قناة الكالسيوم TRPC1 بعيدًا عن السطح الخلوي المسطح ونحو الهدب. ونتيجة لذلك انخفض التدفق الضار للكالسيوم إلى داخل الخلية، هدأت إشارات حساسة للكالسيوم في المسار التتابعي، وتعافى مستوى E‑cadherin وZO‑1، مما ساعد الخلايا على الاحتفاظ بهويتها الظهارية المنظمة بدل الانزلاق إلى حالات تشبه الندب. ومن الجدير بالذكر أن الأهداب كانت أكثر بروزًا على مجموعة فرعية من الخلايا السنخية من النوع الثاني، مما يشير إلى أن اللايسين يدعم هذه الخلايا السلفية الحيوية بشكل خاص.
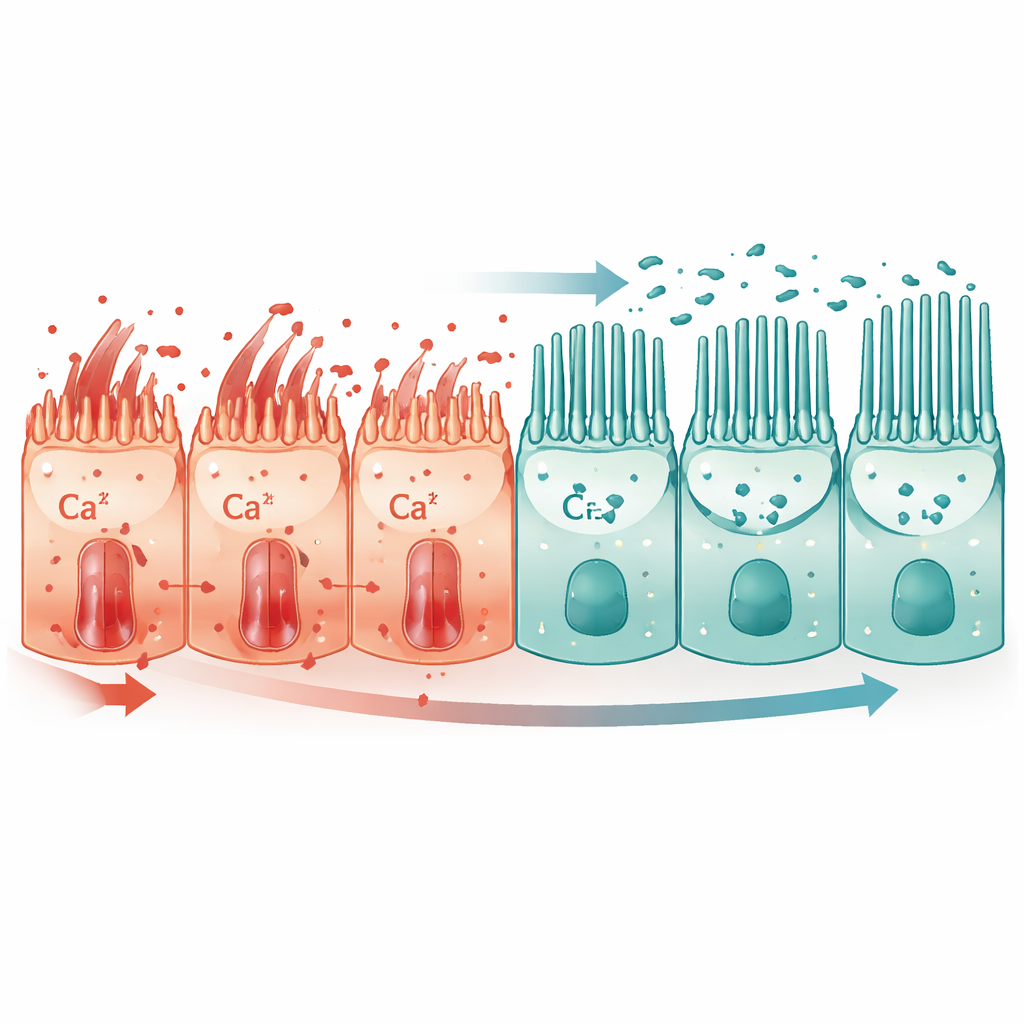
الكالسيوم في الدم كعلامة إنذار
نظرت الدراسة أيضًا إلى الخارج، إلى مسار الدم. في المرضى المتسممين بالباراكووات كانت مستويات الكالسيوم المصلية أقل بشكل ملحوظ مقارنة بالمتطوعين الأصحاء وواصلت الانخفاض مع زيادة مستويات الباراكووات في الدم وتفاقم إصابة الكلى. في كل من الفئران والرئيسيات خفض الباراكووات الكالسيوم في الدم، بينما أعاده علاج اللايسين جزئيًا. إلى جانب بيانات مستوى الخلايا، يشير هذا إلى اضطراب في تعامل الجسم مع الكالسيوم كخاصية مركزية للإصابة الرئوية الشديدة ويضع تطبيع اللايسين لتدفقات الكالسيوم كجزء أساسي من تأثيره الحامي.
ماذا قد يعني هذا للمرضى
بعبارة بسيطة، يقترح المؤلفون أن اللايسين يعمل كدعم ذو غرضين: يعيد تزويد الخلايا الرئوية المتوترة بالمكوّن الأيضي أسيتيل‑CoA ويستخدم ذلك الوقود لتقوية الهيكل الدقيق الذي يربط الخلايا ببعضها ويدعم أهدابها. من خلال استعادة هذه «الفرش» الصغيرة وشد الوصلات بين الخلايا، يساعد اللايسين على تهدئة إشارات الكالسيوم الجامحة التي كانت ستدفع الخلايا نحو التندب. وبما أن اللايسين يُستخدم سريريًا بالفعل وأظهر فوائد في نماذج حيوانية متعددة، فإن العمل يقترح أن تجارب مصممة بعناية قد تختبره كعلاج تكميلي آمن لإصابة الرئة الحادة وربما للوقاية من التليف اللاحق.
الاستشهاد: Yang, W., Meng, X., Zhu, Y. et al. Lysine attenuates acute lung injury by restoring α-tubulin acetylation and ciliary activity. Cell Death Discov. 12, 150 (2026). https://doi.org/10.1038/s41420-026-03025-x
الكلمات المفتاحية: إصابة الرئة الحادة, اللايسين, خلايا ظهارة الحويصلات الهوائية, الأهداب, إشارة الكالسيوم