Clear Sky Science · zh
使用超极化和低场弛豫进行配体结合的单次扫描检测
这对未来药物的意义
设计新药常常从一个简单的问题开始:这个小分子真的会与我们关心的蛋白结合吗?核磁共振(NMR)是观察溶液中此类结合的有力手段,但通常需要大量贵重的蛋白质。本研究提出了一种巧妙方法,通过增强NMR信号并利用在低磁场下分子运动的特性来缩减这些需求,从而为更高效、更经济的药物发现实验打开了大门。
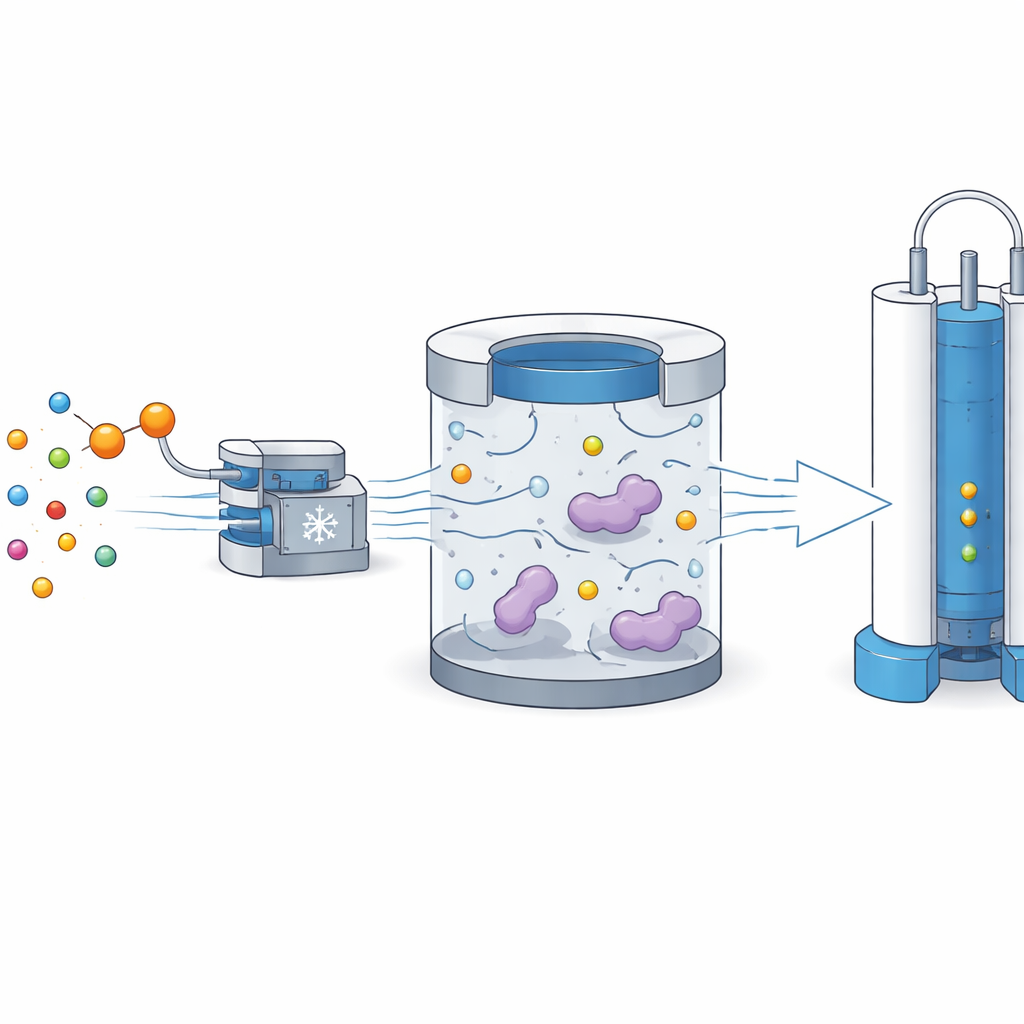
观察分子内部的微小磁体
NMR 检测的是原子“自旋”的行为,即位于氢或碳等核内的微小磁体。当小分子配体与大蛋白结合时,其转动变慢,这会影响自旋在被激发后回到平衡状态的速度。传统的NMR筛选方法主要跟踪横向弛豫(称为 T2),它在配体结合时会发生变化。相比之下,作者关注纵向弛豫(T1),T1 对分子翻转速率也十分敏感,而且在低于常规高分辨NMR所用的磁场时,其信息量会显著增加。
放大信号并利用低场等待时间
团队结合了两种思路:超极化和低场弛豫。首先,他们用称为动态核极化的方法在极低温和高磁场下显著增强了报告配体上一个特殊标记碳原子的信号。随后,他们并不立即测量,而是快速溶解样品并将其转移到约1.3特斯拉的中等磁场,在那里将配体与目标蛋白混合。在这个较低磁场下的10秒等待期内,结合到蛋白的配体因转动变慢而弛豫得更快,经历更强的波动磁场,因此其信号下降明显快于不结合的配体。
在单次NMR扫描中读取结合信息
经过低场暂停后,溶液被转入常规高场NMR磁体。在那里,配体剩余的增强碳极化被用标准脉冲序列转换为可检测的氢信号。研究人员从每次超极化射次中记录两个谱图:第一个主要反映低场下发生了多少T1弛豫,而第二个在自旋锁下探测类似T2的过程。通过比较有无蛋白条件下这两个谱图的强度,他们定义了简单的评分来报告是否发生了结合。仅用14微摩尔的13C标记丙酮酸报告分子,他们就能清晰检测到对与癌症相关酶PHD1的结合——即使蛋白浓度仅为2微摩尔——并且只需一次扫描,而非多次重复测量。
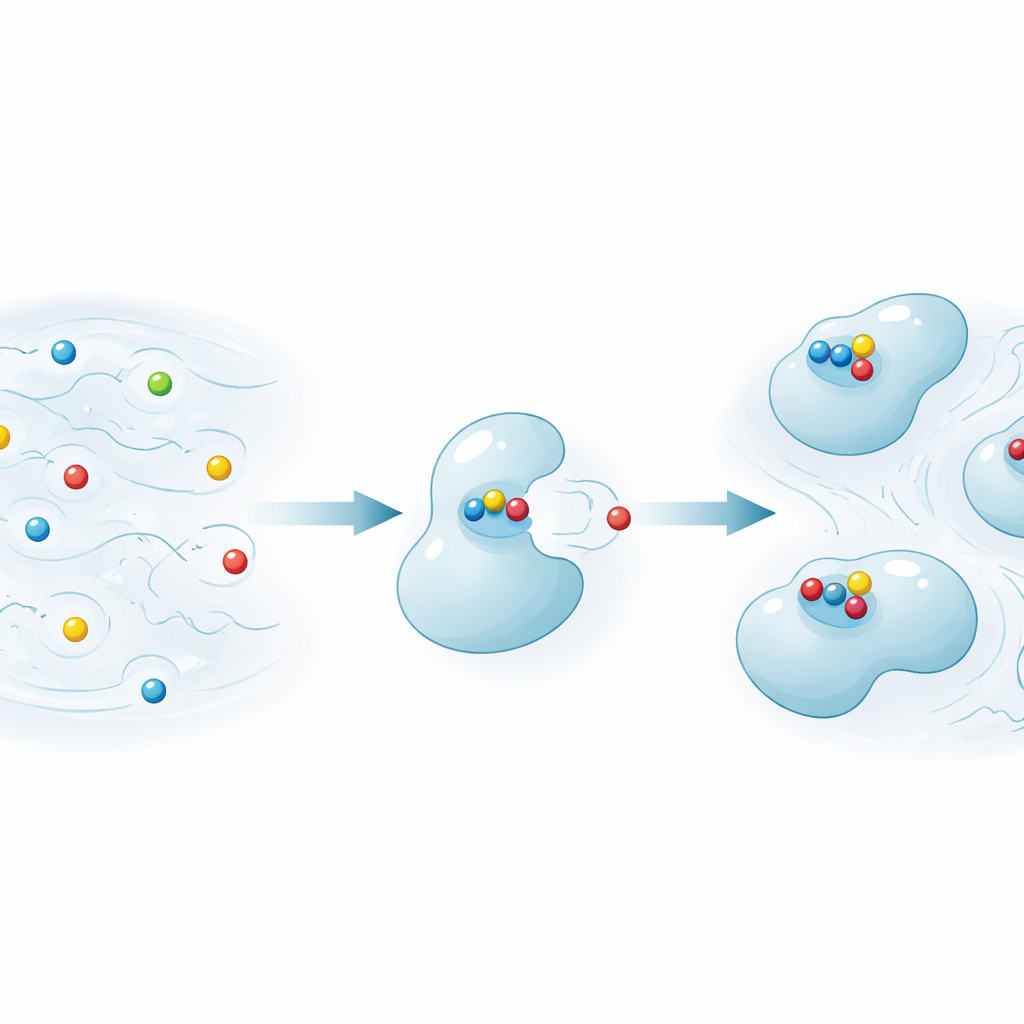
测试竞争与灵敏度
该方法还能够揭示未标记配体何时竞争相同的结合位点。作者加入了一个强竞争分子,将标记的报告分子从蛋白上置换下来。随着竞争分子阻断了蛋白与报告分子的相互作用,报告分子在高场的信号会回升到接近无蛋白时的水平。这一变化在基于T1的低场评分中最为明显,而更传统的基于T2的测量有时接近噪声水平。在相似条件下重复实验表明,超极化过程具备足够的重复性,使得由蛋白结合引起的信号变化——以及竞争分子抑制结合时的信号恢复——能够可靠地被识别。
这对药物发现意味着什么
简单来说,作者把低场等待时间变成了一种对分子是否结合蛋白高度敏感的测试。通过以超极化配体为起点,他们可以使用非常低的浓度却仍获得强烈的NMR信号;通过测量低场暂停期间损失了多少信号,可以得到结合与未结合状态之间的清晰对比。这种方法将所需的蛋白浓度降至低微摩尔范围,当蛋白难以制备时这是一个重要优势。随着进一步改进,例如将更多步骤在低场完成或采用微流控装置,这一策略有望成为筛选药物候选物的实用工具,同时消耗远少于以往的珍贵蛋白材料。
引用: Narwal, P., Lorz, N., Minaei, M. et al. Single-scan detection of ligand-binding using hyperpolarization and low-field relaxation. Commun Chem 9, 140 (2026). https://doi.org/10.1038/s42004-026-01934-7
关键词: NMR 配体结合, 超极化, 低场弛豫, 药物发现, 蛋白–配体相互作用