Clear Sky Science · he
גילוי קשירת ליגנדים בסריקה יחידה באמצעות היפרפולריזציה והרפיה בשדה נמוך
מדוע זה חשוב עבור תרופות עתידיות
עיצוב תרופות חדשות מתחיל לעתים קרובות משאלה פשוטה: האם המולקולה הקטנה הזו אכן נקשרת לחלבון שמעניין אותנו? תהודה מגנטית גרעינית (NMR) היא כלי עוצמתי לצפייה בקשירה כזו בתמיסה, אך בדרך כלל היא דורשת כמויות גדולות של חלבון יקר. המחקר הזה מציג דרך חכמה לצמצם את הדרישות הללו על ידי הגברת אות ה-NMR וניצול תנועת המולקולות בשדה מגנטי נמוך, מה שפותח פתח לניסויי גילוי תרופות יעילים וחסכוניים יותר.
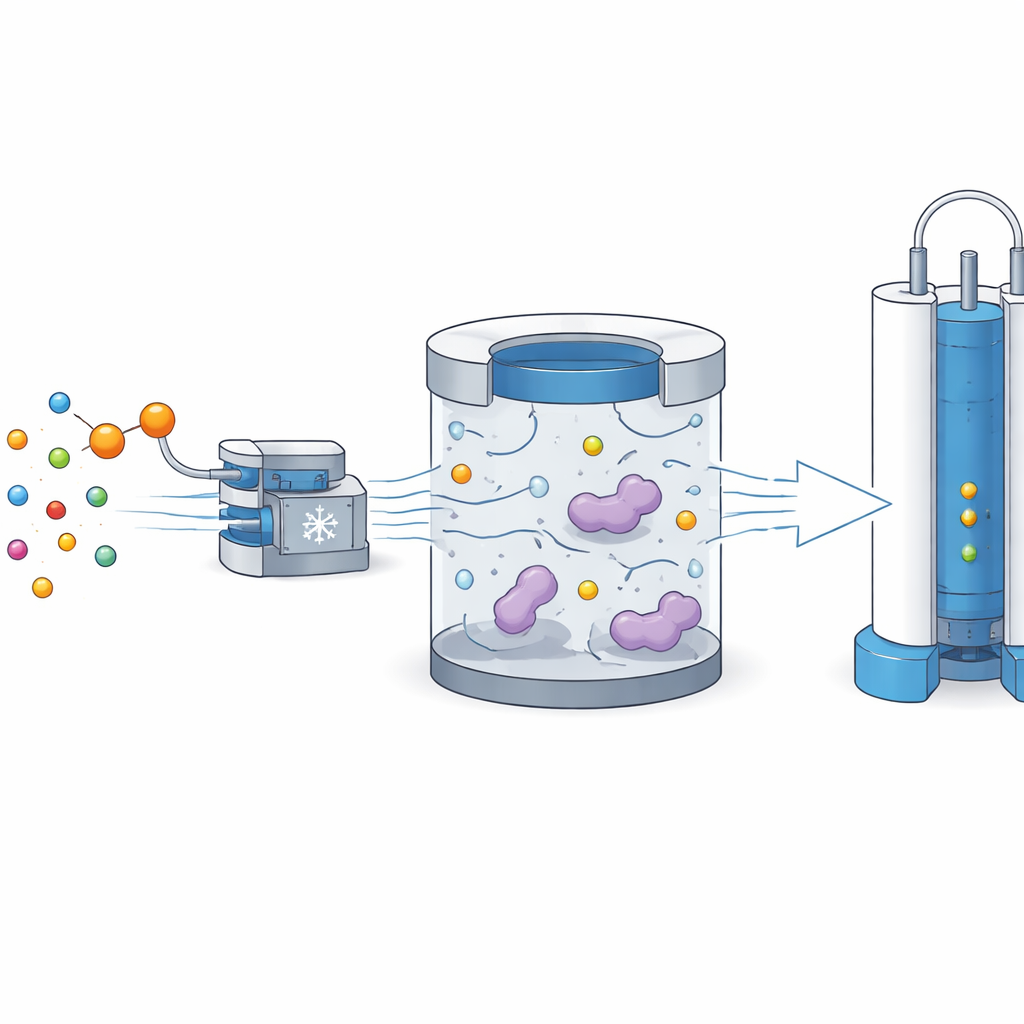
צפייה במגנטים זעירים בתוך מולקולות
פעולת ה-NMR מבוססת על זיהוי התנהגות ה"ספינים" האטומיים, מגנטים זעירים בתוך גרעינים כמו מימן או פחמן. כאשר ליגנד מולקולרי קטן נקשר לחלבון גדול, תנועתו מאטה, וזה משפיע על קצב הרפיית הספינים חזרה למצב המנוחה לאחר גירוי. שיטות סקר NMR מסורתיות עוקבות בעיקר אחרי הרפיה צידית (המכונה T2), שמשתנה בעת קשירה. לעומת זאת, המחברים מתמקדים בהרפיה לאורך (T1), שגם היא רגישה לקצב הסיבוב של המולקולה אך נעשית אינפורמטיבית הרבה יותר בשדות מגנטיים נמוכים מאלה המשמשים בדרך כלל ל-NMR ברזולוציה גבוהה.
הגברת אותות ושימוש בזמן המתנה בשדה נמוך
הקבוצה משלבת שתי רעיונות: היפרפולריזציה והרפיה בשדה נמוך. ראשית, הם מגבירים באופן דרמטי את האות של אטום פחמן מסומן בליגנד מדווח באמצעות שיטה שנקראת דינמית פולריזציה גרעינית בטמפרטורה מאוד נמוכה ושדה גבוה. לאחר מכן, במקום למדוד מיד, הם ממיסים במהירות את הדוגמה ומעבירים אותה לשדה מגנטי מתון של כ-1.3 טסלה, שם הליגנד מעורבב עם חלבון היעד. במהלך תקופת המתנה של 10 שניות בשדה הנמוך הזה, ליגנדים שנקשרים לחלבון נרפים מהר הרבה יותר מאלו שנשארים חופשיים, משום שתנועתם האטה והם חווים שדות מגנטיים מתנדנדים חזקים יותר.
קריאת קשירה בסריקה יחידה של NMR
לאחר העצירה בשדה הנמוך, התמיסה מועברת למגנט NMR קונבנציונלי בשדה גבוה. שם, המפלור המוגבר שנותר של אטום הפחמן בליגנד מומר לאותות מימן הניתנים לגילוי באמצעות רצף פולסים סטנדרטי. החוקרים מקליטים שני ספקטרות מכל זריקה היפרפולריזית: הראשונה משקפת בעיקר כמה הרפיית T1 התרחשה בשדה הנמוך, בעוד שהשנייה בוחנת תהליך דמוי T2 תחת כנף סיבוב (spin-lock). על ידי השוואת האינטנסיביות של שתי הספקטרות עם ובלי חלבון, הם מגדירים סקורים פשוטים המדווחים האם התרחשה קשירה. באמצעות רק 14 מיקרומולר של פירובט מתויג בפחמן-13 הם מצליחים לזהות בבירור קשירה לאנזים הקשור לסרטן, PHD1, גם כאשר ריכוז החלבון הוא רק 2 מיקרומולר — ובכך עושים זאת בסריקה יחידה במקום במספר מדידות חוזרות.
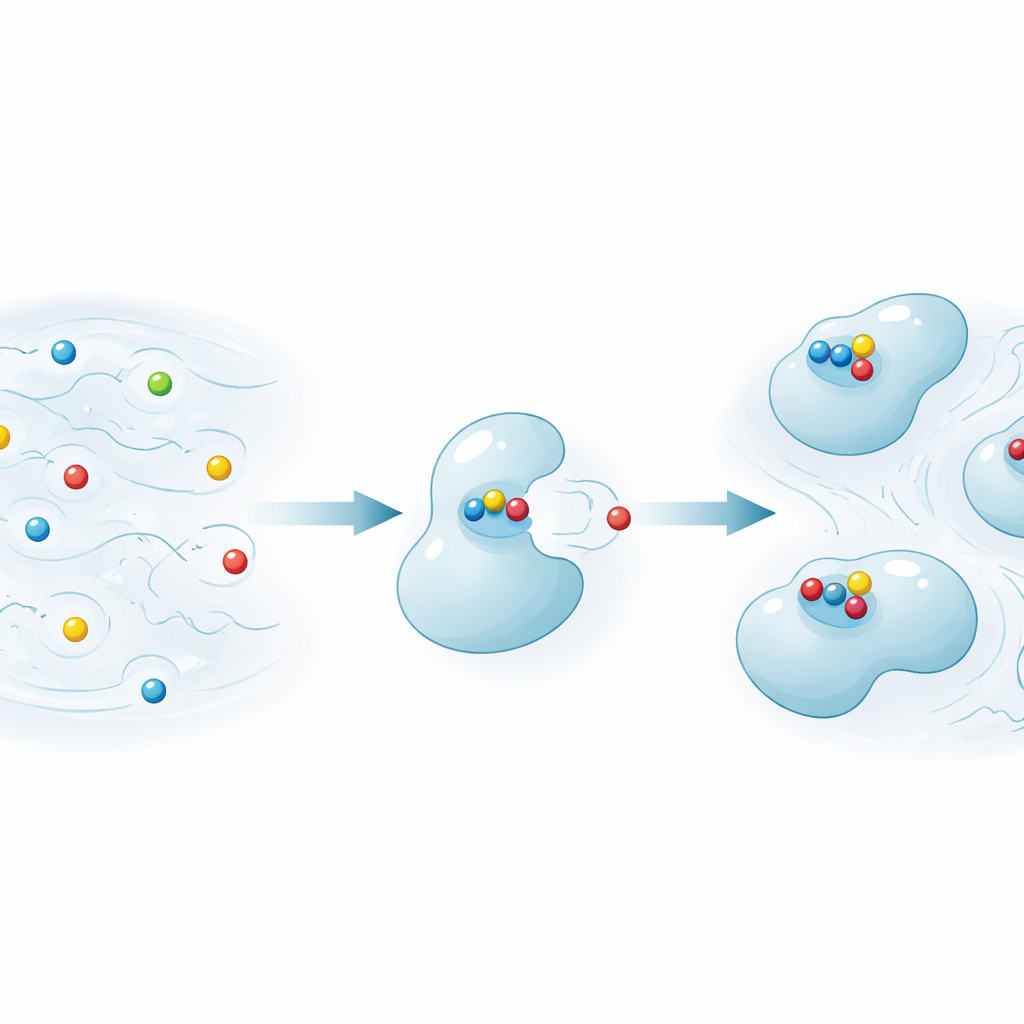
בדיקת תחרות ורגישות
השיטה מסוגלת גם לחשוף מתי ליגנד לא מתויג מתחרה על אותו אתר קשירה. המחברים מוסיפים מולקולת מתחרה חזקה שמדיחה את הדיוחן המסומן מהחלבון. כאשר המתחרה חוסם את האינטראקציה בין החלבון לדיוחן, האות של הדיוחן בשדה גבוה חוזרת לכיוון הרמה של חופשי־חלבון. שינוי זה מתבטא בבירור בעיקר בסקור המבוסס על T1 בשדה הנמוך, בעוד שהמדידה היותר שגרתית המבוססת על T2 לעיתים נשארת קרובה לרעש. חזרה על ניסויים בתנאים דומים מראה שהתהליך של היפרפולריזציה חוזר על עצמו מספיק כך ששינויים באות הנובעים מקשירת חלבון — ומהמדיכוי שלה על ידי מתחרה — בולטים באופן אמין.
מה המשמעות עבור גילוי תרופות
בקצרה, המחברים הפכו את זמן ההמתנה בשדה הנמוך למבחן רגיש מאוד לקשירת מולקולה לחלבון. על ידי התחלה מליגנד היפרפולריזי, הם יכולים לעבוד בריכוזים מאוד נמוכים ועדיין לראות אותות NMR חזקים, ועל ידי מדידת כמות האות שאבדה במהלך העצירה בשדה הנמוך הם מקבלים ניגוד ברור בין המצבים הקשורים לחוסרי הקשירה. גישה זו מפחיתה את ריכוז החלבון הנדרש לטווח המיקרומולרי הנמוך, יתרון משמעותי כאשר חלבונים קשים לייצור. עם שיפורים נוספים, כגון ביצוע חלקים גדולים יותר מהניסוי בשדה נמוך או בהתקנים מיקרופלואידיים, אסטרטגיה זו עשויה להפוך לכלי מעשי לסינון מועמדי תרופות תוך צריכת פחות חומר חלבוני יקר.
ציטוט: Narwal, P., Lorz, N., Minaei, M. et al. Single-scan detection of ligand-binding using hyperpolarization and low-field relaxation. Commun Chem 9, 140 (2026). https://doi.org/10.1038/s42004-026-01934-7
מילות מפתח: קשירת ליגנדים ב-NMR, היפרפולריזציה, הרפיה בשדה נמוך, גילוי תרופות, אינטראקציות חלבון–ליגנד