Clear Sky Science · zh
外泌体来源的ACLY抑制星形胶质细胞EAAT1导致POCD中的谷氨酸失衡与认知受损
为何手术后的记忆问题值得关注
许多老年人在大手术后会感觉思维和记忆“有问题”。这种被称为术后认知功能障碍的状况会延缓康复并削弱独立性,但其生物学机制长期不清晰。本研究揭示了大脑内的一连串反应,显示手术改变的免疫细胞如何扰乱脑内化学平衡并削弱学习与记忆所需的神经连接。
血液中的微小信使
研究者聚焦于细胞用来通过血液传递货物的微小囊泡,称为细胞外囊泡。他们从出现术后认知问题的患者和健康对照者的血液中分离出这些囊泡。当把受影响患者的囊泡注入衰老小鼠时,动物出现脑部炎症、谷氨酸水平升高以及在莫里斯水迷宫等记忆任务中的表现受损。详细的大脑记录显示,它们的突触——神经细胞相互交流的接触点——在应对刺激时增强能力下降,这是健康学习回路的重要特征。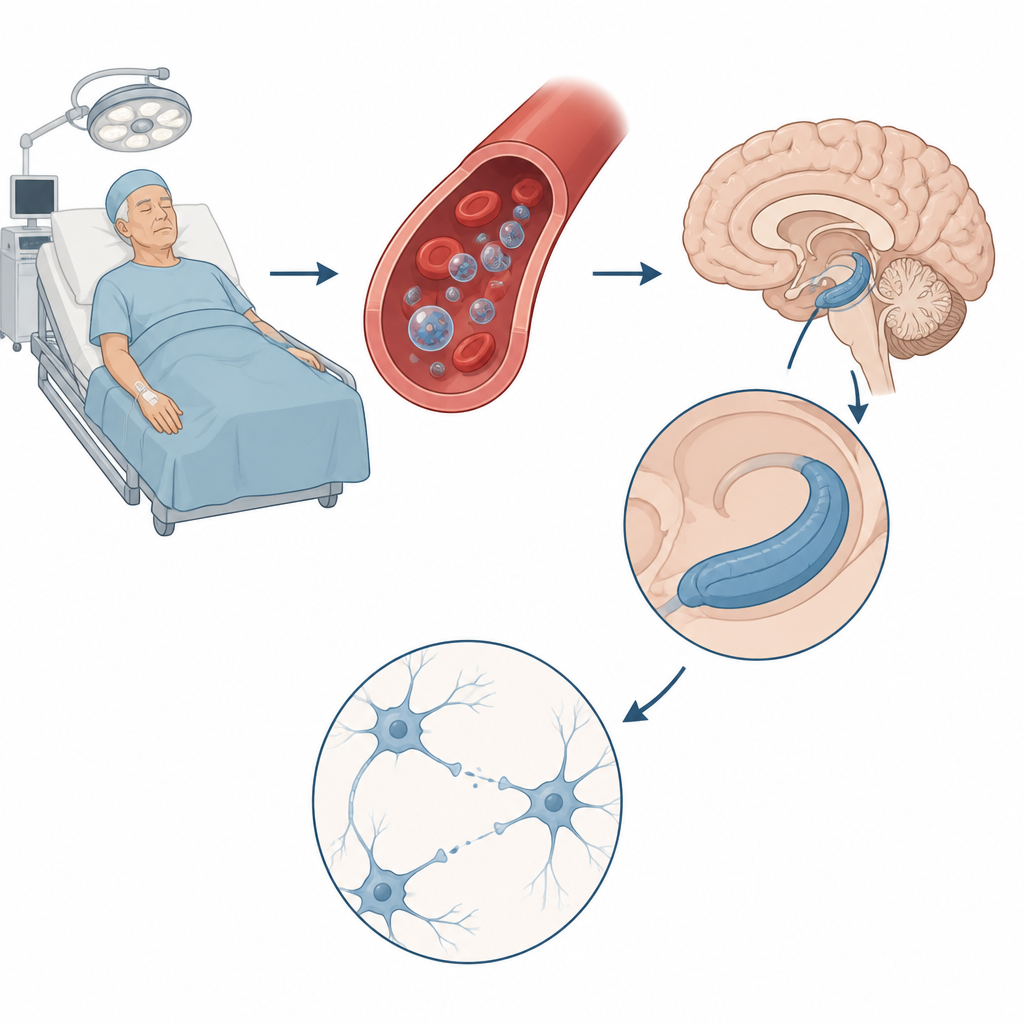
来自脑内免疫细胞的有害信息
进一步分析指向了微胶质细胞——大脑中的常驻免疫细胞——作为这些有害囊泡的重要来源。当实验室中激活微胶质细胞时,它们释放的囊泡中富含一种名为乙酰辅酶A裂解酶(ACLY)的酶。这些囊泡很容易被邻近的星形胶质细胞摄取,后者是维持脑内化学平衡的星形支持细胞。在小鼠中,用药物抑制微胶质细胞可大幅减少脑部炎症、降低谷氨酸积累、保护神经分支和棘突的结构,并在术后改善记忆表现,提示微胶质细胞的信号在此问题中居于核心地位。
支持细胞如何失去对谷氨酸的控制
星形胶质细胞通常像清道夫一样,通过一种名为EAAT1的转运蛋白清除神经细胞间隙中过量的谷氨酸。研究团队发现,囊泡携带的酶进入星形胶质细胞后会促进乙酰辅酶A的生成,这种小分子为控制基因活动的蛋白质上的化学标记提供底物。进而增加了转录调控蛋白NF-κB p65的修饰形式,该修饰型会结合到EAAT1基因并抑制其表达。EAAT1受抑后,星形胶质细胞无法有效清除谷氨酸,导致这种兴奋性化学物质在突触周围积聚,从而为神经元及其连接的损伤创造条件。
动物模型提供的证据
在老年小鼠中,将手术患者或激活微胶质细胞来源的囊泡注入海马会引发微胶质细胞和星形胶质细胞活化、树突棘丧失、突触信号减弱以及明显的记忆缺陷。当研究者使用基因工具去除这些囊泡中的酶,或阻断囊泡的释放或摄取时,星形胶质细胞恢复了EAAT1表达,谷氨酸水平回归正常,突触功能和行为表现得到改善。时间进程实验显示,重复暴露于囊泡会导致逐步恶化的突触功能和记忆,强调这是一个累积过程而非单次冲击。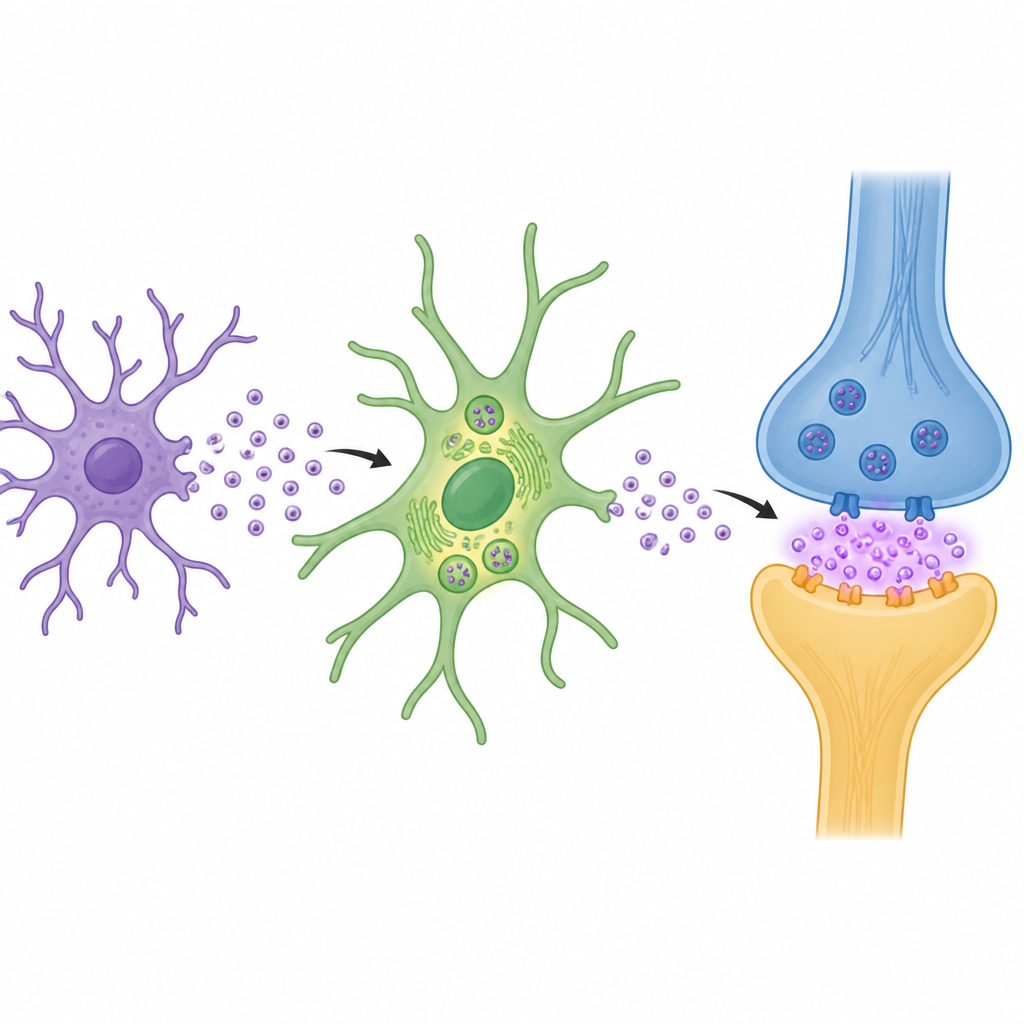
对患者意味着什么
通俗来说,这项研究表明术后大脑免疫细胞可能释放装载酶的囊泡,“重新编程”邻近的支持细胞,使它们清除谷氨酸的能力下降。由此产生的化学失衡在脆弱的老年大脑中悄然侵蚀突触与记忆。通过将这一路径识别为炎症、谷氨酸过载与认知下降之间的关键联系,研究为新的治疗思路提供了方向,例如在围手术期使用抑制该酶活性或限制囊泡运输的药物干预。
引用: Qi, Z., Ding, L., Zhao, Y. et al. Astrocytic EAAT1 suppression by EV-ACLY underlies glutamate imbalance and cognitive impairment in POCD. Commun Biol 9, 636 (2026). https://doi.org/10.1038/s42003-026-09888-1
关键词: 术后认知功能障碍, 微胶质细胞, 星形胶质细胞, 谷氨酸失衡, 细胞外囊泡