Clear Sky Science · ja
EV由来ACLYによるアストロサイトのEAAT1抑制はPOCDにおけるグルタミン酸不均衡と認知障害の基盤となる
なぜ手術と記憶障害が重要なのか
多くの高齢者は大きな手術の後で思考や記憶が「おかしい」と感じることがあります。この状態は術後認知機能障害と呼ばれ、回復を遅らせ自立性を低下させる一方で、その生物学的な原因ははっきりしていませんでした。本研究は脳内で起きる連鎖反応を明らかにし、手術によって変化した免疫細胞がどのように脳の化学バランスを乱し、学習や記憶に必要な結合を弱めるかを示しています。
血中を巡る小さな伝達体
研究者らは細胞が血流を介して物質を送るために使う微小な泡、いわゆる細胞外小胞に注目しました。彼らは、術後に認知障害を呈した患者と健康対照者の血液からこれらの小胞を分離しました。影響を受けた患者由来の小胞を高齢マウスに投与すると、動物は脳の炎症、神経伝達物質グルタミン酸の上昇、モリス水迷路などの記憶課題での障害を示しました。詳細な脳の記録では、神経細胞が互いに連絡する接触点であるシナプスが刺激に応じて強化されにくくなっており、これは健全な学習回路の重要な特徴が損なわれていることを示します。 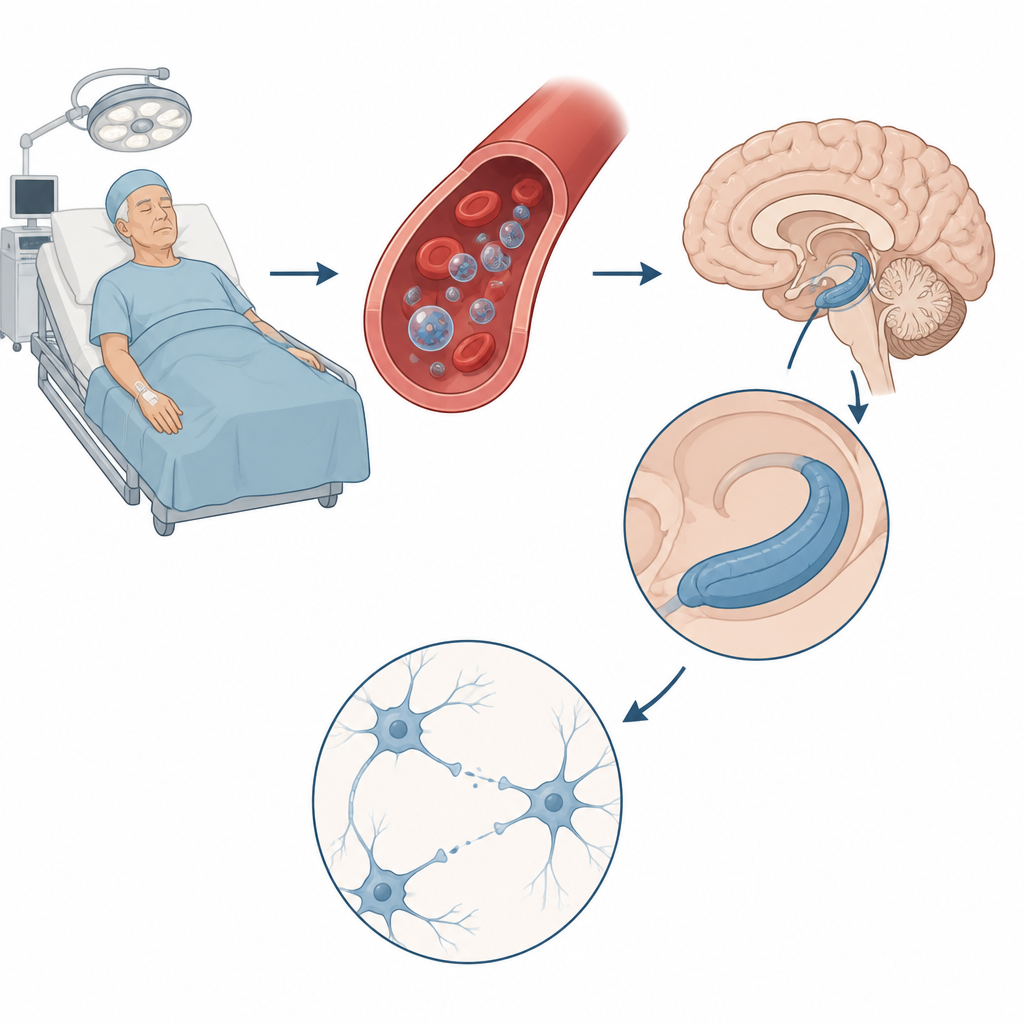
脳の免疫細胞からの有害なメッセージ
詳しく調べると、これらの有害な小胞の主要な供給源は脳固有の免疫細胞であるミクログリアであることが示されました。試験管内でミクログリアを活性化すると、ATPクエン酸リアーゼ(ACLY)という酵素を多く含む小胞を放出しました。これらの小胞は隣接するアストロサイト、つまり脳内の化学バランスを保つ星状の支援細胞に容易に取り込まれました。マウスではミクログリアを薬で抑えると脳の炎症が大幅に減り、グルタミン酸の蓄積が低下し、神経細胞の樹状突起やスパインの構造が保たれ、術後の記憶パフォーマンスが改善しました。これらはミクログリア由来のシグナルが問題の中心であることを示唆します。
支援細胞はどのようにグルタミン酸制御を失うか
アストロサイトは通常、EAAT1と呼ばれるトランスポータータンパク質を介して神経細胞間の余剰グルタミン酸を掃除する役割を持っています。研究チームは、小胞で運ばれる酵素がアストロサイト内でアセチルCoAの産生を高め、これは遺伝子活性を制御するタンパク質に化学的なタグ(アセチル化)を付けるための基質になることを発見しました。その結果、スイッチ役タンパク質であるNF-κB p65の修飾された形が増え、EAAT1遺伝子の上に作用してその発現を抑えます。EAAT1が抑えられるとアストロサイトはグルタミン酸を効率的に除去できなくなり、シナプス付近に興奮性の高いこの化学物質が蓄積して神経細胞とその結合にダメージを与える状況を招きます。
動物モデルからの証拠
高齢マウスで、術後患者由来または活性化ミクログリア由来の小胞を海馬に注入すると、ミクログリアとアストロサイトの活性化、樹状突起スパインの喪失、シナプス伝達の弱化、明らかな記憶障害が生じました。遺伝学的手法でこれらの小胞から酵素を除去したり、小胞の放出や取り込みを阻害したりすると、アストロサイトはEAAT1を取り戻し、グルタミン酸濃度は正常化し、シナプスと行動が改善しました。時間経過実験では、小胞への反復曝露が段階的にシナプス機能と記憶を悪化させることが示され、これは単発のイベントではなく蓄積的な過程であることを強調しています。 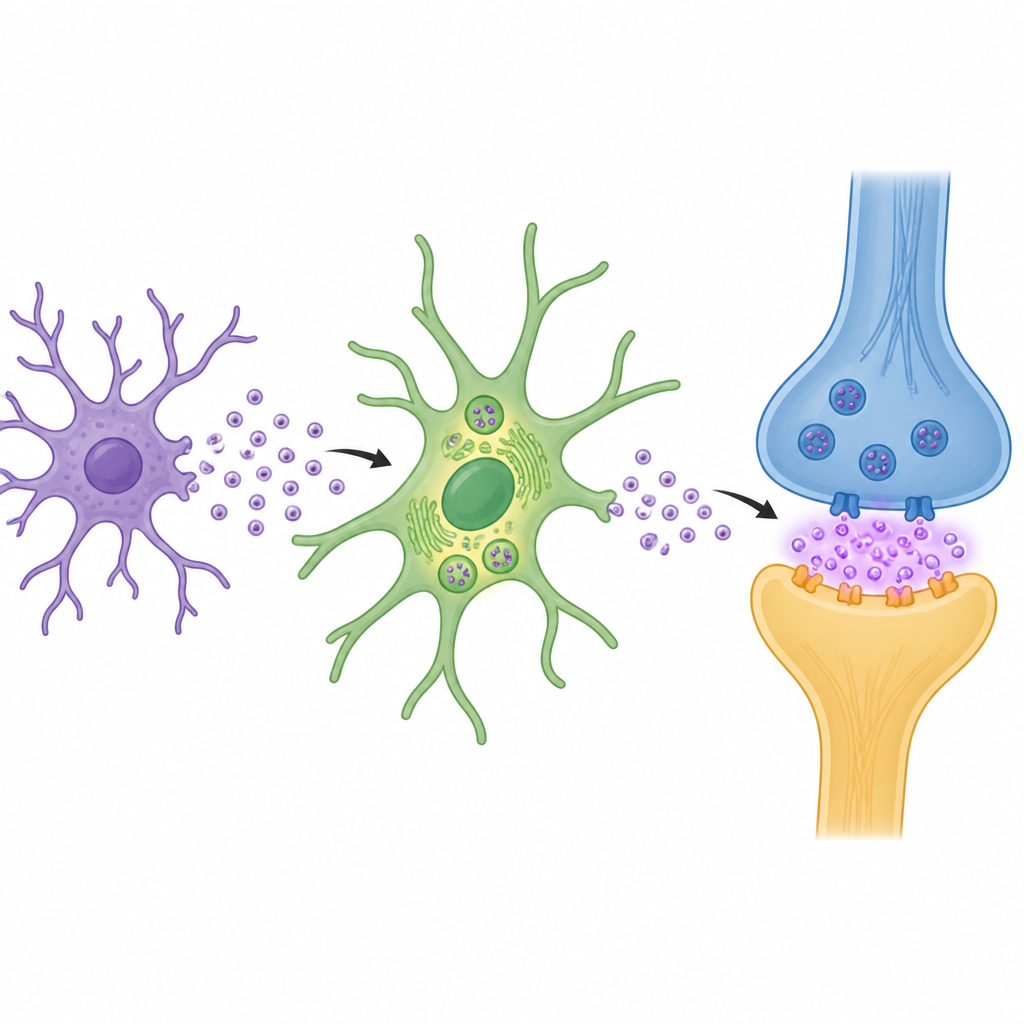
患者への意味
日常的な観点から言えば、本研究は術後に脳の免疫細胞が酵素を詰めた小胞を放出し、周囲の支援細胞を「再プログラム」してグルタミン酸の除去能力を低下させる可能性があることを示唆します。その結果生じる化学的な不均衡が、脆弱な高齢の脳でシナプスと記憶を静かに蝕んでいきます。炎症、グルタミン酸過負荷、認知低下を結ぶ重要な経路としてこの酵素駆動のメカニズムを特定したことで、術前後の重要期間における酵素活性を抑える薬剤や小胞の移動を制限する介入など、新しい治療アイデアへの道が開かれます。
引用: Qi, Z., Ding, L., Zhao, Y. et al. Astrocytic EAAT1 suppression by EV-ACLY underlies glutamate imbalance and cognitive impairment in POCD. Commun Biol 9, 636 (2026). https://doi.org/10.1038/s42003-026-09888-1
キーワード: 術後認知機能障害, ミクログリア, アストロサイト, グルタミン酸不均衡, 細胞外小胞