Clear Sky Science · zh
微胶质细胞丝氨酸消旋酶敲除通过乳酸基化介导的抗炎作用缓解类阿尔茨海默病的神经病理和行为缺陷
大脑清道夫能力获增强
阿尔茨海默病会逐步剥夺患者的记忆与独立能力,现有治疗手段很少能阻止这一过程。本研究探索了一个出人意料的新角度:研究者并非直接针对大脑中粘性的蛋白团块,而是调整大脑自身的免疫细胞——微胶质细胞,使它们更善于清理碎屑并且不易助长有害炎症。通过在这些细胞中关闭一种单一酶,研究显示在小鼠中可缓解类似阿尔茨海默病的脑损伤和记忆问题,提示了一条新的治疗思路。
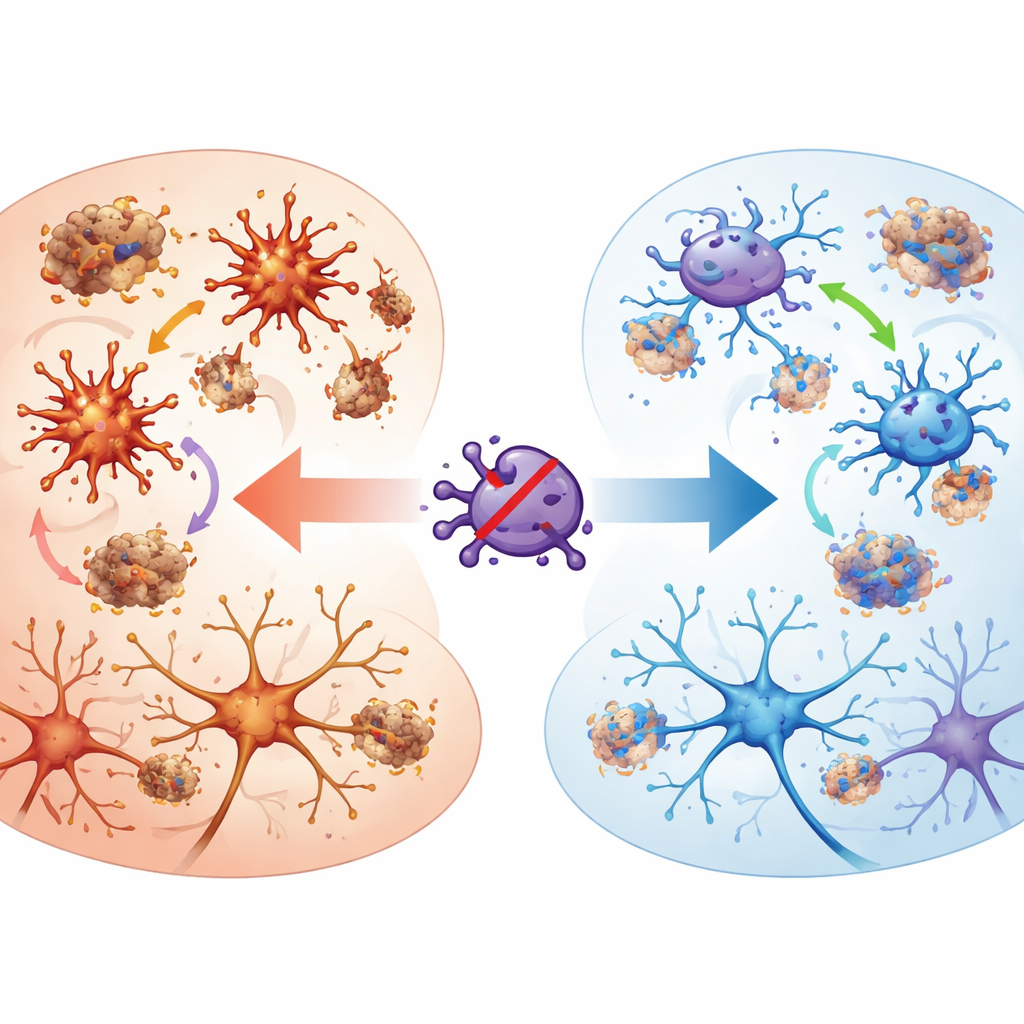
既助益又有害的免疫细胞
微胶质细胞是大脑的常驻清道夫和第一响应者。在阿尔茨海默病早期,它们可以吞噬并清除形成斑块的淀粉样β蛋白。然而随着疾病进展,这些细胞常常改变状态:变得慢性激活,释放炎性分子,并逐渐丧失对斑块的吞噬能力。作者关注了一种名为丝氨酸消旋酶的酶,它参与生成D-丝氨酸——一种与谷氨酸在神经受体上协同作用的化学信使。过多的D-丝氨酸会过度刺激这些受体并损伤神经元,而过少则会削弱正常的神经通信。在老化的大脑中,神经元产生这种酶较少,但包括微胶质在内的胶质细胞倾向于产生更多——这就提出了一个问题:是否通过专门在微胶质细胞中降低该酶的活性,能将它们重新调整为保护性角色?
调低单一酶的水平
为验证这一想法,研究组首先使用体外培养的微胶质细胞。在这些细胞中降低或删除丝氨酸消旋酶基因后,微胶质细胞吞噬更多的淀粉样β颗粒和荧光微球,表明其清理能力增强。相反,强制使微胶质产生额外该酶会使它们吞噬这些靶标的能力变差。研究者随后考察了这些改变的细胞在炎症刺激下的反应。缺乏该酶的微胶质细胞提高了与平息炎症、组织修复相关分子的产生,例如精氨酸酶1和抗炎信号分子IL-10,而经典的促炎标志并未进一步上升。这提示去除该酶将微胶质从有害的慢性战斗状态,引导向更有利于修复和滋养的状态。
重写细胞行为的化学标记
进一步深入研究时,科学家们探索了这种行为转变的控制机制。他们聚焦于“乳酸基化”——一种相对较新的化学修饰,可附加在组蛋白上,组蛋白是包装DNA并帮助调控基因开启的蛋白质。在缺乏丝氨酸消旋酶的微胶质细胞中,炎症刺激导致组蛋白H3特定位点的乳酸基化水平升高,而这一修饰已知可促进像精氨酸酶1这样的基因表达。当团队阻断支持这些乳酸基修饰的酶或代谢步骤时,酶缺失的微胶质细胞中平息型基因的上升就消失了。这指向了一个因果链:细胞代谢与组蛋白修饰的改变重新编程免疫细胞,使其变得不那么炎性、并更善于清除斑块。
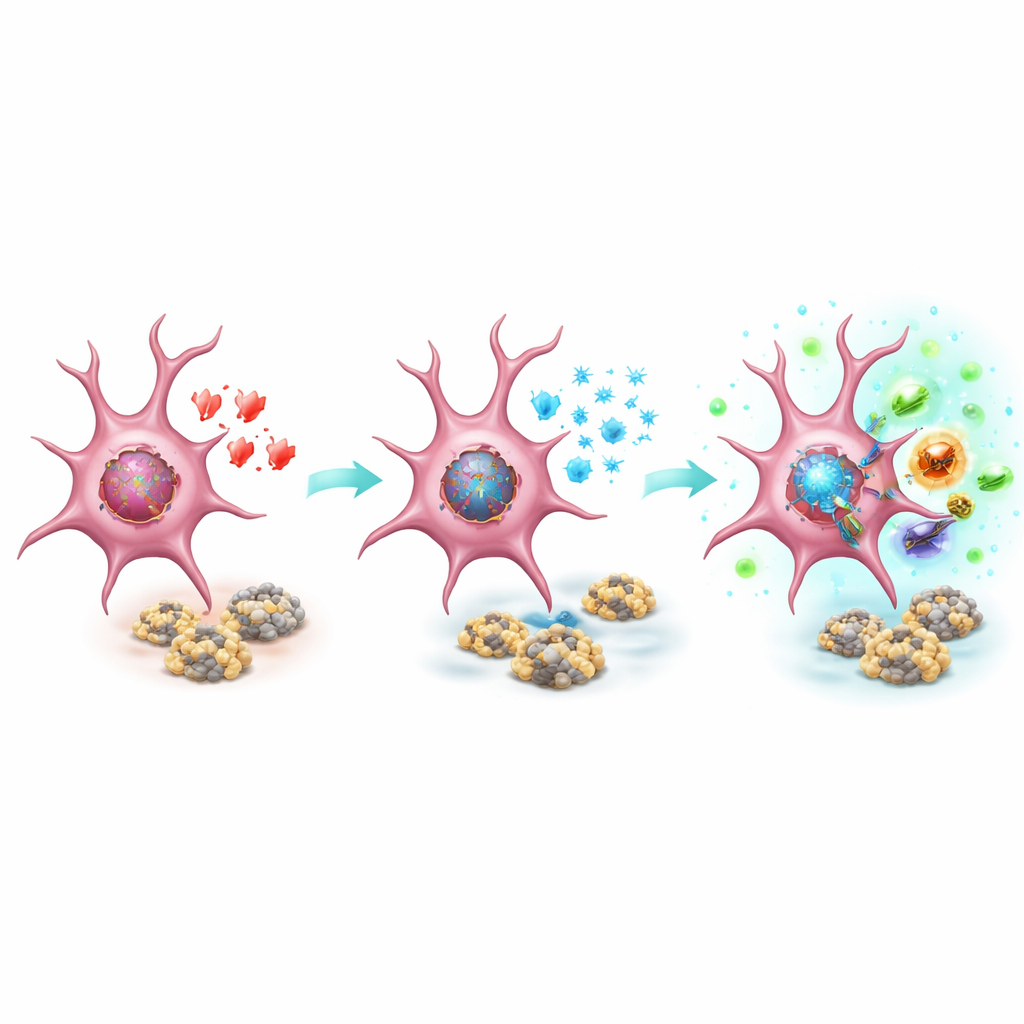
在类阿尔茨海默大脑中助益记忆
关键的检验是这种微胶质重编程能否在活体大脑中真正改善疾病特征。研究者将易患阿尔茨海默的5×FAD小鼠——一种会快速出现淀粉样斑块和记忆缺陷的成熟模型——与仅在微胶质细胞中丧失丝氨酸消旋酶的小鼠交配。在这些动物中,斑块周围的微胶质细胞显示出更多有益的组蛋白乳酸基化标记、更高水平的精氨酸酶1以及与更高效能量利用相关的代谢酶增加。携带微胶质酶缺失的雄性小鼠在关键记忆区域的淀粉样斑块更少,而雄雌两性在空间学习和记忆任务中都表现出某些改善,尽管具体改善因性别而异。这些性别差异可能反映出雄性与雌性在大脑中处理D-丝氨酸及相关酶时的不同方式。
这对未来治疗可能意味着什么
简而言之,这项研究表明在大脑免疫细胞中关闭一种单一酶,能使它们更善于吞噬有害的蛋白团块并减少促成破坏性炎症的倾向,进而缓解类阿尔茨海默的改变并改善小鼠的记忆。通过将这些益处与细胞代谢和DNA包装蛋白上的化学标记变化联系起来,该工作凸显了以精确方式重编程微胶质而非完全抑制它们的可行杠杆。尽管要把这转化为人体治疗还需大量工作,微胶质丝氨酸消旋酶现在已成为一个有前景的药物靶点,可用于帮助大脑自我清洁并维持更长时间的健康。
引用: Zhou, J., Yang, Y., Liu, S. et al. Microglial serine racemase knockout alleviates Alzheimer-like neuropathology and behavioral deficit via lactylation-mediated anti-inflammation. Commun Biol 9, 493 (2026). https://doi.org/10.1038/s42003-026-09772-y
关键词: 微胶质细胞, 阿尔茨海默病, D-丝氨酸, 神经炎症, 表观遗传调控