Clear Sky Science · zh
SOX9抑制SW1353细胞中人类半乳凝素-3启动子:对骨关节炎的潜在影响
这对酸痛关节为何重要
骨关节炎是最常见的关节炎类型,会逐步磨损关节中的缓冲软骨,使数百万人长期忍受疼痛。半乳凝素-3是一种逐渐被认定为关键的捣蛋蛋白,它会激发炎症并加速软骨降解。本研究提出了一个看似简单但重要的问题:细胞内什么机制使半乳凝素-3基因被打开或关闭?通过揭示一种称为SOX9的软骨“身份”因子如何抑制半乳凝素-3,这项工作描绘了骨关节炎更深层的调控图谱,并提示了从源头缓解疾病的新方向。 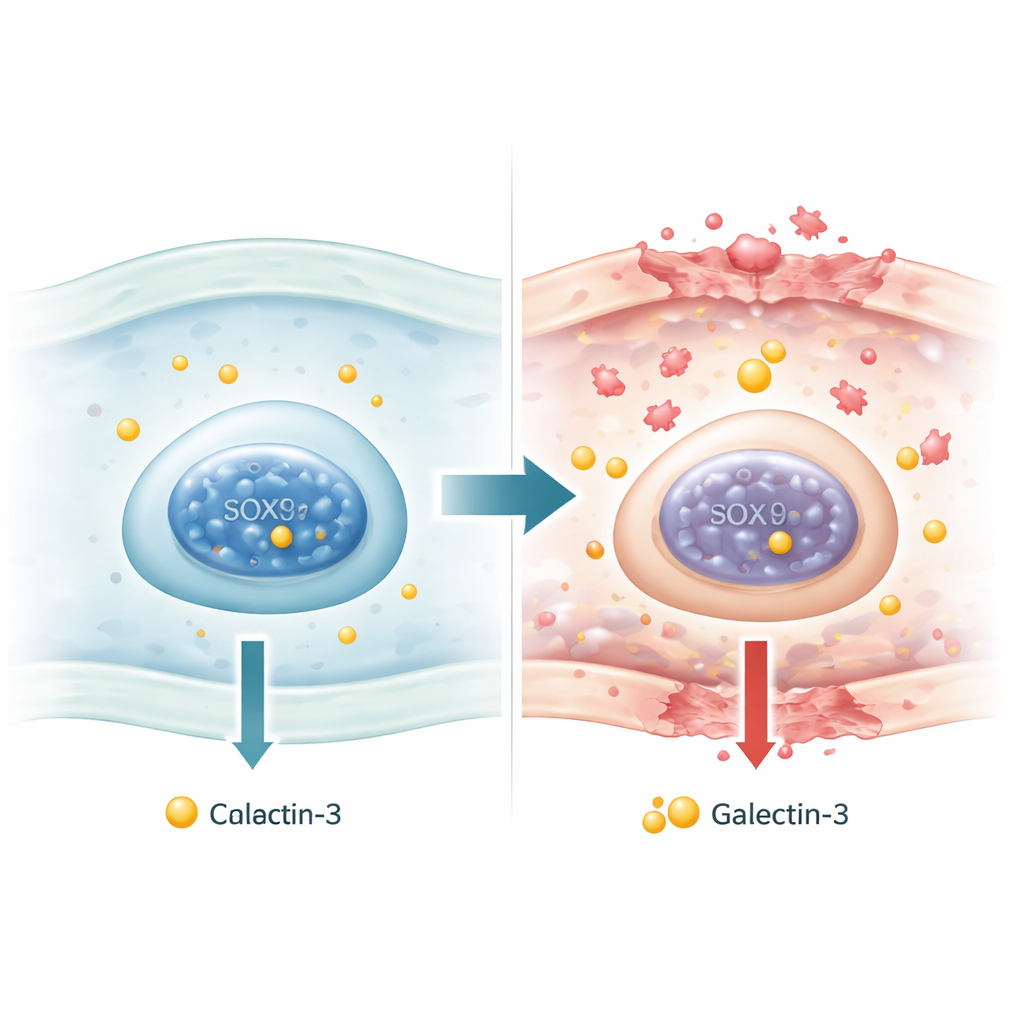
损耗软骨中的捣蛋蛋白
半乳凝素-3是一种结合糖类的蛋白,存在于多种组织和物种中。在患有骨关节炎和早期类风湿关节炎的患者中,其在血液和关节软骨中的含量常常升高。在受损的膝关节软骨中,产生更多半乳凝素-3的细胞往往位于组织破坏最严重的区域。实验显示,细胞外的半乳凝素-3可以附着于软骨细胞,触发炎症信号,并激活分解周围基质的酶。然而,尽管其在病理中发挥中心作用,为什么半乳凝素-3基因(称为LGALS3)在病变软骨中变得过度活跃,仍不清楚。
软骨的身份守护者介入
软骨细胞(软骨细胞)由一类被称为SOX因子的DNA结合蛋白调控。在这些因子中,SOX9常被描述为主调控因子:它帮助软骨细胞合成并维持赋予软骨弹性的胶原和凝胶状分子。在健康软骨中,SOX9与其搭档SOX5和SOX6协同维持这一程序。然而在骨关节炎中,这一网络失衡:SOX5和SOX6,尤其是SOX9减少,而另一个家族成员SOX4增加。由于SOX蛋白能够弯曲DNA并重塑基因的局部环境,作者推测SOX活性变化可能直接改变软骨细胞表达半乳凝素-3基因的强度。
聚焦基因的开关
为检验这一想法,研究人员使用了一种称为SW1353的人类软骨样细胞系,构建了一系列覆盖LGALS3基因上游区域(即转录机器结合位点)的DNA片段。他们将这些片段与荧光素酶报告基因融合,荧光素酶的发光强度与启动子活性成比例。通过从远端上游向基因方向逐步截短片段,他们发现一段仅约149个碱基对、围绕起始位点(从−97到+52)的短序列就足以驱动强烈活性。在该区域内进一步去除较小片段会导致信号逐步下降,表明关键控制元件集中在这一紧凑片段中,并富含吸引其他转录因子的GC富集基序。
SOX9如何踩下半乳凝素-3的刹车
接着,团队评估了不同SOX蛋白对该启动子的影响。当人为增加SOX2或SOX9时,LGALS3启动子活性呈剂量依赖性显著下降,而SOX4、SOX5和SOX6未表现出一致影响。进一步测试表明SOX2表现为非特异性作用,与软骨生物学关系不大,而SOX9则表现出针对性的调控。当存在全长启动子时,SOX9对活性的抑制最为显著,但即使在最小的−97/+52片段中,抑制效应仍然明显。利用染色质拉下方法,作者证明SOX9能物理结合在LGALS3启动子的−93/+49区域内。将该片段中预测的SOX9识别位点进行突变会降低启动子的基线活性,并略微削弱SOX9的抑制作用,表明该位点重要但不是唯一贡献者。重要的是,当在细胞中过表达SOX9时,内源性LGALS3信使RNA水平下降约30%,证实这种调控作用作用于天然基因,而不仅仅是人工报告子。 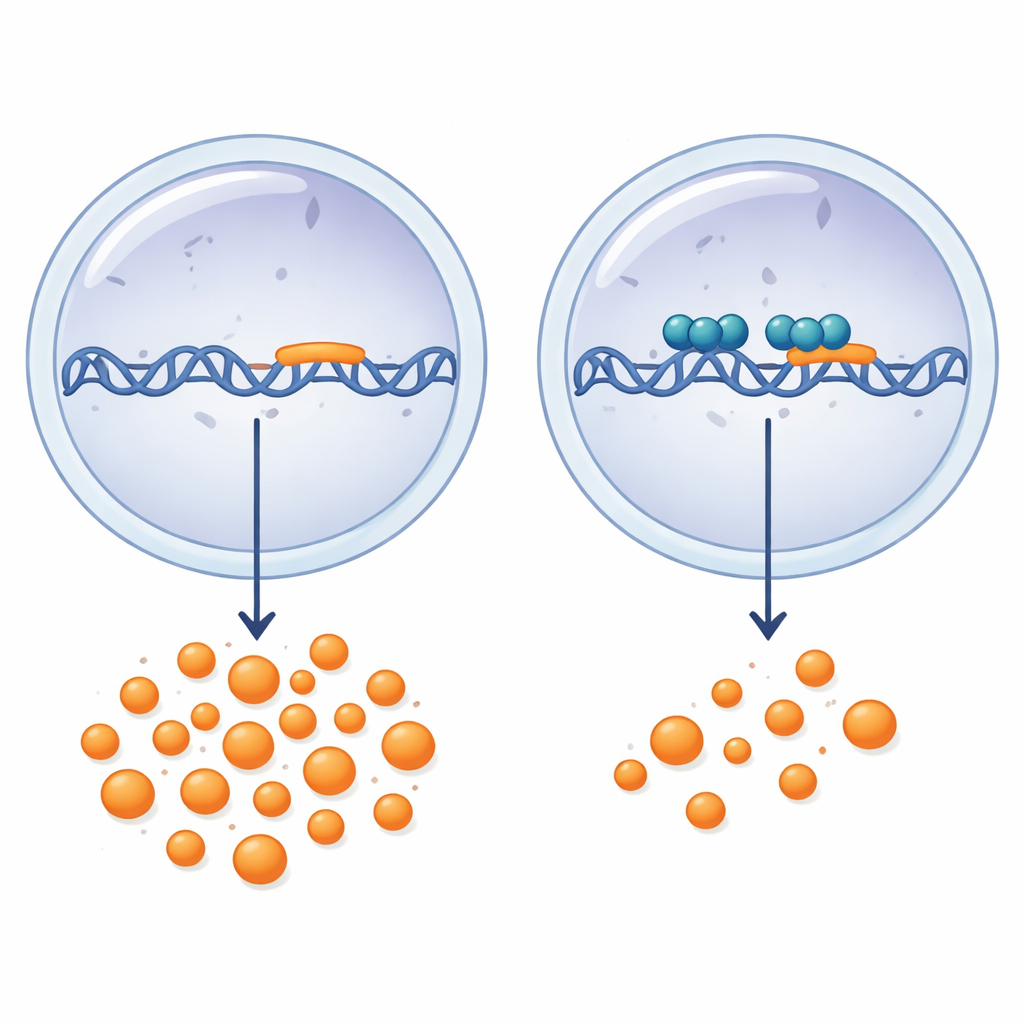
对理解与治疗骨关节炎的意义
综合来看,研究鉴定出控制人类半乳凝素-3基因的一个紧凑核心启动子,并确认SOX9在软骨样细胞中作为该开关的直接抑制因子。在骨关节炎中,SOX9水平通常降低,刹车的丧失可能有助于解释为何半乳凝素-3过度积累并推动炎症与基质降解。尽管本研究在来源于癌症的细胞系中进行,仍需在原代软骨细胞和动物模型中验证,但它描绘了软骨身份因子与有害炎症介质之间的关键联系。从长远来看,恢复或模拟SOX9对LGALS3的抑制作用的策略——无论通过基因调控、表观遗传药物还是基于RNA的疗法——可能有助于降低半乳凝素-3水平并减缓导致骨关节炎疼痛的关节损伤。
引用: Alba, B., Buddiga, S., Kaltner, H. et al. SOX9 represses the human galectin-3 promoter in SW1353 cells: potential implications for osteoarthritis. Sci Rep 16, 14284 (2026). https://doi.org/10.1038/s41598-026-50507-0
关键词: 骨关节炎, 半乳凝素-3, SOX9, 软骨, 基因调控