Clear Sky Science · de
SOX9 unterdrückt den humanen Galectin‑3-Promotor in SW1353‑Zellen: mögliche Folgen für Osteoarthritis
Warum das für schmerzende Gelenke wichtig ist
Osteoarthritis, die häufigste Form von Arthritis, nutzt den dämpfenden Knorpel in unseren Gelenken langsam ab und verursacht bei Millionen von Menschen tägliche Schmerzen. Ein Protein, Galectin‑3, hat sich als zentraler Störer herauskristallisiert, das Entzündungen anheizt und den Knorpelabbau beschleunigt. Diese Studie stellt eine auf den ersten Blick einfache Frage: Was in unseren Zellen schaltet das Galectin‑3‑Gen hoch oder runter? Indem sie zeigt, wie ein Knorpel‑„Identitätsfaktor“ namens SOX9 Galectin‑3 bremst, liefert die Arbeit Einblicke in die zugrunde liegende Schaltlogik der Osteoarthritis und deutet auf neue Wege hin, die Krankheit an ihrer Quelle zu dämpfen. 
Ein störendes Protein in verschlissenem Knorpel
Galectin‑3 ist ein zuckerbindendes Protein, das in vielen Geweben und Spezies vorkommt. Bei Menschen mit Osteoarthritis und in frühen Stadien der rheumatoiden Arthritis sind seine Werte im Blut und im Gelenkknorpel häufig erhöht. In geschädigtem Knieknorpel finden sich Zellen mit höherer Galectin‑3‑Produktion oft in den Bereichen mit der stärksten Gewebezerstörung. Experimente haben gezeigt, dass extrazelluläres Galectin‑3 an Knorpelzellen binden, Entzündungssignale auslösen und Enzyme aktivieren kann, die die umgebende Matrix abbauen. Trotzdem war lange unklar, warum das Galectin‑3‑Gen (LGALS3 genannt) in erkranktem Knorpel überhaupt überaktiv wird.
Der Hüter der Knorpelidentität tritt auf den Plan
Knorpelzellen, die Chondrozyten, werden von einer Familie DNA‑bindender Proteine namens SOX‑Faktoren gesteuert. Unter ihnen wird SOX9 oft als Masterregulator beschrieben: Er hilft Chondrozyten dabei, Kollagen und gelartige Moleküle herzustellen und zu erhalten, die dem Knorpel seine Federung verleihen. In gesundem Knorpel arbeitet SOX9 zusammen mit seinen Partnern SOX5 und SOX6, um dieses Programm aufrechtzuerhalten. Bei Osteoarthritis gerät dieses Netzwerk jedoch aus dem Gleichgewicht: SOX5 und SOX6 und besonders SOX9 sind vermindert, während ein anderes Familienmitglied, SOX4, zunimmt. Da SOX‑Proteine DNA verformen und die lokale Genlandschaft umgestalten können, vermuteten die Autoren, dass Veränderungen in der SOX‑Aktivität direkt beeinflussen könnten, wie stark Chondrozyten das Galectin‑3‑Gen exprimieren.
Auf Spurensuche am Ein/Aus‑Schalter des Gens
Um diese Idee zu testen, verwendeten die Forschenden eine humane, chondrozytenähnliche Zelllinie namens SW1353 und konstruierten eine Reihe von DNA‑Fragmenten, die den Bereich vor dem LGALS3‑Gen abdecken, wo die Transkriptionsmaschinerie andockt. Sie fusionierten diese Fragmente mit einem Luciferase‑Reporter, einem lichtproduzierenden Gen, das proportional zur Promotoraktivität leuchtet. Durch sukzessives Kürzen der weiter upstream gelegenen Regionen in Richtung Gen entdeckten sie, dass ein kurzer DNA‑Abschnitt von nur 149 Basenpaaren rund um den Startpunkt (von −97 bis +52) bereits starke Aktivität trieb. Das Entfernen kleinerer Bereiche innerhalb dieses Abschnitts führte zu stufenweisen Signalabfällen und zeigte, dass wichtige Kontroll‑Elemente, reich an GC‑haltigen Motiven, die andere Transkriptionsfaktoren anziehen, in diesem kompakten Segment liegen.
Wie SOX9 die Bremse auf Galectin‑3 betätigt
Als Nächstes untersuchte das Team, wie unterschiedliche SOX‑Proteine diesen Promotor beeinflussen. Bei künstlicher Erhöhung von SOX2 oder SOX9 fiel die LGALS3‑Promotoraktivität dosisabhängig stark ab, während SOX4, SOX5 und SOX6 keinen konsistenten Effekt zeigten. Weitere Tests deuteten darauf hin, dass SOX2 unspezifisch wirkt und für die Knorpelbiologie nicht relevant ist, während SOX9 gezielte Kontrolle ausübt. SOX9 verringerte die Aktivität am stärksten bei Vorhandensein des vollständigen Promotors, doch die Repression blieb auch im minimalen −97/+52‑Fragment deutlich. Mit einer Chromatin‑Pull‑Down‑Methode zeigten die Autoren, dass SOX9 physisch innerhalb einer −93/+49‑Region des LGALS3‑Promotors bindet. Die Mutation eines vorhergesagten SOX9‑Erkennungsmotivs in diesem Segment senkte die Basisaktivität des Promotors und schwächte SOX9s repressiven Effekt leicht ab, was darauf hinweist, dass diese Stelle wichtig, aber nicht der einzige Beitragende ist. Wichtig ist: Bei Überexpression von SOX9 in den Zellen sanken die endogenen LGALS3‑mRNA‑Niveaus um etwa 30 %, was bestätigt, dass diese Verschaltung am natürlichen Gen und nicht nur an einem künstlichen Reporter wirkt. 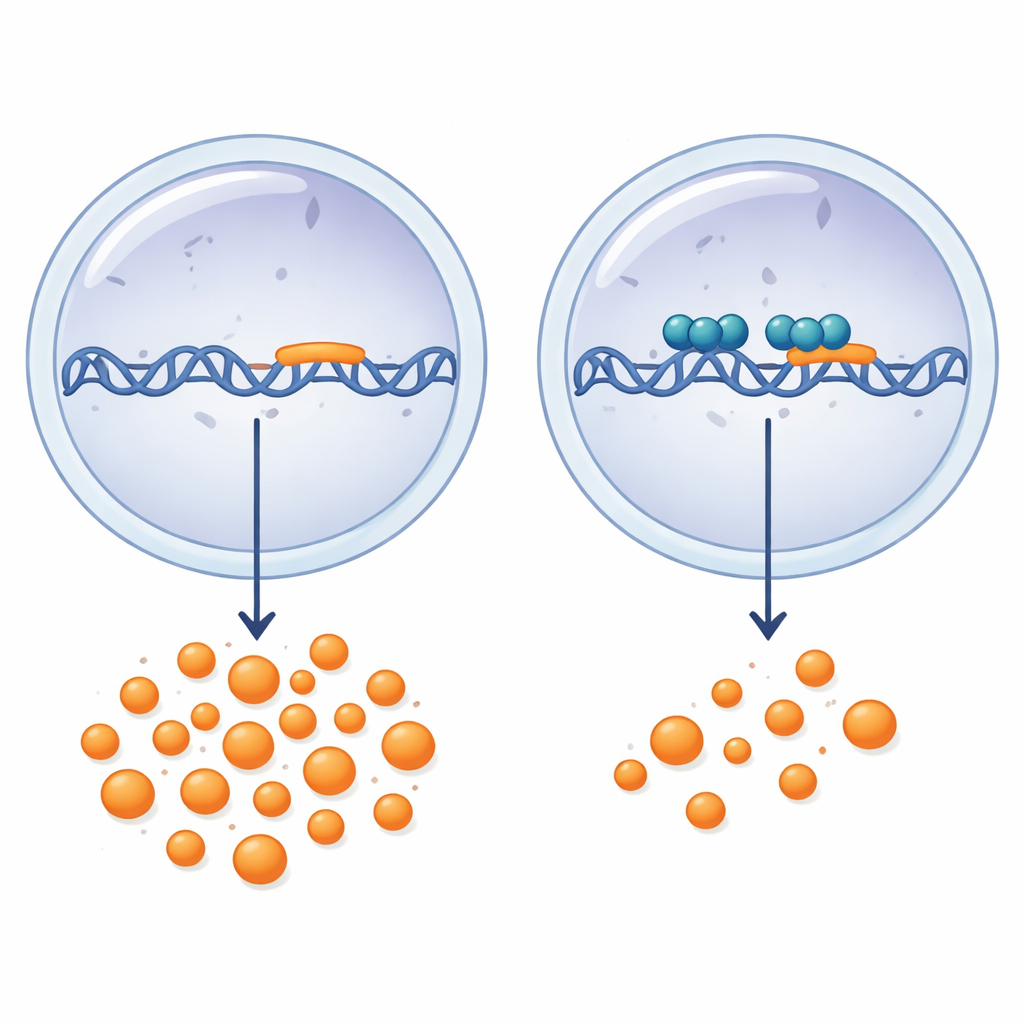
Was das für das Verständnis und die Behandlung von Osteoarthritis bedeutet
Zusammengefasst zeigen die Befunde einen kompakten Kernpromotor, der das humane Galectin‑3‑Gen steuert, und identifizieren SOX9 als direkten Bremser dieses Schalters in knorpelähnlichen Zellen. Bei Osteoarthritis, wo SOX9‑Spiegel typischerweise reduziert sind, könnte der Verlust dieser Bremse erklären, warum Galectin‑3 übermäßig ansteigt und Entzündung sowie Matrixabbau vorantreibt. Obwohl diese Studie in einer krebsabgeleiteten Zelllinie durchgeführt wurde und noch in primären Knorpelzellen sowie Tiermodellen bestätigt werden muss, stellt sie eine wichtige Verbindung zwischen einem Knorpel‑Identitätsfaktor und einem schädlichen entzündlichen Mediator her. Langfristig könnten Strategien, die SOX9s hemmenden Einfluss auf LGALS3 wiederherstellen oder nachahmen — etwa durch Genregulation, epigenetische Medikamente oder RNA‑basierte Therapien — dazu beitragen, Galectin‑3‑Spiegel zu senken und den Gelenk‑Schaden zu verlangsamen, der den Schmerzen der Osteoarthritis zugrunde liegt.
Zitation: Alba, B., Buddiga, S., Kaltner, H. et al. SOX9 represses the human galectin-3 promoter in SW1353 cells: potential implications for osteoarthritis. Sci Rep 16, 14284 (2026). https://doi.org/10.1038/s41598-026-50507-0
Schlüsselwörter: Osteoarthritis, Galectin‑3, SOX9, Knorpel, Genregulation