Clear Sky Science · zh
抑制 CDK9 使多药耐药的卵巢癌细胞对紫杉醇重新敏感
这项研究为何关系到女性健康
卵巢癌是危及女性生命的最致命癌症之一,主要因为常常在晚期被发现,且许多肿瘤最终对化疗失去反应。本研究探索了一种让顽固的、耐药的卵巢癌细胞重新对主力化疗药物紫杉醇敏感的新方法。研究者聚焦于称为 CDK9 的细胞“开关”,它有助于癌细胞存活,提出了一种策略,或许将来能延长现有治疗的有效期并降低复发。
不听话的癌细胞问题
大多数卵巢癌患者最初对紫杉醇与铂类药物的联合治疗有反应,但许多人之后面临令人心碎的疾病复发。随着时间推移,肿瘤细胞可能发展出多药耐药,意味着它们不仅对紫杉醇无效,还能抵抗多种化疗药物。这种耐药通过多种把戏产生,包括将药物泵出细胞和启动强大的存活程序。作者将注意力放在 CDK9——一种控制基因读取并转化为存活分子的蛋白上。他们早期的工作表明,CDK9 水平高的卵巢肿瘤更具侵袭性且更易复发,因此提出阻断 CDK9 是否能解除耐药这一问题。
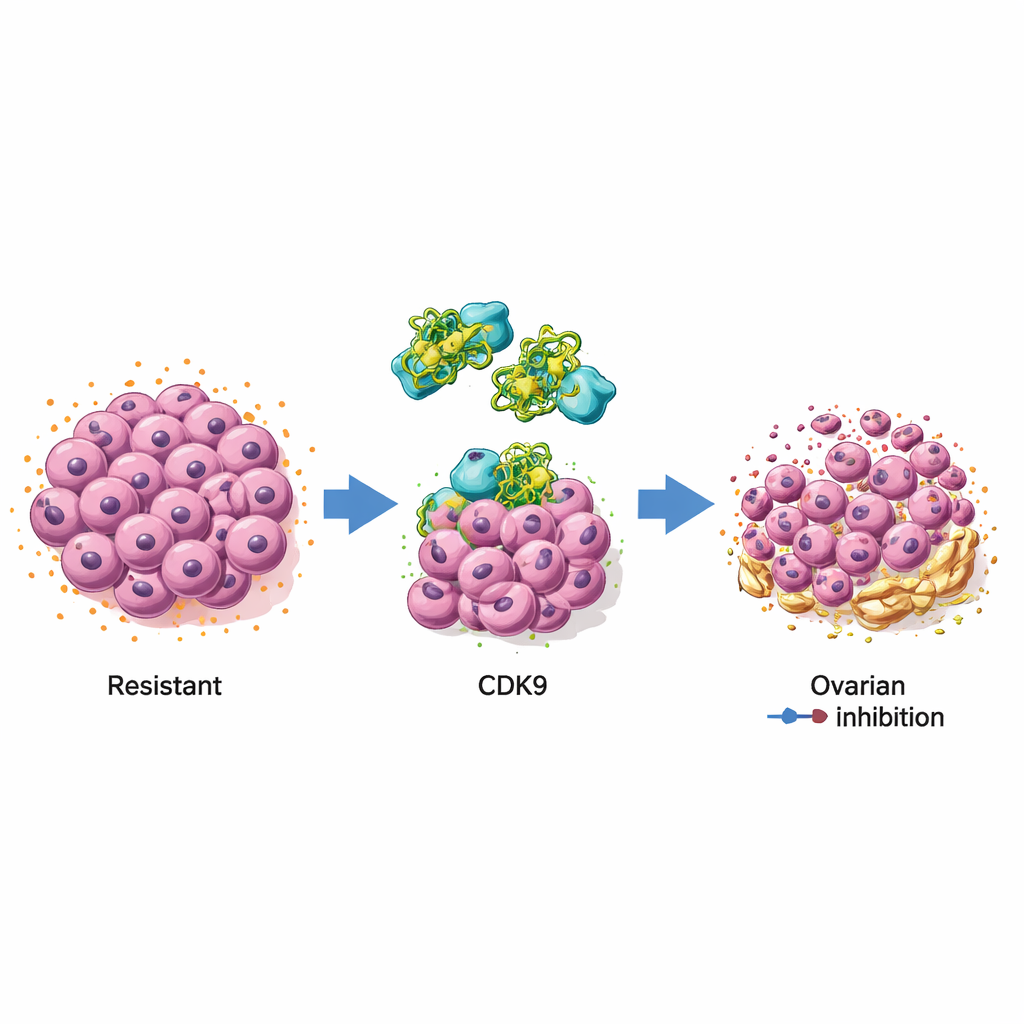
癌细胞内的关键控制旋钮
为探究 CDK9 的作用,团队比较了两株标准卵巢癌细胞系与经长期选择获得高紫杉醇耐药性的对应细胞。耐药细胞能在更高的药物浓度下存活,而这些浓度会杀死更敏感的细胞。蛋白水平检测显示,耐药细胞持续表现出更高的 CDK9 含量,以及与基因转录相关的分子(RNA 聚合酶 II)和信号蛋白 Stat3 更强的活性,这些因子都助长生长和存活。该模式提示耐药细胞特别依赖由 CDK9 驱动的转录程序来应对化疗压力。
降低 CDK9 活性以重新唤醒药物反应
随后科学家测试了降低 CDK9 活性会如何影响细胞。通过基因沉默工具(siRNA)敲低 CDK9 或用选择性 CDK9 抑制剂 LDC067 处理细胞,他们观察到被激活形式的 RNA 聚合酶 II 和 Stat3 明显下降。与此同时,促存活分子如 Mcl‑1 水平下降,而促凋亡信号如 Bax 及剪切的 PARP 增加——这些都是细胞程序性自毁(凋亡)的明确标志。重要的是,一旦 CDK9 被抑制,先前耐药的细胞对紫杉醇的敏感性显著提高。当紫杉醇与 CDK9 抑制剂联合使用时,组合治疗比任何单一处理杀死更多癌细胞,在多个剂量下显示出强烈的协同效应。
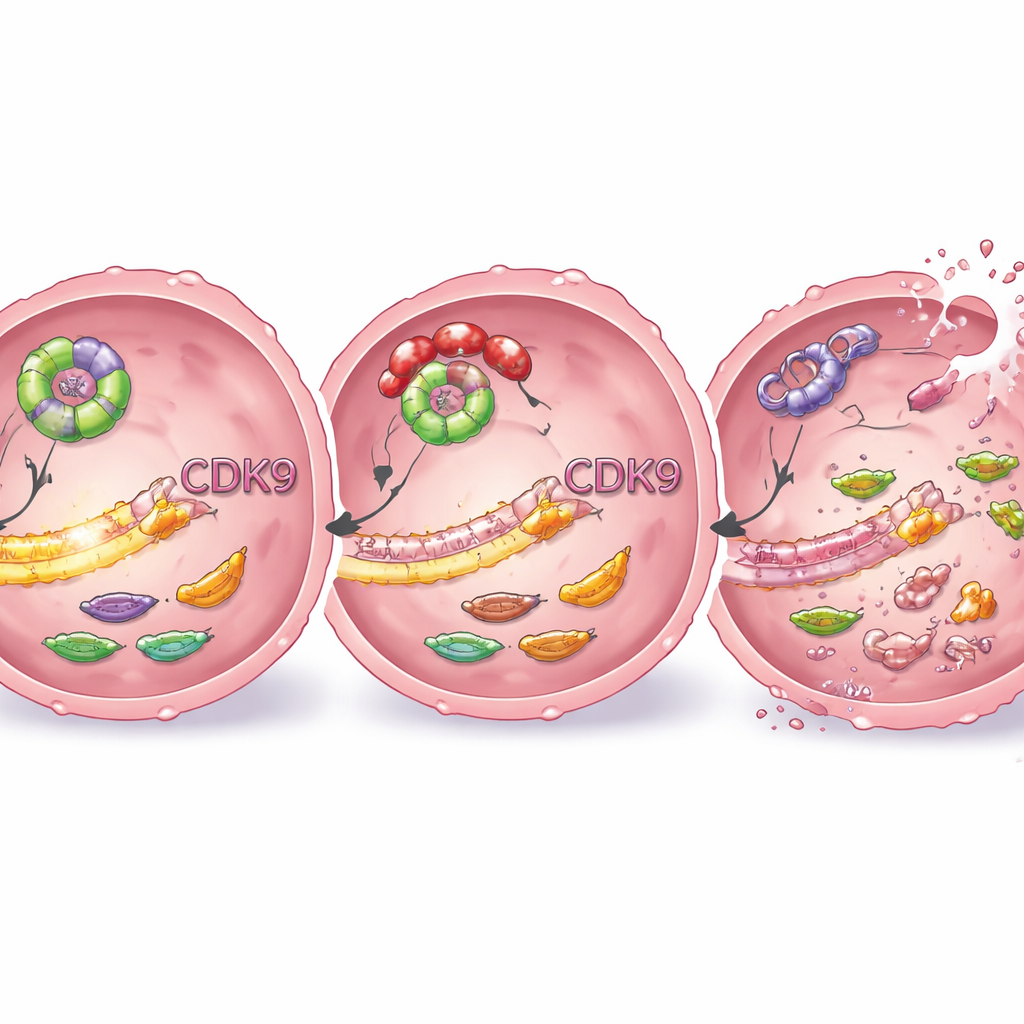
减缓生长、扩散和类肿瘤三维团块
除了单纯杀死个体细胞外,研究者还探究了阻断 CDK9 是否削弱与体内真实肿瘤相关的行为。在模拟癌细胞形成致密球状体的三维培养中,耐药细胞系通常形成大型且不断生长的团块。在 CDK9 抑制下,这些球体在两周内保持明显更小,长期集落形成能力显著下降。在伤口愈合实验中(在细胞单层上划出缝隙),被 CDK9 抑制的细胞迁移速度明显慢于未处理细胞,暗示 CDK9 也支持促进转移和复发的运动能力。
这对未来治疗的可能意义
综合来看,研究结果将 CDK9 描绘为耐药卵巢癌细胞用以持续分裂、避免死亡和移动的核心帮手。通过关闭 CDK9——无论是用针对性的基因工具还是小分子抑制剂——研究者能够恢复对紫杉醇的敏感性、诱导细胞自杀,并抑制耐药细胞的增殖与迁移。尽管这些结果来自实验室模型而非患者,但表明将 CDK9 靶向药物加入标准化疗,有望在未来帮助克服耐药并改善复发性卵巢癌患者的结局。
引用: Wang, J., Hornicek, F.J., Shi, H. et al. Inhibition of CDK9 sensitizes multidrug resistant ovarian cancer cells to paclitaxel. Sci Rep 16, 11671 (2026). https://doi.org/10.1038/s41598-026-47843-6
关键词: 卵巢癌, 药物耐药, CDK9, 紫杉醇, 靶向治疗