Clear Sky Science · zh
基因表达与机器学习技术揭示与近视进展中氧化应激相关的角膜生物标志物
这对日常视力有何意义
近视正在全球迅速增加,尤其是在长时间进行近距离任务和使用屏幕的年轻人中。大部分研究集中在眼球后部,但本研究将目光投向眼睛前面的透明窗——角膜。通过探查与氧化应激相关的角膜基因和免疫活动的细微变化,作者提出角膜是否可能在无声中助推近视进程,以及它是否有朝一日能指引新的检测或治疗方法。
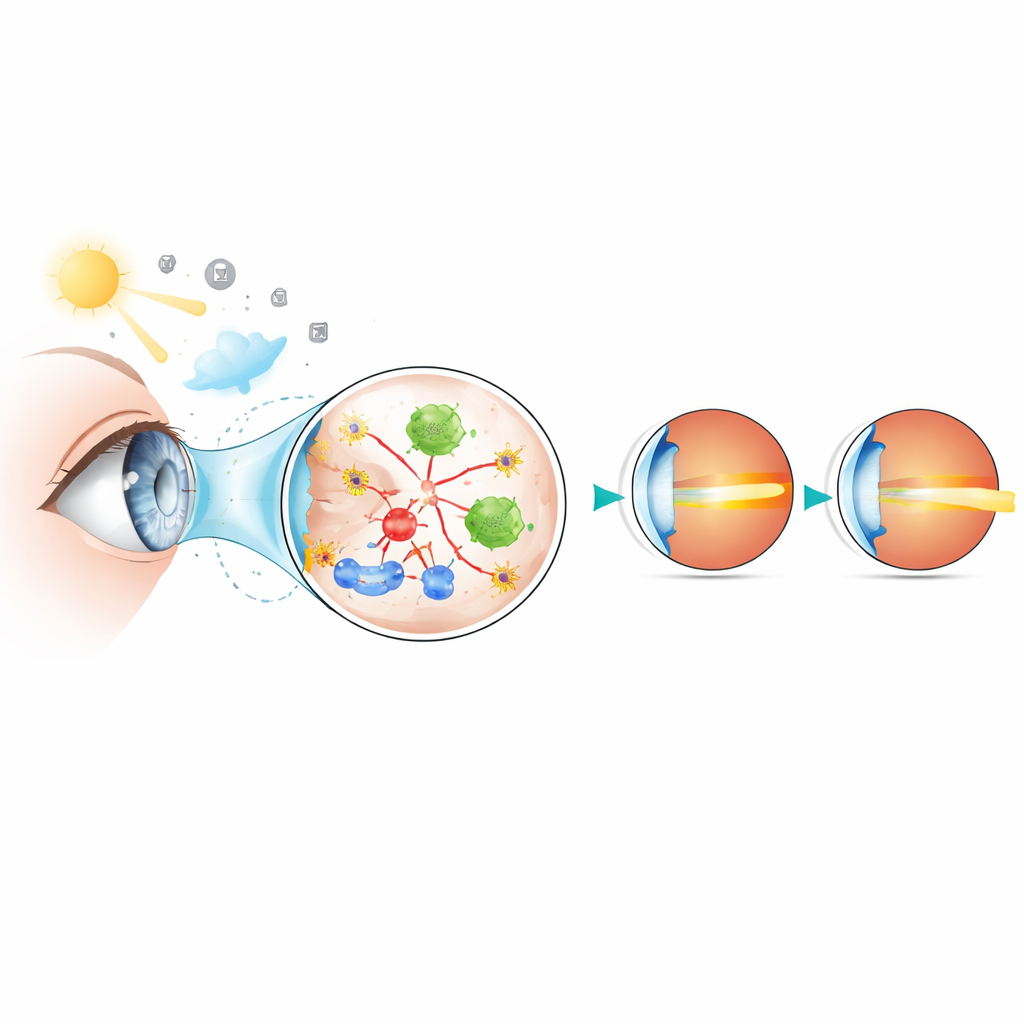
承受压力的眼前窗
角膜提供约三分之二的眼睛屈光力,因此即便是其透明度或形状的细微变化也能影响视力。研究者关注的是氧化应激,一种有害氧副产物超过机体防御能力的生化失衡。先前研究表明近视眼的眼液和视网膜中存在氧化应激,但角膜很少受到重视。鉴于角膜在常规眼科手术和治疗中易于获得,研究团队认为角膜既可能是有害应激的传感器,也可能是实用的生物标志物来源——即可测量的疾病分子信号。
挖掘大数据以发现分子指纹
为寻找此类指纹,科学家将若干公开可得的角膜组织和晶状体细胞的基因表达数据集进行了整合,比较有无近视者。首先他们识别出数千个在近视样本与非近视样本中表达差异的基因,再将该列表缩小到已知与氧化应激相关的小范围基因。利用现代机器学习技术,包括LASSO回归和Boruta特征选择算法,他们锁定了三个关键基因——ATF3、GRIN2B和GSTM3,这些基因在区分近视组织与正常组织时表现稳定。
角膜中的三盏警示灯
ATF3帮助细胞应对应激信号,GRIN2B是通常在大脑中研究的一种信号通道成分,GSTM3通过抗氧化剂谷胱甘肽帮助解毒活性分子。在合并的数据集和独立验证集里,这三种标志物在近视样本中表达均较低。团队随后检查了在SMILE激光手术中取下的真实人类角膜组织,样本来自有低度和高度近视的年轻成人。发现ATF3和GSTM3信使RNA在高度近视角膜中显著降低,蛋白质测量也证实三者均减少。有趣的是,一种称为孟德尔随机化的统计技术并不支持这些基因作为近视的直接遗传因子,这暗示近视或其相关环境可能抑制了它们的活性。
免疫变化与受压细胞通路
超越单个基因,作者还研究了免疫细胞和更广泛的细胞通路在两组间的差异。他们估算了角膜样本中22种免疫细胞类型的构成,发现在近视个体中存在显著变化,包括CD8+ T细胞和单核细胞增多,以及嗜酸性粒细胞和静息记忆CD4+ T细胞减少。三种生物标志物与CD8+ T细胞呈显著负相关,与嗜酸性粒细胞呈正相关,表明抗氧化防御能力下降与更具炎症性的免疫景观相伴而生。额外的通路分析将这些标志物与细胞间连接、缺氧反应及紫外线损伤等机制关联起来。总体而言,这些发现支持这样一种图景:角膜微环境中的慢性应激同时重塑了细胞信号传导和免疫活动。
未来治疗的线索与当前的局限
为探索治疗方向,研究者使用药物—基因数据库和基于计算的分子对接来预测可能与三种生物标志物相互作用的化合物。视黄酸(一种维生素A的活性形式,对角膜健康重要)作为一个共同候选物浮现出来,理论上可能影响这三者。然而,这些预测纯属计算推断,需经过严谨的实验室与临床验证。作者还强调他们的研究依赖于相对较小的样本量和混合的组织来源,许多推断的机制仍需实验证实。
这对近视患者意味着什么
总体来看,该研究提示眼睛前部并非仅为被动的透镜,而是在近视发展中发挥积极作用,氧化应激相关基因与免疫细胞的变化与疾病严重程度相一致。ATF3、GRIN2B和GSTM3作为有前途的生物标志物,未来可能帮助医生利用易于获得的角膜组织评估近视风险或监测进展。尽管尚不足以改变临床实践,但这项工作为未来旨在保护角膜抗氧化防御并抑制有害免疫反应以减缓或预防近视加重的策略奠定了分子基础。
引用: Zhou, Q., Ye, M., Zhang, Z. et al. Gene expression and machine learning techniques uncover corneal biomarkers associated with oxidative stress in the myopia progression. Sci Rep 16, 10651 (2026). https://doi.org/10.1038/s41598-026-46896-x
关键词: 近视, 角膜, 氧化应激, 生物标志物, 眼部免疫