Clear Sky Science · pl
Ekspresja genów i techniki uczenia maszynowego ujawniają biomarkery rogówki związane ze stresem oksydacyjnym w progresji krótkowzroczności
Dlaczego to ma znaczenie dla codziennego widzenia
Krótkowzroczność, czyli trudność w widzeniu przedmiotów oddalonych, szybko rośnie na całym świecie, zwłaszcza wśród młodych osób spędzających wiele godzin na czynnościach wykonywanych z bliska i przed ekranami. Większość badań koncentrowała się na tylnej części oka, ale w tym badaniu uwaga skierowana została ku przezroczystemu przedniemu oknu oka — rogówce. Poprzez badanie drobnych zmian w genach rogówki i aktywności układu odpornościowego związanych ze stresem oksydacyjnym, autorzy pytają, czy ta tkanka może potajemnie przyczyniać się do krótkowzroczności i czy w przyszłości mogłaby wskazywać nowe testy lub terapie.
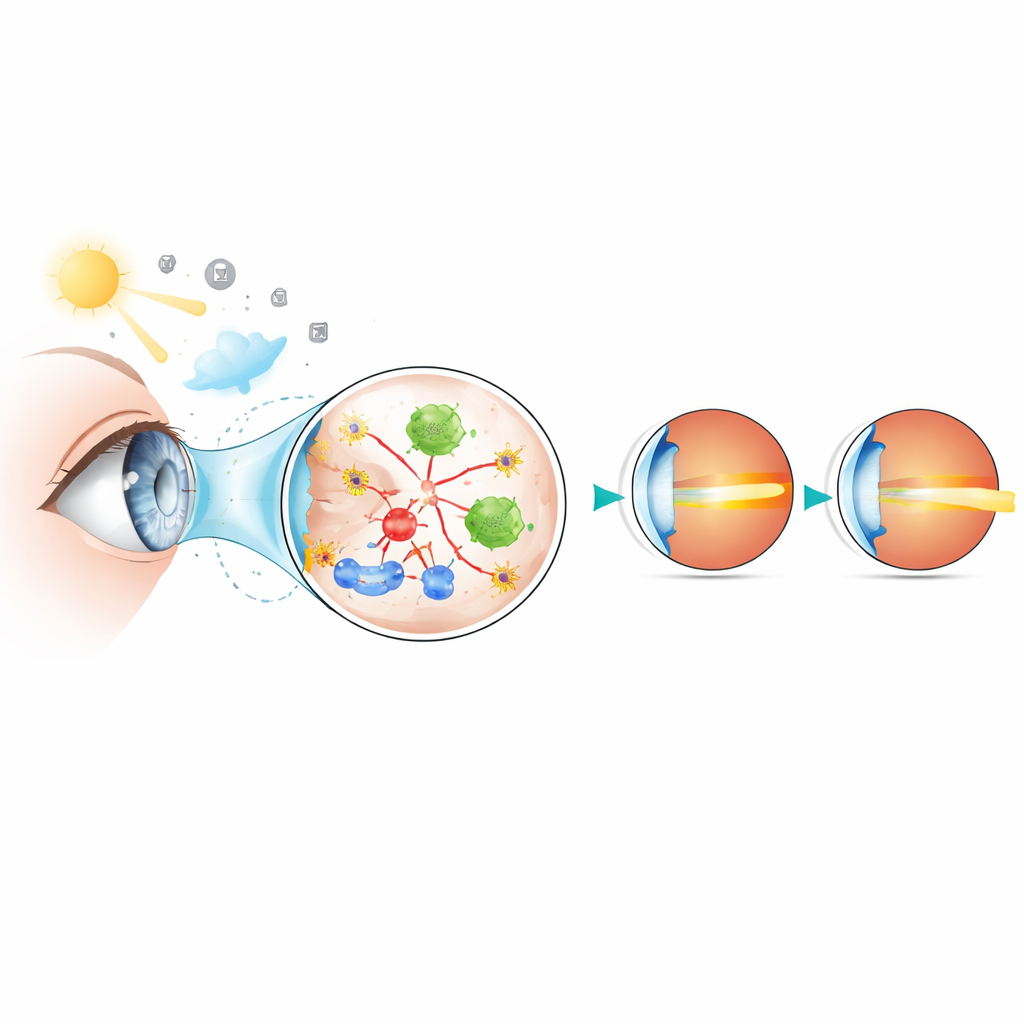
Przednie okno oka pod presją
Rogówka odpowiada za około dwie trzecie mocy skupiającej oka, więc nawet subtelne zmiany jej przejrzystości czy kształtu mogą wpłynąć na widzenie. Badacze zainteresowali się stresem oksydacyjnym — zaburzeniem biochemicznym, w którym szkodliwe produkty reakcji tlenowych przewyższają mechanizmy obronne organizmu. Wcześniejsze badania sugerowały obecność stresu oksydacyjnego w cieczach oka i siatkówce w oku krótkowzrocznym, ale rogówka była słabiej zbadana. Ponieważ jest ona łatwo dostępna podczas rutynowych zabiegów okulistycznych, zespół założył, że rogówka może jednocześnie pełnić rolę sensora uszkadzającego stresu i praktycznego źródła biomarkerów — mierzalnych molekularnych oznak choroby.
Kopanie w dużych zbiorach danych w poszukiwaniu molekularnych odcisków palca
Aby odnaleźć takie „odciski”, naukowcy połączyli kilka publicznie dostępnych zestawów danych ekspresji genów z tkanki rogówki i komórek soczewki osób z krótkowzrocznością i bez niej. Najpierw zidentyfikowali tysiące genów, których aktywność różniła się między próbkami krótkowzrocznymi a kontrolnymi, a następnie zawęzili tę listę do mniejszej grupy już powiązanej ze stresem oksydacyjnym. Przy użyciu nowoczesnych technik uczenia maszynowego, w tym regresji LASSO i algorytmu selekcji cech Boruta, skupili się na trzech kluczowych genach — ATF3, GRIN2B i GSTM3 — które konsekwentnie odróżniały tkankę krótkowzroczną od normalnej.
Trzy lampki ostrzegawcze w rogówce
ATF3 pomaga komórkom reagować na sygnały stresowe, GRIN2B jest elementem kanału komunikacyjnego zwykle badanym w mózgu, a GSTM3 uczestniczy w detoksykacji reaktywnych cząsteczek przy udziale antyoksydantu glutationu. Zarówno w połączonych zestawach danych, jak i w niezależnym zbiorze walidacyjnym, wszystkie trzy markery miały niższą ekspresję w próbkach krótkowzrocznych. Zespół sprawdził następnie rzeczywistą ludzką tkankę rogówki pobraną podczas operacji laserowej SMILE u młodych dorosłych z niską i wysoką krótkowzrocznością. Stwierdzono, że poziomy mRNA ATF3 i GSTM3 były istotnie niższe w rogówkach z dużą krótkowzrocznością, a pomiary białek potwierdziły obniżenie wszystkich trzech markerów. Ciekawie, analiza statystyczna zwana randomizacją Mendla nie potwierdziła tych genów jako bezpośrednich przyczyn genetycznych krótkowzroczności, sugerując raczej, że sama krótkowzroczność lub jej środowisko może tłumić ich aktywność.
Zmiany odpornościowe i szlaki stresowych komórek
Patrząc poza pojedyncze geny, autorzy zbadali, jak komórki odpornościowe i szersze szlaki komórkowe różnią się między grupami. Oszacowali mieszankę 22 typów komórek odpornościowych obecnych w próbkach rogówki i znaleźli istotne zmiany u osób z krótkowzrocznością, w tym więcej komórek CD8+ i monocytów oraz mniej eozynofilów i odpoczywających pamięciowych komórek CD4+. Trzy biomarkery były silnie ujemnie skorelowane z komórkami CD8+ i dodatnio powiązane z eozynofilami, co sugeruje, że obniżona obrona przeciwko stresowi oksydacyjnemu idzie w parze z bardziej zapalnym krajobrazem immunologicznym. Dodatkowe analizy szlaków łączyły te markery z połączeniami międzykomórkowymi, reakcjami na niskie stężenie tlenu i uszkodzeniami od promieniowania UV. Razem wyniki te wspierają obraz, w którym chroniczny stres w mikrośrodowisku rogówki przekształca zarówno sygnalizację komórkową, jak i aktywność układu odpornościowego.
Wskazówki dotyczące przyszłych terapii i obecne ograniczenia
Aby zbadać potencjalne podejścia terapeutyczne, badacze wykorzystali bazy danych lek–gen oraz komputerowe dokowanie molekularne, by przewidzieć związki, które mogłyby wchodzić w interakcje z trzema biomarkerami. Kwas retinowy, aktywna forma witaminy A ważna dla zdrowia rogówki, wyłonił się jako wspólny kandydat, który teoretycznie mógłby wpływać na wszystkie trzy. Jednak te przewidywania mają charakter wyłącznie obliczeniowy i wymagają starannych badań laboratoryjnych i klinicznych. Autorzy podkreślają także, że ich badanie opiera się na stosunkowo niewielkich próbach i mieszanych źródłach tkanek, a wiele wnioskowanych mechanizmów nadal musi zostać potwierdzonych eksperymentalnie.
Co to oznacza dla osób z krótkowzrocznością
Ogólnie rzecz biorąc, badanie sugeruje, że przednia część oka nie jest jedynie bierną soczewką, lecz aktywnym uczestnikiem krótkowzroczności, przy czym geny związane ze stresem oksydacyjnym i komórki odpornościowe zmieniają się w sposób korespondujący z ciężkością choroby. ATF3, GRIN2B i GSTM3 wyróżniają się jako obiecujące biomarkery, które kiedyś mogą pomóc lekarzom ocenić ryzyko krótkowzroczności lub monitorować jej postęp na podstawie łatwo pozyskiwanej tkanki rogówki. Chociaż jest za wcześnie, by zmieniać praktykę kliniczną, praca ta kładzie molekularne podstawy pod przyszłe strategie mające na celu ochronę antyoksydacyjnych mechanizmów rogówki i uspokojenie szkodliwych reakcji immunologicznych, aby spowolnić lub zapobiec pogarszaniu się krótkowzroczności.
Cytowanie: Zhou, Q., Ye, M., Zhang, Z. et al. Gene expression and machine learning techniques uncover corneal biomarkers associated with oxidative stress in the myopia progression. Sci Rep 16, 10651 (2026). https://doi.org/10.1038/s41598-026-46896-x
Słowa kluczowe: krótkowzroczność, rogówka, stres oksydacyjny, biomarkery, odporność oka