Clear Sky Science · zh
整合分子与组织学剖析的先兆子痫研究提示与母婴结局相关的血管生成失调
当孕期血压变得危险
先兆子痫是一种发生于妊娠期的严重高血压形式,可能危及母亲和胎儿的生命。多年来临床已知胎盘——连接母婴的共同生命线——在该疾病中起着核心作用,但究竟在这个器官内部发生了什么变化更难以明确。本研究深入分析了有无先兆子痫女性的胎盘结构与化学特征,尝试将显微镜下的改变与诸如新生儿出生体重和分娩时间等现实结局联系起来。
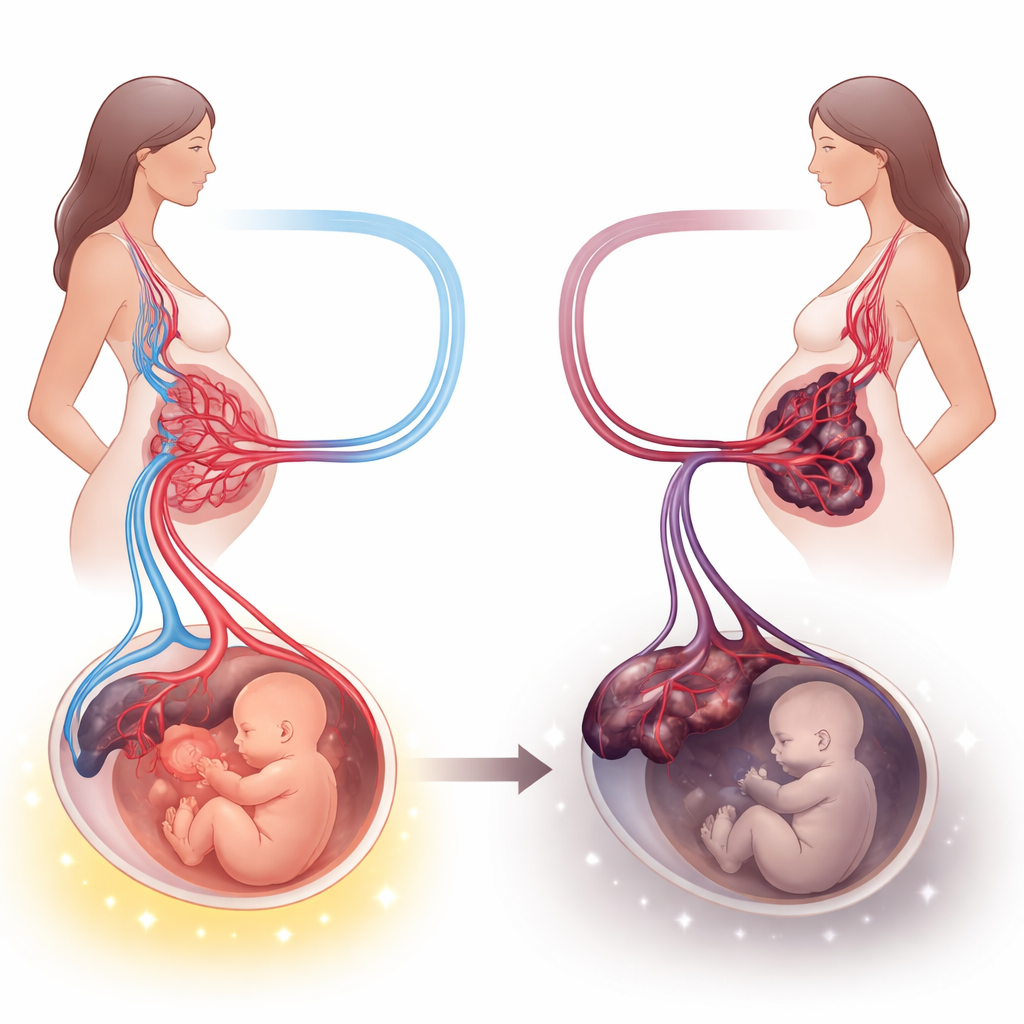
仔细观察孕期生命线
研究者检查了30例先兆子痫患者和30例血压正常妊娠女性的胎盘。他们不仅称量并测量这些器官,还对薄切组织进行显微镜观察,并使用特殊染色来突出关键分子。这些标志物包括有助于血管生长、维持血管内皮健康、控制炎症与调节细胞凋亡的物质。通过将这些实验室发现与血压、用药、分娩周数和新生儿健康等病历数据相结合,研究团队构建了先兆子痫如何重塑胎盘的综合图景。
胎盘应激的物理征象
与健康妊娠相比,先兆子痫母体的胎盘更小、重量更轻,且其婴儿通常较早出生且体重较低。在显微镜下,先兆子痫胎盘显示出慢性应激的特征:更多的衰老表面细胞簇(称为合胞块)、绒毛间类凝块样增厚、用于物质交换的细小分支发育不全、肿胀空隙、缺血区以及大量钙化沉积。这些特征共同提示胎盘血流受损,组织在低氧高压环境下试图但未能成功适应。
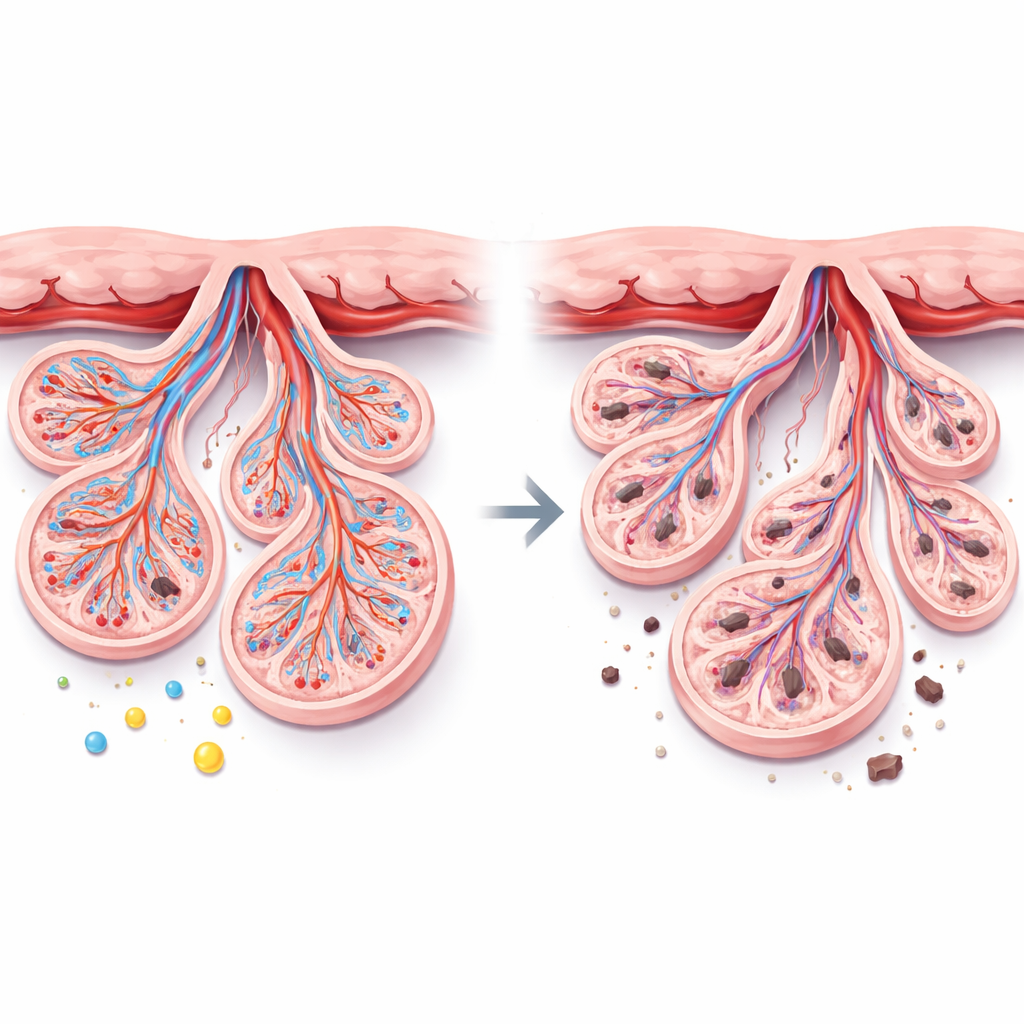
分子线索:生长信号、保护与损伤
在分子水平上,研究发现若干具有保护和促进生长作用的信号在先兆子痫中被下调,而损伤信号则被上调。具有细胞保护作用并支持血管健康的α‑Klotho蛋白显著降低。引导新血管生成和功能的标志物,如VEGF、PlGF和eNOS,也明显减少。相反,强烈的炎症分子TNF‑α大幅升高。一项检测断裂DNA的检测显示胎盘内细胞凋亡显著增加。重要的是,α‑Klotho的变化通常与这些促进健康生长的标志物及胎盘重量同向变化,而与炎症和细胞死亡呈相反方向,这暗示它可能在维持胎盘平衡中起关键作用。
将胎盘改变与母婴结局联系起来
通过在统计模型中校正年龄、吸烟和妊娠时长等因素,作者表明先兆子痫本身与这一组胎盘改变有强关联:更多的炎症与细胞死亡,以及较少的促进血管健康的蛋白。这些变化也与更小的胎盘和更低的出生体重相关,哪怕在调整了早产因素后依然存在。早发型先兆子痫表现出尤其明显的α‑Klotho下降,同时血管相关酶的活性在一定程度上保留,提示机体可能在早期尝试对胎盘应激作出补偿。镁硫酸等治疗似乎对部分血管生长信号有轻度支持作用,但本研究样本量有限,无法得出确定结论。
对未来妊娠的意义
简而言之,这项工作支持这样一种观点:先兆子痫不仅仅是高血压问题;它是胎盘受损、血管形成或功能异常的疾病。胎盘变得更小、更瘢痕化、更容易发生细胞死亡,进而限制胎儿生长并可能导致早产。通过将胎盘的形态变化与化学信号和临床结局联系起来,研究突出显示α‑Klotho及相关血管生长因子,作为未来检测或治疗的有希望目标。尽管该研究尚不能证明因果关系,但它指向了保护母婴共同生命线的新途径。
引用: Gelenli Dolanbay, E., Hocaoglu, M., Mert, T. et al. Integrated molecular and histological profiling of preeclampsia suggests angiogenic dysregulation associated with maternal and fetal outcomes. Sci Rep 16, 12874 (2026). https://doi.org/10.1038/s41598-026-45626-7
关键词: 先兆子痫, 胎盘, 血管生成, 妊娠并发症, 出生体重