Clear Sky Science · de
Integrierte molekulare und histologische Profilierung der Präeklampsie deutet auf angiogene Fehlregulation in Verbindung mit maternalen und fetalen Ergebnissen hin
Wenn der Blutdruck in der Schwangerschaft gefährlich wird
Präeklampsie ist eine schwere Form von Bluthochdruck, die während der Schwangerschaft auftritt und Mutter und Kind gefährden kann. Ärztinnen und Ärzte wissen seit Jahren, dass die Plazenta – die gemeinsame Lebensader zwischen beiden – eine zentrale Rolle in dieser Erkrankung spielt; was genau in diesem Organ schiefgeht, war jedoch schwer zu fassen. Diese Studie untersucht eingehend Aufbau und Chemie der Plazenta bei Frauen mit und ohne Präeklampsie, mit dem Ziel, mikroskopische Veränderungen mit realen Ergebnissen wie Geburtsgewicht und Entbindungszeitpunkt zu verknüpfen.
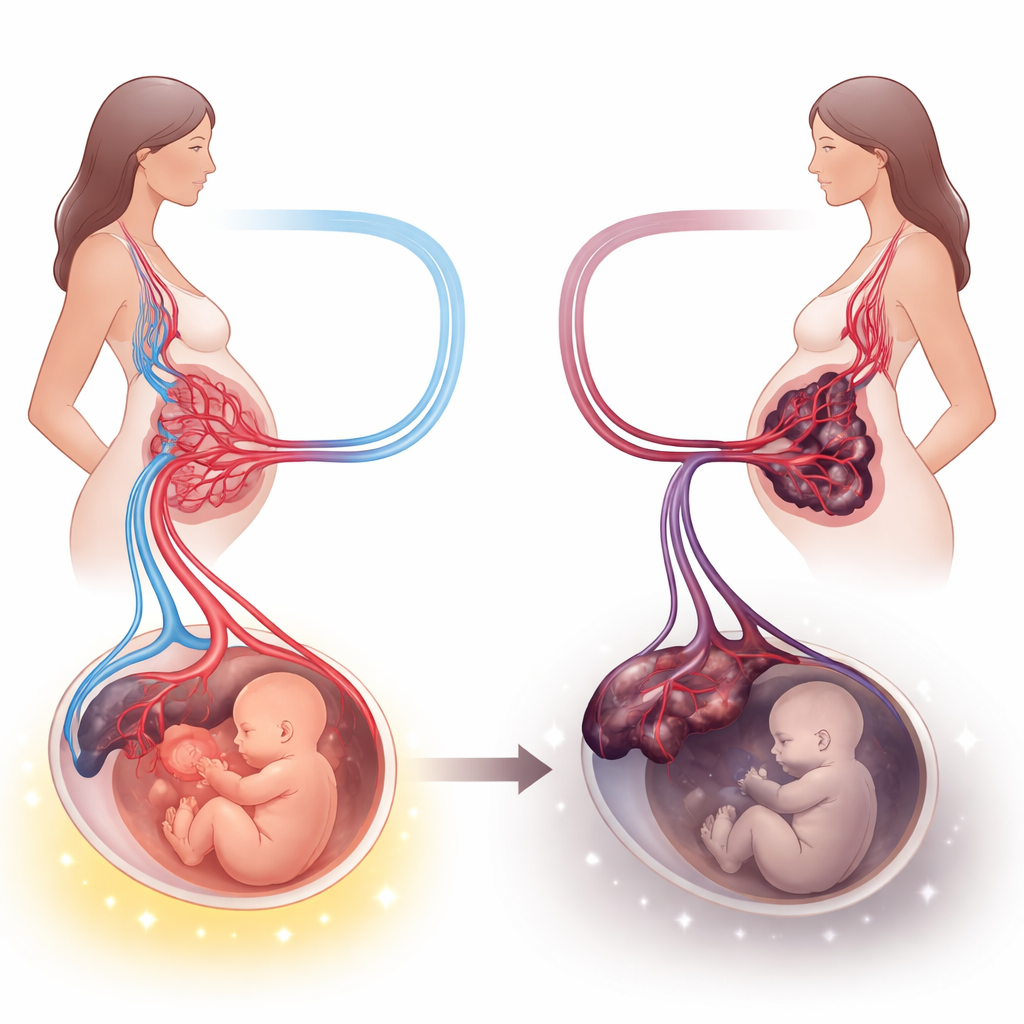
Die Lebensader der Schwangerschaft genau betrachten
Die Forschenden untersuchten Plazenten von 30 Frauen mit Präeklampsie und 30 Frauen mit normalem Blutdruck. Sie wogen und maßen diese Organe nicht nur; sie betrachteten auch dünne Gewebeschnitte im Mikroskop und verwendeten spezielle Färbungen, um entscheidende Moleküle hervorzuheben. Zu diesen Markern gehörten Substanzen, die das Wachstum von Blutgefäßen fördern, die gesunde Gefäßauskleidung erhalten, Entzündungen steuern und den programmierten Zelltod regulieren. Durch die Kombination dieser Laborbefunde mit medizinischen Aufzeichnungen zu Blutdruck, Medikamenten, Schwangerschaftswoche bei der Geburt und Neugeborenenbefunden entstand ein integriertes Bild davon, wie Präeklampsie die Plazenta umgestaltet.
Physische Zeichen einer gestressten Plazenta
Im Vergleich zu gesunden Schwangerschaften waren Plazenten von Müttern mit Präeklampsie kleiner und leichter, und ihre Kinder kamen tendenziell früher und mit geringerem Gewicht zur Welt. Im Mikroskop zeigten die Präeklampsie-Plazenten Kennzeichen chronischen Stresses: mehr Ansammlungen gealterter Oberflächenzellen (sogenannte Syncytialknoten), dichtere Bänder von gerinnungsähnlichem Material zwischen den fingerartigen Villi, unterentwickelte kleine Verzweigungen dort, wo der Austausch stattfinden sollte, Bereiche mit Schwellungen, Regionen ohne Blutgefäße und starke Ablagerungen von Kalzium. Zusammengenommen deuten diese Merkmale darauf hin, dass der Blutfluss durch die Plazenta beeinträchtigt ist und das Gewebe versucht – und dabei scheitert –, sich an eine sauerstoffarme, hochdruckbelastete Umgebung anzupassen.
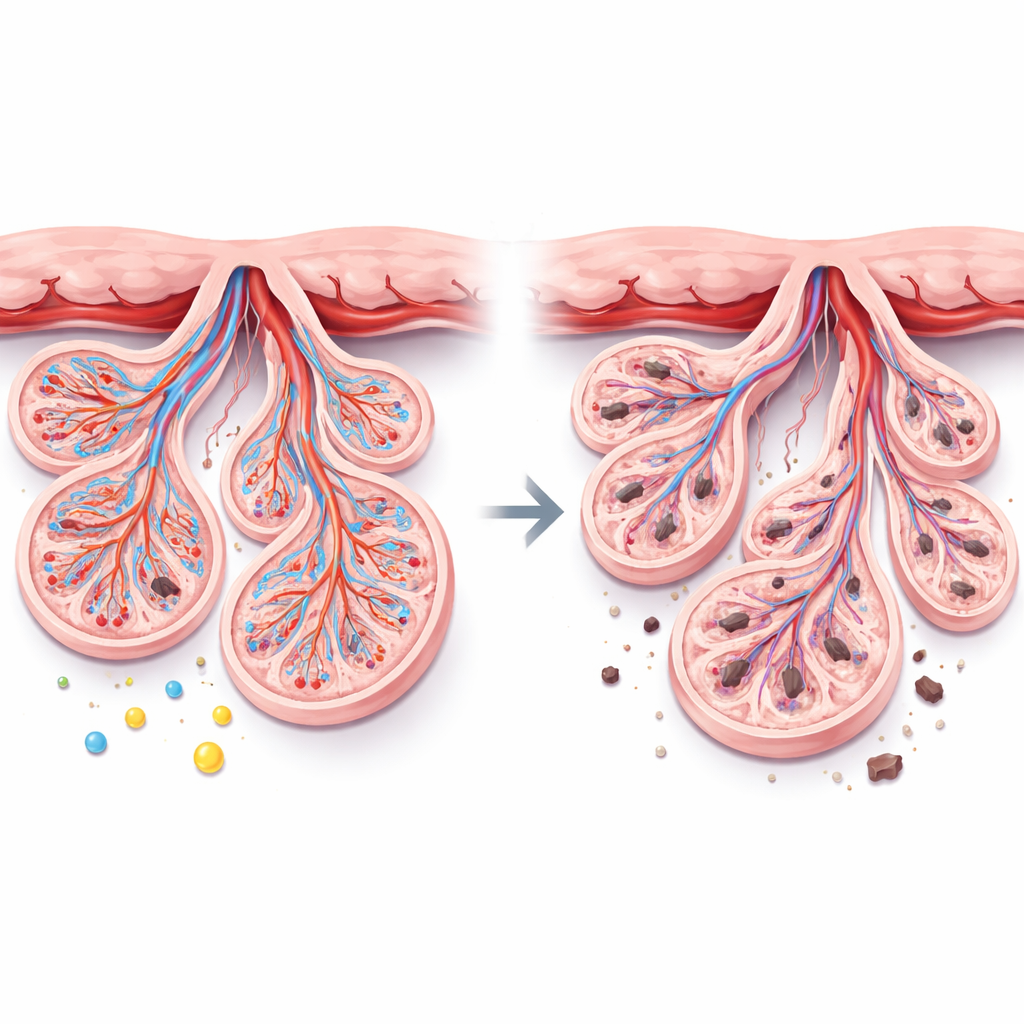
Molekulare Hinweise: Wachstumssignale, Schutz und Schäden
Auf molekularer Ebene zeigte die Studie, dass mehrere schützende und wachstumsfördernde Signale bei Präeklampsie gedämpft sind, während schädliche Signale verstärkt auftreten. Die Spiegel von α-Klotho, einem Protein, das Zellen vor Stress schützt und gesunde Blutgefäße unterstützt, waren deutlich niedriger. Ebenso reduziert waren Marker, die das Wachstum und die Funktion neuer Gefäße steuern, wie VEGF, PlGF und eNOS. Dagegen war TNF-α, ein starkes entzündliches Molekül, deutlich erhöht. Ein Test zum Nachweis von DNA-Bruchstücken zeigte einen Anstieg des Zelltods in der Plazenta. Wichtig ist, dass α-Klotho tendenziell mit den gesunden Wachstumsmarkern und dem Plazentagewicht zusammenhing und sich entgegengesetzt zu Entzündung und Zelltod bewegte, was darauf hindeutet, dass es eine zentrale Rolle bei der Aufrechterhaltung des Plazentagleichgewichts spielen könnte.
Verknüpfung plazentarer Veränderungen mit Mutter und Kind
Mithilfe statistischer Modelle, die Alter, Rauchen und Schwangerschaftsdauer berücksichtigten, zeigten die Autorinnen und Autoren, dass Präeklampsie selbst stark mit diesem Cluster plazentarer Veränderungen verbunden war: mehr Entzündung und Zelltod sowie weniger Proteine, die gesunde Gefäße fördern. Diese Verschiebungen standen außerdem mit kleineren Plazenten und niedrigerem Geburtsgewicht in Zusammenhang, selbst nach Anpassung an das Frühgeburtsalter. Bei früh einsetzender Präeklampsie zeigte sich ein besonders ausgeprägter Verlust von α-Klotho bei teilweise erhaltenem Gefäßenzymaktivitätsmuster, was darauf hindeutet, dass der Körper zunächst versucht, dem plazentaren Stress entgegenzusteuern. Behandlungen wie Magnesiumsulfat schienen einige gefäßfördernde Signale moderat zu unterstützen, wobei die Studie zu klein war, um definitive Schlussfolgerungen zu erlauben.
Was das für künftige Schwangerschaften bedeutet
Einfach gesagt unterstützt diese Arbeit die Auffassung, dass Präeklampsie nicht nur mit hohem Blutdruck zu tun hat; sie ist eine Erkrankung einer belasteten Plazenta, deren Blutgefäße nicht richtig ausgebildet sind oder funktionieren. Das Organ wird kleiner, vernarbt stärker und ist anfälliger für Zelltod, was wiederum das Wachstum des Kindes einschränkt und eine vorzeitige Geburt auslösen kann. Indem die Studie das Aussehen der Plazenta mit chemischen Signalen und klinischen Ergebnissen verknüpft, hebt sie α-Klotho und verwandte gefäßfördernde Faktoren als vielversprechende Ziele für künftige Tests oder Behandlungen hervor. Zwar kann die Forschung noch keinen kausalen Zusammenhang beweisen, doch sie weist auf neue Möglichkeiten hin, die gemeinsame Lebensader von Mutter und Kind zu schützen.
Zitation: Gelenli Dolanbay, E., Hocaoglu, M., Mert, T. et al. Integrated molecular and histological profiling of preeclampsia suggests angiogenic dysregulation associated with maternal and fetal outcomes. Sci Rep 16, 12874 (2026). https://doi.org/10.1038/s41598-026-45626-7
Schlüsselwörter: Präeklampsie, Plazenta, Angiogenese, Komplikationen in der Schwangerschaft, Geburtsgewicht