Clear Sky Science · zh
硫氧还蛋白通过调控TOMM22介导的线粒体自噬保护糖尿病性听力损失并抑制小胶质细胞的M1极化
为什么糖尿病会悄悄夺走你的听力
许多人知道糖尿病会损害眼睛、肾脏和神经,但很少意识到它也会渐进性地侵蚀听力。本研究探讨了这种现象的原因,并强调了一种体内的天然保护蛋白——硫氧还蛋白,它既可能作为早期损伤的信号,也可能帮助保护内耳中敏感的感音细胞。理解这一隐匿联系,有望推动更早的诊断以及新的方法来保护糖尿病患者的听力。
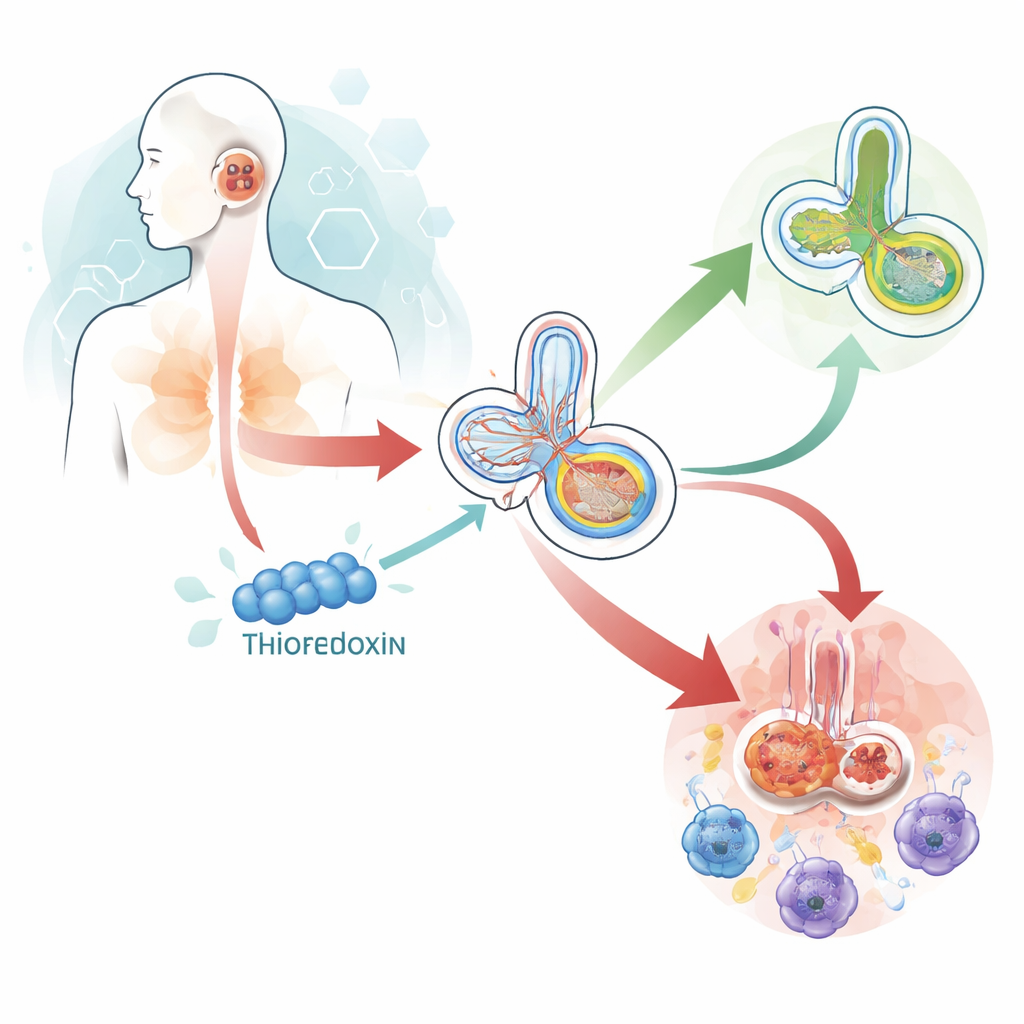
高血糖如何给内耳施加压力
糖尿病使血糖长期升高,产生有害代谢产物并压垮机体防御能力。内耳特别脆弱,因为其毛细胞和神经细胞对能量要求高,富含线粒体——细胞的能量工厂。在高糖环境下,这些线粒体产生过量的活性分子,损伤蛋白质、脂质和DNA。当损伤过大时,细胞要么通过清除机制销毁受损线粒体,要么在不堪重负时触发自我毁灭程序。随着时间推移,这会导致负责放大声响的外毛细胞减少,引发许多糖尿病患者常见的高频听力下降。
一种天然防御者与早期预警信号
硫氧还蛋白是一种小型蛋白,有助于维持细胞内化学平衡并减轻有害氧化。研究者测量了2型糖尿病患者血液中的硫氧还蛋白水平,并将其与能够检测耳蜗微弱回声的详尽听力测试结果进行比较。结果显示,出现糖尿病性听力损失的个体具有较差的耳蜗回声信号和更高的血中硫氧还蛋白水平。在糖尿病群体中,血中硫氧还蛋白越高,耳蜗功能越差。硫氧还蛋白并非单纯良性或有害:它似乎随着机体抗压能力的消耗而上升,因此可能成为一个有前景的血液标志,提示内耳正在出现问题——甚至可能在日常交流困难出现之前就先发出警报。
保护耳朵的“能量工厂”免于超负荷
为从相关性走向因果,研究团队使用糖尿病小鼠和培养的内耳细胞追踪耳蜗内部的变化。在糖尿病小鼠中,耳蜗出现了与细胞死亡相关的蛋白活性增加,以及以PINK1/Parkin系统为中心的过度活跃的线粒体清除路径,这一系统是已知的质量控制机制。通过计算分析,作者识别出线粒体表面一个关键的门控蛋白TOMM22,作为连接硫氧还蛋白与该通路的枢纽。在糖尿病动物中,TOMM22水平下降而PINK1及相关信号上升,提示维护性清理向破坏性过度响应的转变。当小鼠被改造以产生更多硫氧还蛋白时,这一模式发生逆转:细胞死亡信号减轻,TOMM22水平得以维持,线粒体清除机制趋于平稳。
双重防护:毛细胞与免疫细胞
在暴露于类似糖尿病应激的培养听觉细胞中,增加硫氧还蛋白能恢复线粒体膜健康、减少细胞死亡并抑制过度的清除活动,这些变化与TOMM22的维持一致。研究者在人工破坏线粒体功能并抑制TOMM22时,这些保护效应大多消失,强调了TOMM22的核心作用。研究还关注了小胶质细胞——巡逻内耳的免疫细胞。在糖相关应激下,这些细胞会转向侵袭性、促炎状态,可能加剧组织损伤。提升硫氧还蛋白水平则使它们转向更平和、倾向修复的表型。当将富含硫氧还蛋白的小胶质细胞分泌物应用于听觉细胞时,线粒体功能改善且有害的清除信号下降,表明硫氧还蛋白既能在毛细胞内直接保护听力,也能通过重塑其免疫环境间接发挥保护作用。
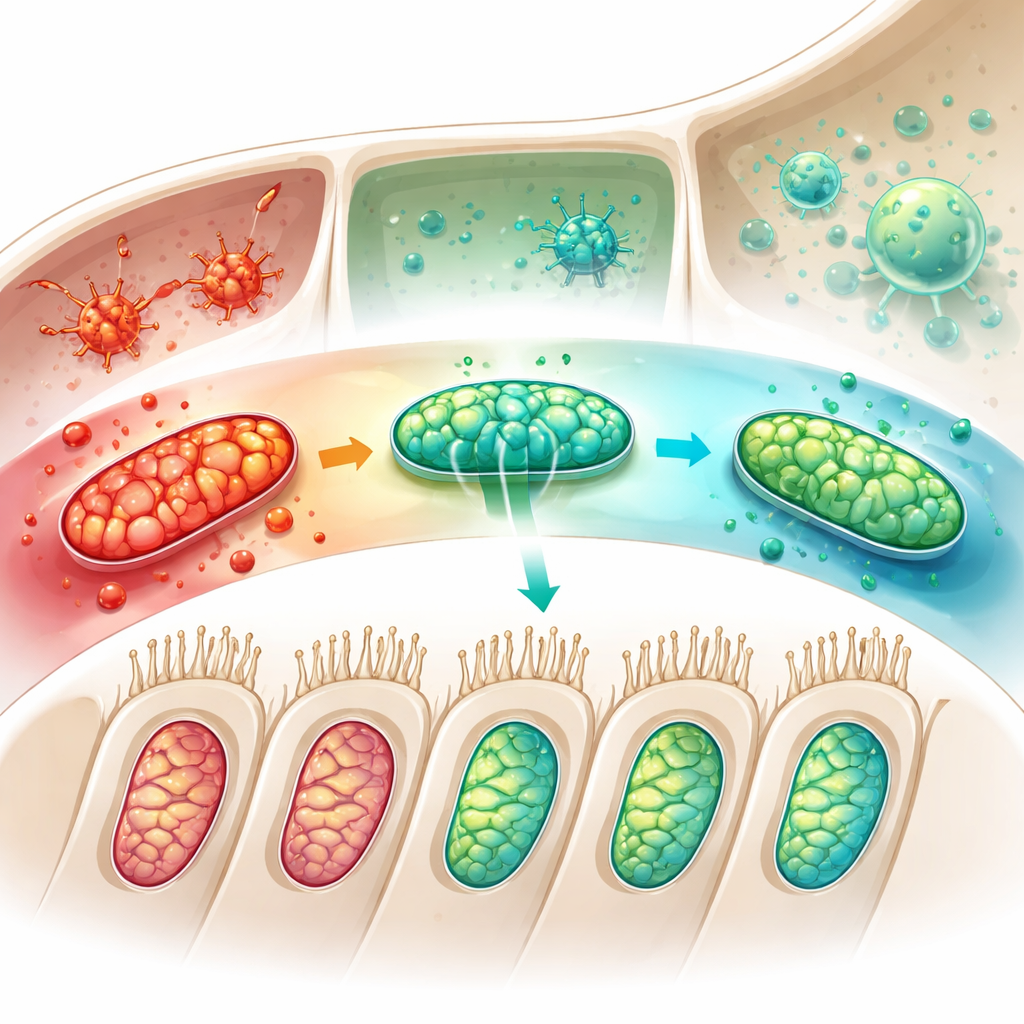
这对糖尿病患者意味着什么
简而言之,这项工作表明硫氧还蛋白在糖尿病性内耳中既像烟雾报警器又像消防员。血中升高的水平可能预示耳蜗正遭受氧化性攻击,而在耳内硫氧还蛋白有助于稳定一个关键的线粒体门控蛋白,抑制对受损“能量工厂”的过度清除,并使炎性免疫细胞平静下来。综合这些作用,有助于保护将声音转换为神经信号的脆弱毛细胞。尽管还需要更多长期且面向人群的研究,但硫氧还蛋白及其相关分子现已成为有前景的血液筛查指标和未来旨在预防或减缓糖尿病患者听力丧失的治疗靶点。
引用: Zhong, S., Xu, M., Wang, Q. et al. Thioredoxin protects against diabetic hearing loss by regulating TOMM22 mediated mitochondrial autophagy in hair cells and inhibiting microglial M1 polarization. Sci Rep 16, 14332 (2026). https://doi.org/10.1038/s41598-026-44909-3
关键词: 糖尿病性听力损失, 硫氧还蛋白, 线粒体, 内耳, 神经炎症