Clear Sky Science · ru
Тиоредоксин защищает от диабетической потери слуха, регулируя митохондриальный аутофаг с участием TOMM22 в волосковых клетках и подавляя М1‑поляризацию микроглии
Почему диабет незаметно лишает человека слуха
Многие знают, что диабет может повредить глаза, почки и нервы, но мало кто догадывается, что он также может постепенно разрушать слух. В этом исследовании изучают причины этого явления и выделяют природный защитный белок — тиоредоксин, который может служить ранним сигналом повреждения и одновременно помогать защищать тонкие звуковоспринимающие клетки внутреннего уха. Понимание этой скрытой связи может открыть путь к более ранней диагностике и новым способам сохранения слуха у людей с диабетом.
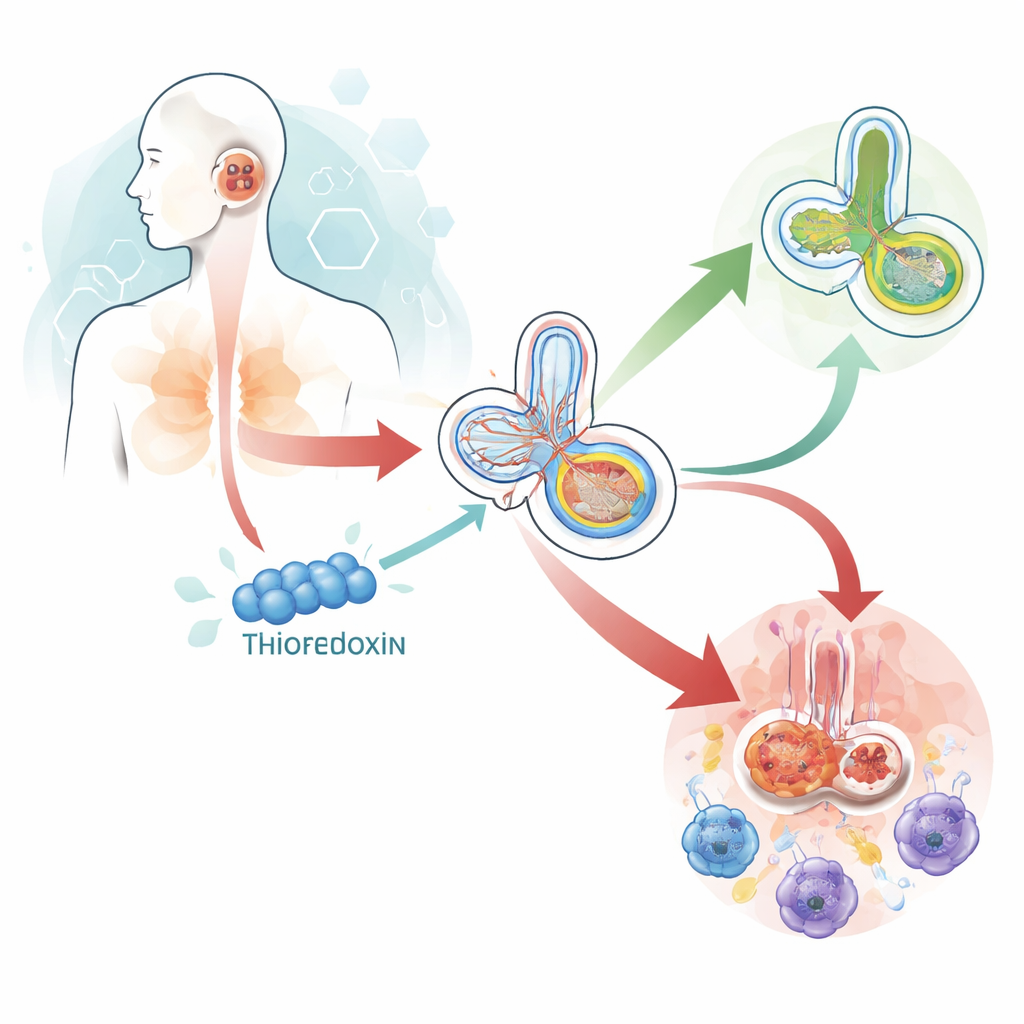
Как высокий уровень сахара нагружает внутреннее ухо
При диабете длительно повышенный уровень глюкозы приводит к образованию вредных побочных продуктов и истощает защитные механизмы организма. Внутреннее ухо особенно уязвимо: его волосковые и нервные клетки энергозависимы и богаты митохондриями — энергетическими станциями клетки. В условиях высокого сахара митохондрии генерируют избыток реактивных молекул, которые повреждают белки, липиды и ДНК. Когда повреждений становится слишком много, клетки либо утилизируют повреждённые митохондрии через процесс очистки, либо, если они перегружены, запускают программы самоуничтожения. Со временем это может истончить наружные волосковые клетки, которые усиливают звук, что приводит к характерной потере слуха в высоких частотах, наблюдаемой у многих людей с диабетом.
Естественный защитник и ранний сигнальный маркер
Тиоредоксин — небольшой белок, который помогает поддерживать внутреннюю химию клетки в равновесии и смягчает вредное окисление. Исследователи измерили уровни тиоредоксина в крови людей с диабетом 2‑го типа и сопоставили их с детальными слуховыми тестами, фиксирующими слабые отклики от улитки. Они обнаружили, что у людей с диабетической потерей слуха сигналы отклика были хуже, а уровень тиоредоксина в крови выше. В пределах группы с диабетом более высокий уровень тиоредоксина в крови коррелировал с худшей работой улитки. Тиоредоксин, по‑всему, не является однозначно «хорошим» или «плохим» — он повышается по мере того, как организм пытается противостоять стрессу, что делает его перспективным кровяным маркером того, что во внутреннем ухе что‑то идёт не так — возможно, ещё до того, как обычный разговор станет затруднительным.
Защита энергетических станций уха от перегрузки
Чтобы перейти от корреляции к причинно‑следственной связи, команда использовала диабетических мышей и культивированные клетки внутреннего уха, чтобы проследить, что происходит внутри улитки. У диабетических мышей в улитке наблюдалась повышенная активность белков, связанных со смертью клеток, и гиперактивность пути очистки митохондрий, сосредоточенного вокруг системы PINK1/Parkin — хорошо известного механизма контроля качества. С помощью вычислительного анализа авторы выявили ключевой воротный белок на поверхности митохондрий, TOMM22, как узловой компонент, связывающий тиоредоксин с этим путём. У диабетических животных уровень TOMM22 снижался, в то время как PINK1 и связанные сигналы повышались, что указывает на смещение от упорядоченного обслуживания к разрушительной гиперактивности. Когда мышей генетически модифицировали для повышенной продукции тиоредоксина, этот паттерн менялся: сигналы смерти клеток уменьшались, уровень TOMM22 лучше сохранялся, а механизм очистки митохондрий успокаивался.
Двусторонний щит: волосковые клетки и иммунные клетки
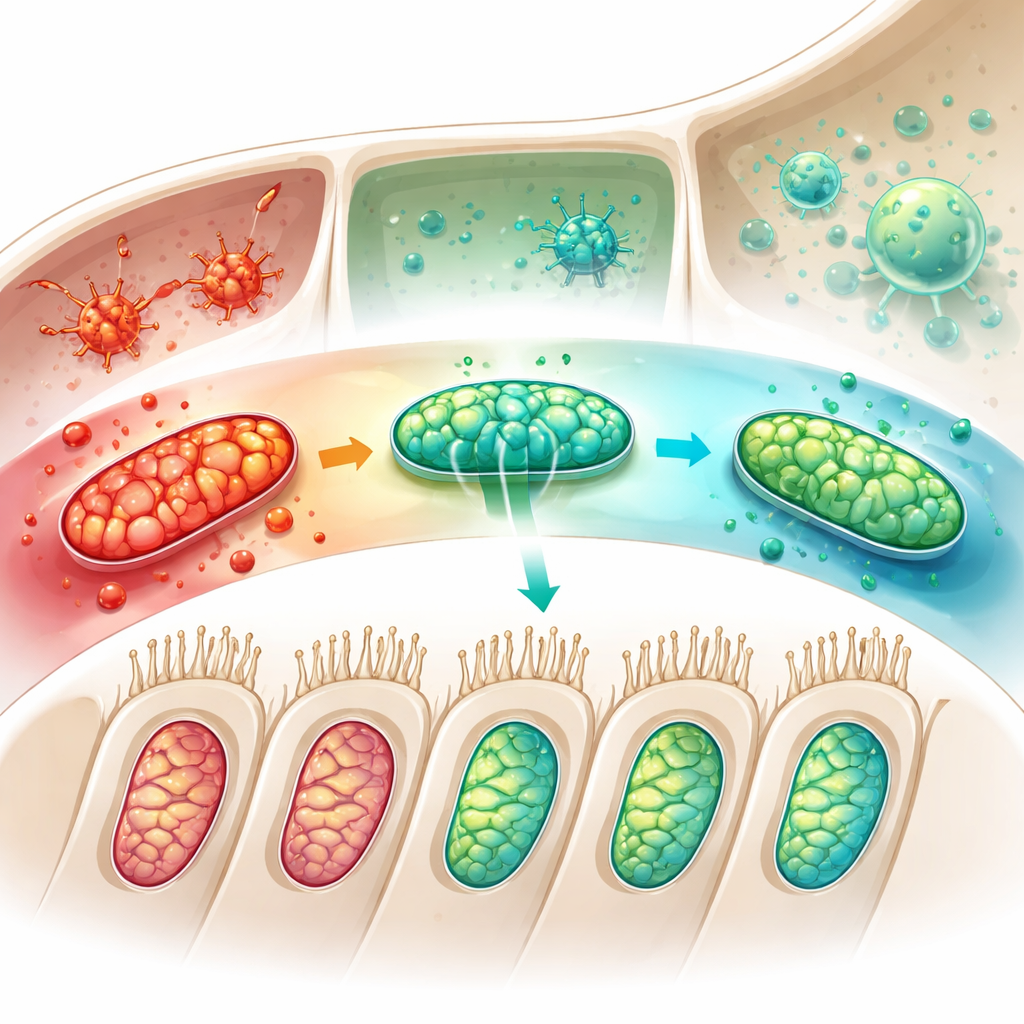
В культивируемых слуховых клетках, подвергнутых стрессу, имитирующему диабет, повышение тиоредоксина восстанавливало целостность митохондриальной мембраны, уменьшало гибель клеток и снижало чрезмерную активность очистки, что вновь сопровождалось сохранением TOMM22. Когда исследователи искусственно нарушали митохондриальную функцию и подавляли TOMM22, эти защитные эффекты в значительной мере исчезали, подчёркивая центральную роль TOMM22. Исследование также обратилось к микроглии — иммунным клеткам, патрулирующим внутреннее ухо. Под влиянием сахар‑связанного стресса эти клетки переходили в агрессивное воспалительное состояние, способное усугублять повреждения тканей. Повышение тиоредоксина направляло их в более спокойный, ориентированный на восстановление профиль. Когда секреты микроглии с высоким содержанием тиоредоксина применяли к слуховым клеткам, митохондриальная функция улучшалась, а вредные сигналы очистки снижались, что показывает: тиоредоксин может защищать слух напрямую в волосковых клетках и косвенно — перепрограммируя их иммунное окружение.
Что это означает для людей с диабетом
Проще говоря, эта работа показывает, что тиоредоксин действует как дымовая сигнализация и как пожарный для диабетического внутреннего уха. Более высокие уровни в крови могут предупреждать о том, что улитка подвергается окислительному натиску, тогда как внутри уха тиоредоксин помогает стабилизировать ключевого митохондриального сторожа, сдерживает чрезмерную утилизацию повреждённых энергетических станций и успокаивает воспалительные иммунные клетки. В совокупности эти действия помогают сохранять хрупкие волосковые клетки, преобразующие звук в нервные сигналы. Хотя необходимы более длительные и ориентированные на человека исследования, тиоредоксин и связанные с ним компоненты выделяются как перспективные цели для скрининга по крови и будущих терапий, направленных на предотвращение или замедление потери слуха у людей с диабетом.
Цитирование: Zhong, S., Xu, M., Wang, Q. et al. Thioredoxin protects against diabetic hearing loss by regulating TOMM22 mediated mitochondrial autophagy in hair cells and inhibiting microglial M1 polarization. Sci Rep 16, 14332 (2026). https://doi.org/10.1038/s41598-026-44909-3
Ключевые слова: диабетическая потеря слуха, тиоредоксин, митохондрии, внутреннее ухо, нейровоспаление