Clear Sky Science · zh
DUSP6通过IL-8诱导的中性粒细胞胞外陷阱促进甲状腺癌细胞的迁移、侵袭和肿瘤形成性
这项甲状腺癌研究为何重要
甲状腺癌通常易于治疗,但有一部分肿瘤会变得更具侵袭性,扩散到身体其他部位并对常规疗法反应减弱。本研究深入探查肿瘤内外某些分子如何帮助癌细胞迁移、侵袭和生长。通过揭示这一潜在的支持体系,研究人员指向了未来药物可能针对的新薄弱环节,以阻止甲状腺癌扩散。
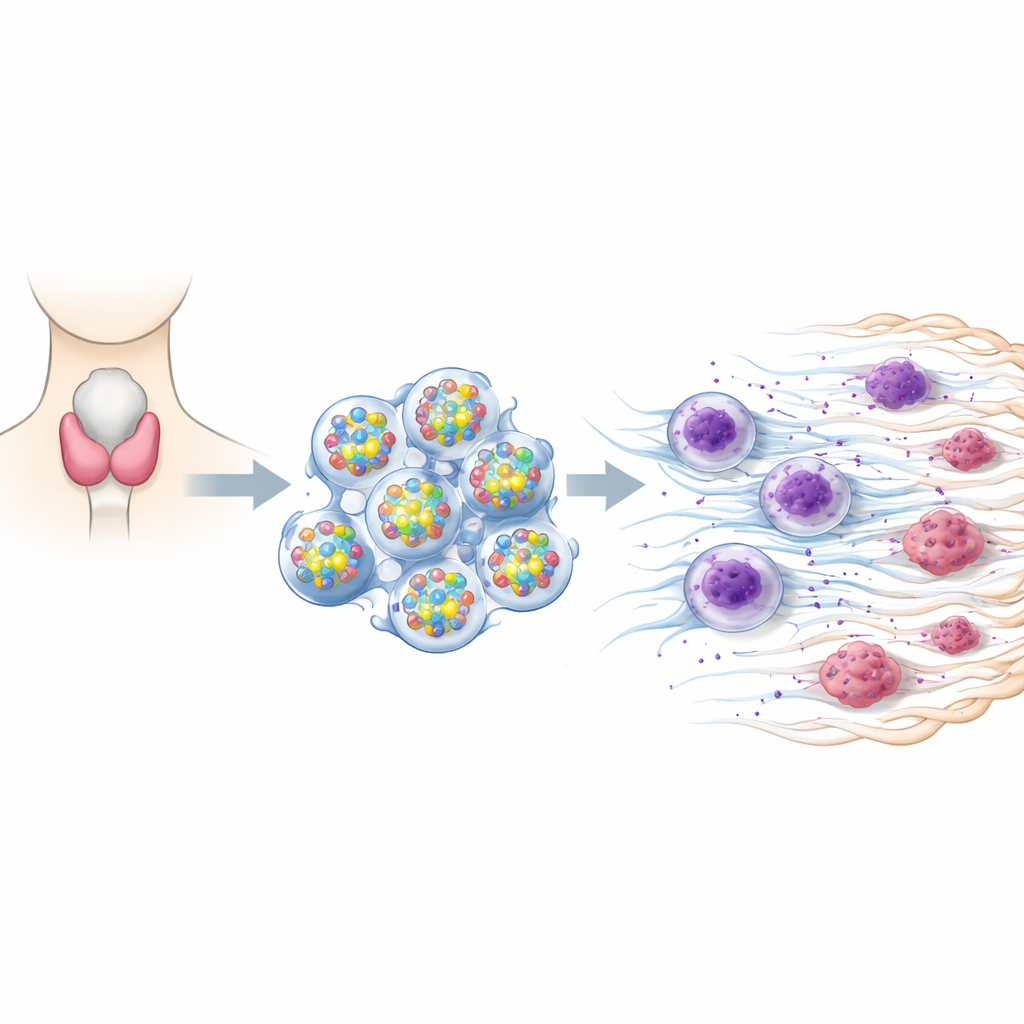
被推到超速的信号开关
团队聚焦于一种名为DUSP6的蛋白,它在细胞内像开关一样调节生长信号的强弱。研究者使用乳头状甲状腺癌患者的样本(这是最常见的甲状腺癌类型),比较了肿瘤组织与邻近健康甲状腺组织。他们发现肿瘤中DUSP6含量显著升高。重要的是,每位患者肿瘤中DUSP6的多少与另外两种标志物——吸引免疫细胞的分子IL-8以及与免疫细胞释放特殊网状结构相关的标志物PAD4——同步变化。该模式提示DUSP6可能在营造有利于肿瘤扩散的微环境中发挥作用。
推动癌细胞生长、移动与侵袭
为了解DUSP6在甲状腺癌细胞内的具体作用,研究人员使用了两种体外培养的人甲状腺癌细胞系。他们在部分细胞中人为提高DUSP6表达,在另一些细胞中将其沉默。当DUSP6被增强时,癌细胞增殖更快、在表面上的迁移更迅速,并且更容易穿过模拟组织的凝胶进行侵袭。这些细胞也更不容易发生程序性细胞死亡。相反,当DUSP6被下调时,生长减慢,迁移和侵袭能力下降,凋亡增加。与此同时,DUSP6改变了细胞表面蛋白的平衡,使细胞趋向于更松散、更具移动性的状态——这在癌症转移时常见。被增强的细胞还产生了更多IL-8,将这一细胞内开关与能够影响周围免疫系统的强效信号联系起来。
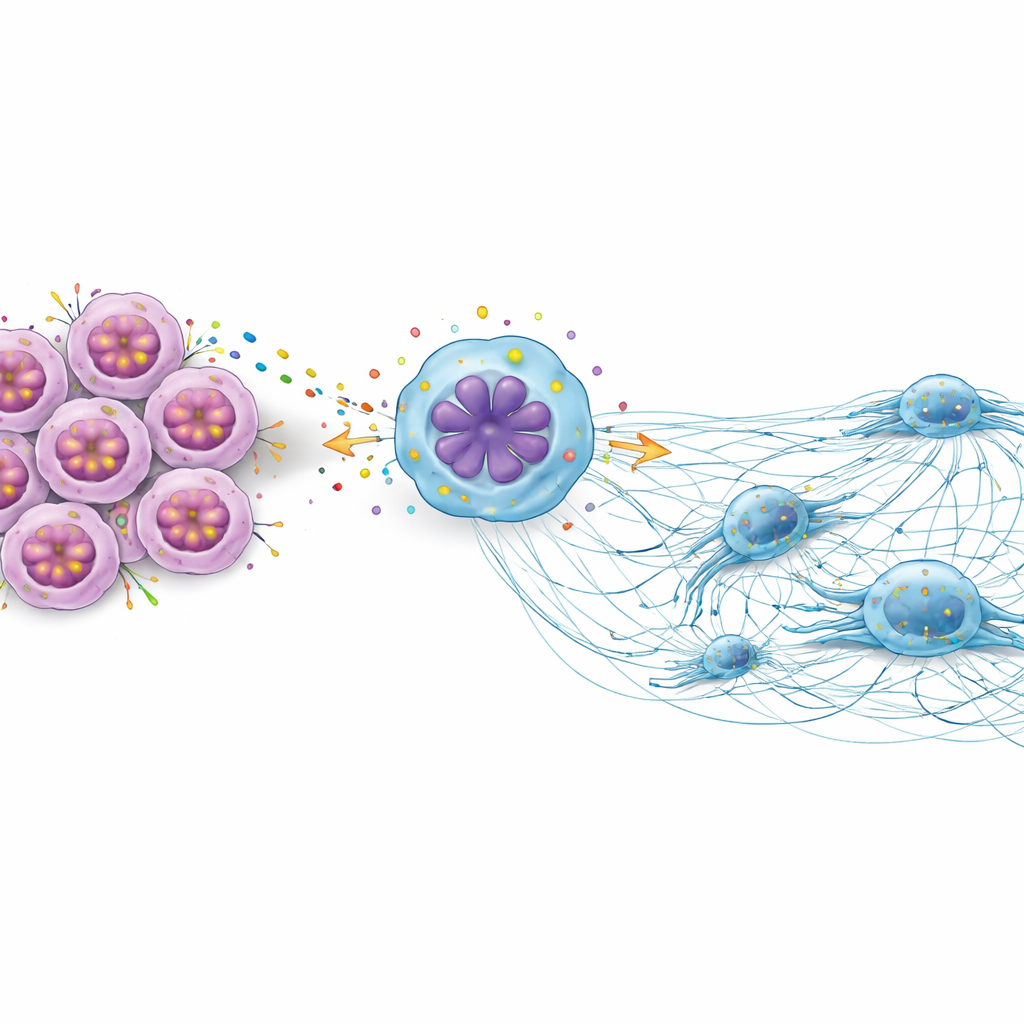
帮助癌症扩散的免疫细胞网
研究随后转向了癌症中较少被关注的角色:中性粒细胞胞外陷阱(NETs)。这些是某些白细胞释放的由DNA和蛋白质构成的黏性网状结构。尽管它们通常有助于捕捉入侵的微生物,NETs也能为癌细胞提供可供行进的通道。在实验皿中,当甲状腺癌细胞暴露于NETs时,它们变得更具迁移性和侵袭性。然而,当DUSP6或IL-8被敲低时,这种由NETs驱动的迁移与侵袭增强就显著减弱。换言之,DUSP6和IL-8使肿瘤细胞对这些有害网状结构更为敏感。
肿瘤信号如何重塑邻近免疫细胞
为了深入研究事件链,研究人员研究了产生NETs的中性粒细胞。当他们在这些细胞中提高DUSP6水平时,NET形成的标志物上升;而当降低DUSP6或阻断IL-8时,这些标志物下降。额外的染色实验证实,当DUSP6水平高且IL-8信号完整时,以DNA为基底的网状结构及其相关蛋白更为丰富。这些发现提示了一个循环:DUSP6升高的甲状腺癌细胞产生更多IL-8,进而促使中性粒细胞释放更多NETs——营造出有利于癌细胞迁移与侵袭的物理和化学环境。
在动物中减缓肿瘤生长
研究团队在小鼠身上测试了该通路的实际影响。他们将甲状腺癌细胞植入小鼠皮下,并使用遗传工具在部分肿瘤中降低DUSP6表达。DUSP6较低的肿瘤生长更慢,最终体积和重量都小于对照组。在显微镜下,这些肿瘤的癌细胞密度较低,蛋白表达模式也显示出更不具侵袭性的特征。来自这些小鼠的肿瘤组织中IL-8和与NET相关的标志物水平也有所降低,与细胞培养中的发现相呼应,支持DUSP6驱动促转移微环境的观点。
这对未来甲状腺癌治疗意味着什么
简而言之,该研究表明,甲状腺癌细胞内的一个蛋白开关DUSP6通过提升IL-8促使免疫细胞释放黏性NETs,从而帮助肿瘤扩散。阻断DUSP6、IL-8或NET形成能够干扰这一链条并在实验中减缓肿瘤生长。尽管还需要更多工作——包括更深入的动物研究和最终的临床试验——这些结果突出了一组三个有前景的靶点,未来有望帮助阻止侵袭性甲状腺癌的侵入与转移。
引用: Xiao, W., Luo, L., Yang, Y. et al. DUSP6 promotes motility, invasion, and tumorigenicity of thyroid cancer cells via IL8-induced neutrophil extracellular traps. Sci Rep 16, 12575 (2026). https://doi.org/10.1038/s41598-026-43233-0
关键词: 甲状腺癌, DUSP6, 白细胞介素-8, 中性粒细胞胞外陷阱, 转移