Clear Sky Science · de
DUSP6 fördert Mobilität, Invasion und Tumorwachstum von Schilddrüsenkrebszellen durch IL-8-induzierte neutrophile extrazelluläre Falle
Warum diese Studie zu Schilddrüsenkrebs wichtig ist
Schilddrüsenkrebs ist in der Regel gut behandelbar, doch ein Teil der Tumoren wird aggressiv, breitet sich in andere Körperregionen aus und spricht nicht mehr gut auf Standardtherapien an. Diese Studie untersucht im Detail, wie bestimmte Moleküle im Tumor und seiner Umgebung Krebszellen helfen, sich zu bewegen, Gewebe zu durchdringen und zu wachsen. Indem die Forschenden dieses verborgene Unterstützungssystem aufdecken, zeigen sie neue potenzielle Schwachstellen auf, die künftige Wirkstoffe anvisieren könnten, um die Ausbreitung von Schilddrüsenkrebs zu verhindern.
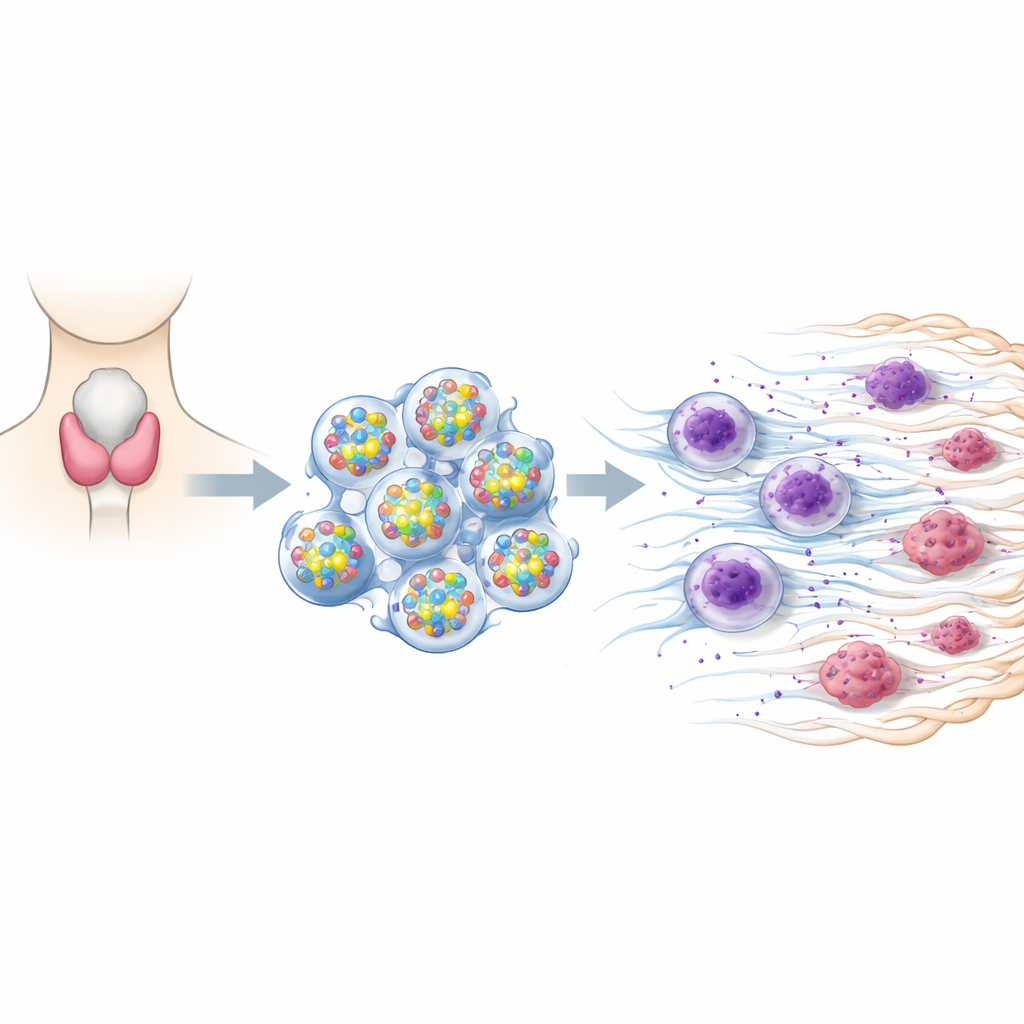
Ein Signalumschalter, der auf Hochtouren läuft
Das Team konzentrierte sich auf ein Protein namens DUSP6, das wie ein Schalter in Zellen wirkt und Wachstumssignale hoch- oder herunterregeln kann. An Patient*innenproben mit papillärer Schilddrüsenkarzinom, der häufigsten Form von Schilddrüsenkrebs, verglichen sie Tumorgewebe mit benachbartem gesundem Schilddrüsengewebe. Sie fanden, dass die Tumoren deutlich höhere DUSP6-Spiegel aufwiesen. Entscheidenderweise schwankte die Menge an DUSP6 in den Tumoren synchron mit zwei weiteren Markern: IL‑8, einem Molekül, das Immunzellen anzieht, und PAD4, einem Marker, der mit speziellen Netzen von Immunzellen in Verbindung steht. Dieses Muster deutete darauf hin, dass DUSP6 zur Entstehung einer Umgebung beitragen könnte, die die Tumorausbreitung begünstigt.
Krebszellen zu Wachstum, Bewegung und Invasion antreiben
Um zu prüfen, was DUSP6 tatsächlich in Schilddrüsenkrebszellen bewirkt, nutzten die Forschenden zwei menschliche Schilddrüsenkrebszelllinien im Labor. Sie erhöhten DUSP6 künstlich in einigen Zellen und schalteten es in anderen aus. Wurde DUSP6 hochreguliert, teilten sich die Krebszellen schneller, bewegten sich schneller über Oberflächen und drangen leichter durch ein Gel, das Gewebe nachahmt. Diese Zellen waren außerdem weniger anfällig für programmierte Zelltodprozesse. Wurde DUSP6 vermindert, zeigte sich das Gegenteil: Wachstum verlangsamte sich, Bewegung und Invasion nahmen ab und mehr Zellen starben. Gleichzeitig veränderte DUSP6 das Gleichgewicht der Oberflächenproteine der Zellen und förderte einen lockereren, mobileren Zustand, wie er häufig bei metastasierenden Krebszellen zu sehen ist. Die hochregulierten Zellen produzierten außerdem mehr IL‑8, wodurch dieser intrazelluläre Schalter mit einem starken Signal verbunden wurde, das das umliegende Immunsystem beeinflussen kann.
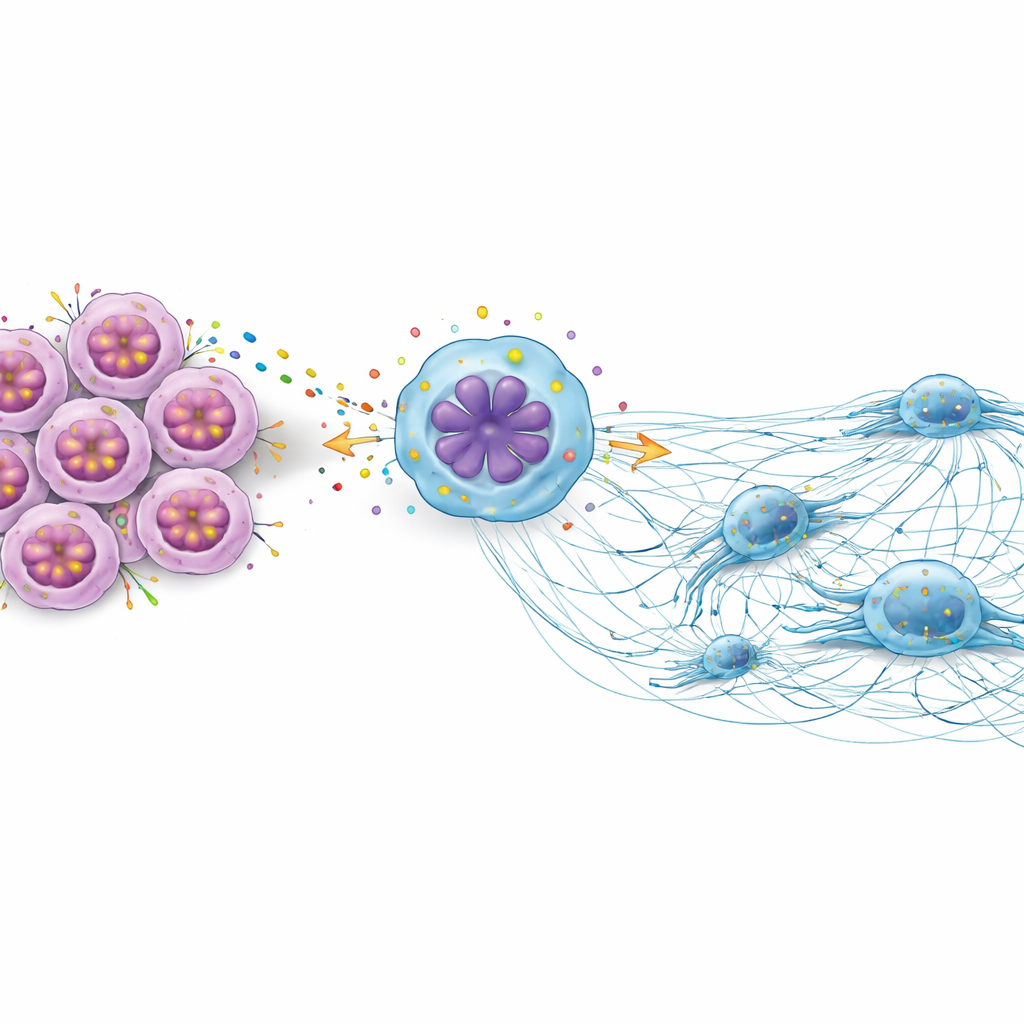
Immunzell‑Netze, die Krebs die Ausbreitung erleichtern
Die Studie richtete den Blick dann auf einen weniger bekannten Akteur im Krebsgeschehen: neutrophile extrazelluläre Fallen (NETs). Dabei handelt es sich um klebrige, netzartige Strukturen aus DNA und Proteinen, die bestimmte weiße Blutkörperchen freisetzen. Zwar helfen NETs normalerweise, eindringende Mikroben einzufangen, sie können aber auch Spuren schaffen, entlang derer Krebszellen migrieren. In Zellkulturversuchen wurden Schilddrüsenkrebszellen, die NETs ausgesetzt waren, noch beweglicher und invasiver. Wurden jedoch DUSP6 oder IL‑8 herunterreguliert, war dieser NET‑vermittelte Zuwachs an Bewegung und Invasion deutlich reduziert. Mit anderen Worten: DUSP6 und IL‑8 machten Tumorzellen empfänglicher für diese schädlichen Netze.
Wie Tumorsignale benachbarte Immunzellen umformen
Um die Ereigniskette weiter zu klären, untersuchten die Forschenden Neutrophile, also jene Immunzellen, die NETs bilden. Erhöhte man DUSP6 in diesen Zellen, stiegen Marker der NET‑Bildung; reduzierte man DUSP6 oder blockierte IL‑8, sanken diese Marker. Zusätzliche Färbeexperimente bestätigten, dass DNA‑basierte Netze und zugehörige Proteine vermehrt vorhanden waren, wenn DUSP6 hoch und die IL‑8‑Signalgebung intakt war. Diese Befunde deuten auf eine Schleife hin, in der Schilddrüsenkrebszellen mit erhöhtem DUSP6 mehr IL‑8 produzieren, was wiederum Neutrophile zur Bildung zusätzlicher NETs anregt — und so eine physische und chemische Umgebung schafft, die Krebszellen bei Bewegung und Invasion unterstützt.
Verlangsamtes Tumorwachstum im Tiermodell
Das Team prüfte die praktische Bedeutung dieses Signalsystems in Mäusen. Sie setzten Schilddrüsenkrebszellen unter die Haut von Mäusen und nutzten genetische Werkzeuge, um DUSP6 in einigen Tumoren zu reduzieren. Tumoren mit geringerem DUSP6 wuchsen langsamer und blieben am Ende kleiner und leichter als die in Kontrolltieren. Unter dem Mikroskop waren diese Tumoren weniger dicht mit Krebszellen besiedelt und zeigten Proteinmuster, die einem weniger invasiven Zustand entsprachen. Tumorgewebe dieser Mäuse wies zudem geringere Mengen an IL‑8 und NET‑bezogenen Markern auf — ein Befund, der die Ergebnisse aus Zellkulturstudien widerspiegelt und die Idee stützt, dass DUSP6 eine pro‑metastatische Umgebung fördert.
Was das für die zukünftige Behandlung von Schilddrüsenkrebs bedeutet
Kurz gefasst zeigt die Studie, dass ein intrazellulärer Schalter in Schilddrüsenkrebszellen, DUSP6, Tumoren dabei hilft, sich auszubreiten, indem er IL‑8 hochreguliert. IL‑8 veranlasst Immunzellen, klebrige NETs zu bilden, die Krebszellen ausnutzen können. Die Blockade von DUSP6, IL‑8 oder der NET‑Bildung unterbrach diese Kette und verlangsamte das Tumorwachstum in den Experimenten. Zwar sind weitere Untersuchungen nötig, darunter ausführlichere Tierstudien und letztlich klinische Studien, doch heben diese Ergebnisse ein vielversprechendes Trio von Angriffspunkten hervor, das eines Tages helfen könnte, aggressive Schilddrüsenkarzinome an der Invasion und Metastasierung zu hindern.
Zitation: Xiao, W., Luo, L., Yang, Y. et al. DUSP6 promotes motility, invasion, and tumorigenicity of thyroid cancer cells via IL8-induced neutrophil extracellular traps. Sci Rep 16, 12575 (2026). https://doi.org/10.1038/s41598-026-43233-0
Schlüsselwörter: Schilddrüsenkrebs, DUSP6, Interleukin-8, neutrophile extrazelluläre Fallen, Metastasen