Clear Sky Science · zh
氧化锌纳米粒子的物化学优化通过抑制RmpA、fnbA、cna和LuxS基因表达增强其抗菌和抗癌活性
微小颗粒,大潜力
抗生素耐药性感染和癌症是当今最令人担忧的两大健康威胁。本研究探讨一种材料——纳米级的氧化锌颗粒——是否能同时应对这两类问题。通过把氧化锌缩小到纳米尺度并精细调控其物理和化学性质,研究者表明这些颗粒不仅能杀灭或抑制有害微生物和癌细胞,还能在极低剂量下悄然关闭关键的细菌“攻击”程序。
超级细菌为何难以对付
许多危险细菌已经学会抵御多种抗生素,使常见感染变成危及生命的事件。这些微生物之所以致病,不仅因为它们生长,还因为它们使用特殊工具:帮助黏附组织的表面钩子、称为生物膜的保护性黏液层,以及用于协调攻击的化学“通讯”系统。研究团队关注了四个此类遗传控制开关——rmpA、fnbA、cna 和 luxS——它们帮助细菌黏附、形成生物膜并进行群体通讯。如果能在不必直接杀死细菌的情况下抑制这些开关,就有可能让感染变得更温和、更易控制,同时对微生物施加更少的进化压力,从而减缓耐药性的出现。
制备与表征微小颗粒
研究者使用一种简单的水相湿法配方合成氧化锌纳米粒子。含锌的盐和碳酸盐被温和混合并加热形成中间化合物,然后煅烧得到近似球形、直径约30纳米的氧化锌颗粒。他们使用电子显微镜、光吸收测量和液相电荷分析等常规实验室手段确认了颗粒的尺寸、形状、晶体结构和表面电荷。颗粒在悬浮液中稳定,短时间超声处理能使其分散得更均匀且略微变小,这一点很重要,因为尺寸和表面电荷强烈影响纳米颗粒与细胞的相互作用。
抑制病菌与肿瘤
当团队将一组与医院相关的细菌暴露于这些氧化锌纳米粒子时,观察到明显的生长抑制区,特别是在大肠埃希菌(Escherichia coli)上。抑制生长所需的最低量因物种而异,某些细菌在相对低浓度下即被抑制,而像金黄色葡萄球菌(Staphylococcus aureus)这样的细菌则需要更高剂量。这反映了细胞壁结构、保护层和内在防御系统的差异。研究者还在两种人类癌细胞系上进行了测试:乳腺组织来源的MCF-7和肝组织来源的HepG2。两种细胞系的存活率随着纳米粒子浓度增加而显著下降,乳腺癌细胞的半数致死浓度约为79微克/毫升,肝癌细胞约为151微克/毫升。显微观察显示受处理的细胞变圆、收缩并失去完整的细胞膜——这些是细胞应激和程序性细胞死亡的可见特征,可能由细胞内的氧化损伤驱动。
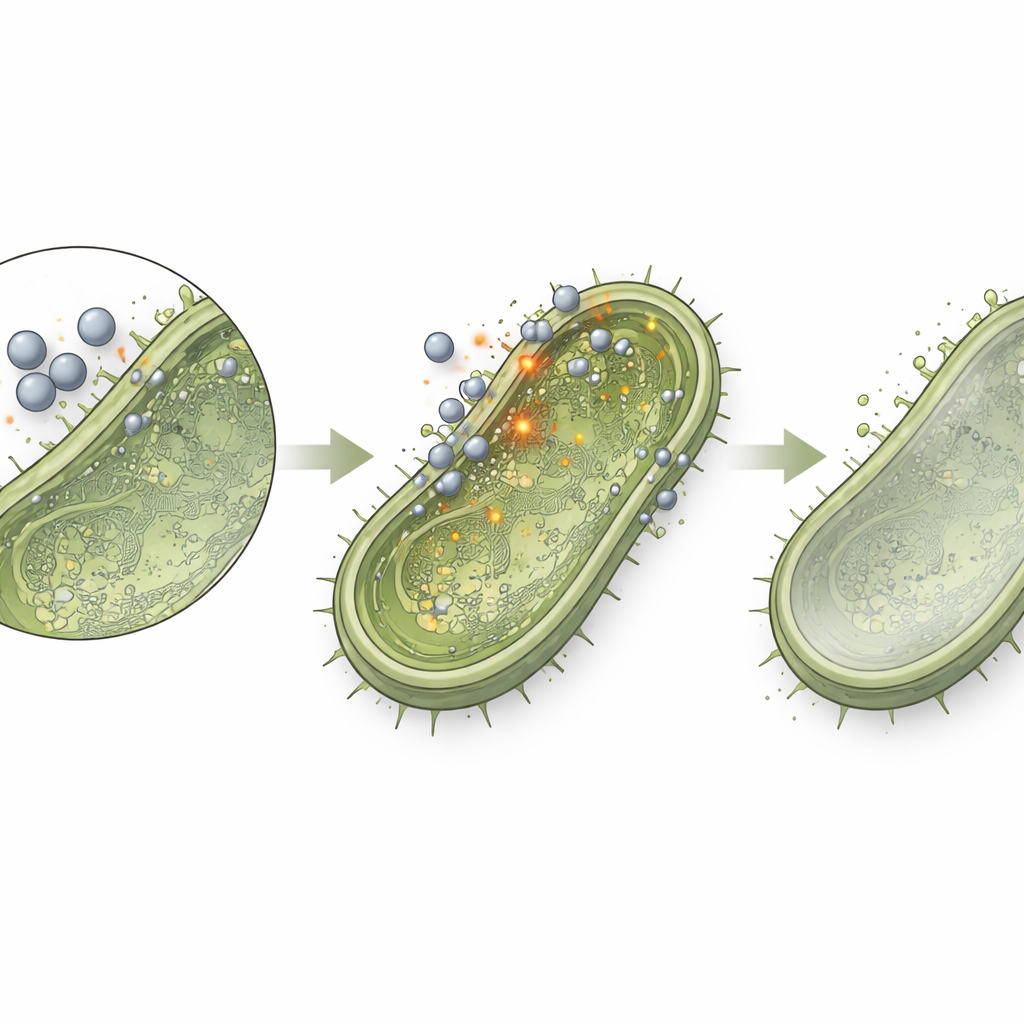
悄然解除细菌武装
研究中最有趣的部分或许是,研究者在故意使用低于完全抑菌水平的氧化锌纳米粒子浓度时的观察。在这些“亚抑制浓度(sub-MIC)”下,细菌仍然存活,但持续接触到温和的纳米粒子。通过测量特定基因的表达活性,团队发现关键的毒力和通讯程序被下调。与黏附和组织侵袭相关的三种基因——克雷伯氏肺炎菌(Klebsiella pneumoniae)中的 rmpA、某些葡萄球菌中的 fnbA 以及金黄色葡萄球菌中的 cna——表达降至约正常水平的60%。作为群体行为和生物膜协调中枢的 luxS 基因表达降至约正常水平的80%。这意味着即使纳米粒子未直接杀死微生物,它们也能让微生物组织性下降、侵袭性减弱,从而更易被免疫系统和现有药物控制。
对未来治疗的潜在意义
综合来看,研究结果表明,经精心设计的氧化锌纳米粒子可能成为医学中一种灵活的新工具。在较高剂量时,它们可直接损伤并杀死多种危险细菌,并对癌细胞呈现明显的剂量依赖性毒性;在较低的非致死剂量时,它们更像分子层面的破坏者,削弱细菌毒力基因并扰乱使感染难以治疗的通讯系统。对于非专业读者而言,核心信息是:微小且设计良好的颗粒不仅可以被调控以攻击细胞,还能微妙地改变有害微生物的行为。这种双重作用——在必要时杀伤,在不需完全杀灭时解除武装——可能有助于延长现有抗生素的有效期,并为更温和、更具针对性的癌症与感染治疗开辟新途径。
引用: khedr, M., Emam, A.N., Dora, M.S. et al. Physicochemical optimization of zinc oxide nanoparticles enhances their antimicrobial and anticancer activities via RmpA, fnbA, cna, and LuxS gene expression suppression. Sci Rep 16, 11367 (2026). https://doi.org/10.1038/s41598-026-42733-3
关键词: 氧化锌纳米粒子, 抗生素耐药性, 纳米医学, 抗癌疗法, 细菌毒力