Clear Sky Science · ar
التحسين الفيزيائي-الكيميائي لجسيمات أكسيد الزنك النانوية يعزز أنشطتها المضادة للميكروبات والمضادة للسرطان عبر تثبيط تعبير الجينات RmpA وfnbA وcna وLuxS
جزيئات صغيرة، إمكانات كبيرة
تُعَدّ العدوى المقاومة للمضادات الحيوية والسرطان من أكبر التهديدات الصحية في عصرنا. تستقصي هذه الدراسة ما إذا كان مكوّن واحد — حبيبات دقيقة من أكسيد الزنك — قادرًا على معالجة المشكلتين معًا. عبر تقليص أكسيد الزنك إلى النطاق النانوي وضبط خصائصه الفيزيائية والكيميائية بعناية، يُظهر الباحثون أن هذه الجسيمات لا تقتصر فقط على قتل أو إبطاء الميكروبات والخلايا السرطانية الضارة، بل يمكنها أيضًا إيقاف برامج بكتيرية «هجومية» رئيسية بهدوء حتى عند جرعات منخفضة جدًا.
لماذا يصعب علاج البكتيريا الخارقة
تعلمت العديد من البكتيريا الخطرة مقاومة عدة مضادات حيوية، ما يحول العدوى الروتينية إلى حالات تهدد الحياة. لا تتسبب هذه الميكروبات بالضرر لمجرد نموها، بل لأنها تستخدم أدوات خاصة: خطاطيف سطحيّة تساعدها على الالتصاق بالأنسجة، وطبقات لزجة واقية تُسمى الأغشية الحيوية، وأنظمة «دردشة» كيميائية تنسق هجماتها. ركز الفريق على أربعة مفاتيح جينية للتحكم — rmpA وfnbA وcna وluxS — التي تساعد البكتيريا على الالتصاق، وتكوين الأغشية الحيوية، والتواصل. إذا أمكن خفض نشاط هذه المفاتيح دون القضاء على البكتيريا بالضرورة، فقد يصبح بالإمكان تخفيف شدة العدوى وجعلها أسهل في السيطرة مع فرض ضغط تطوري أقل على الميكروبات لتطوير مقاومة.
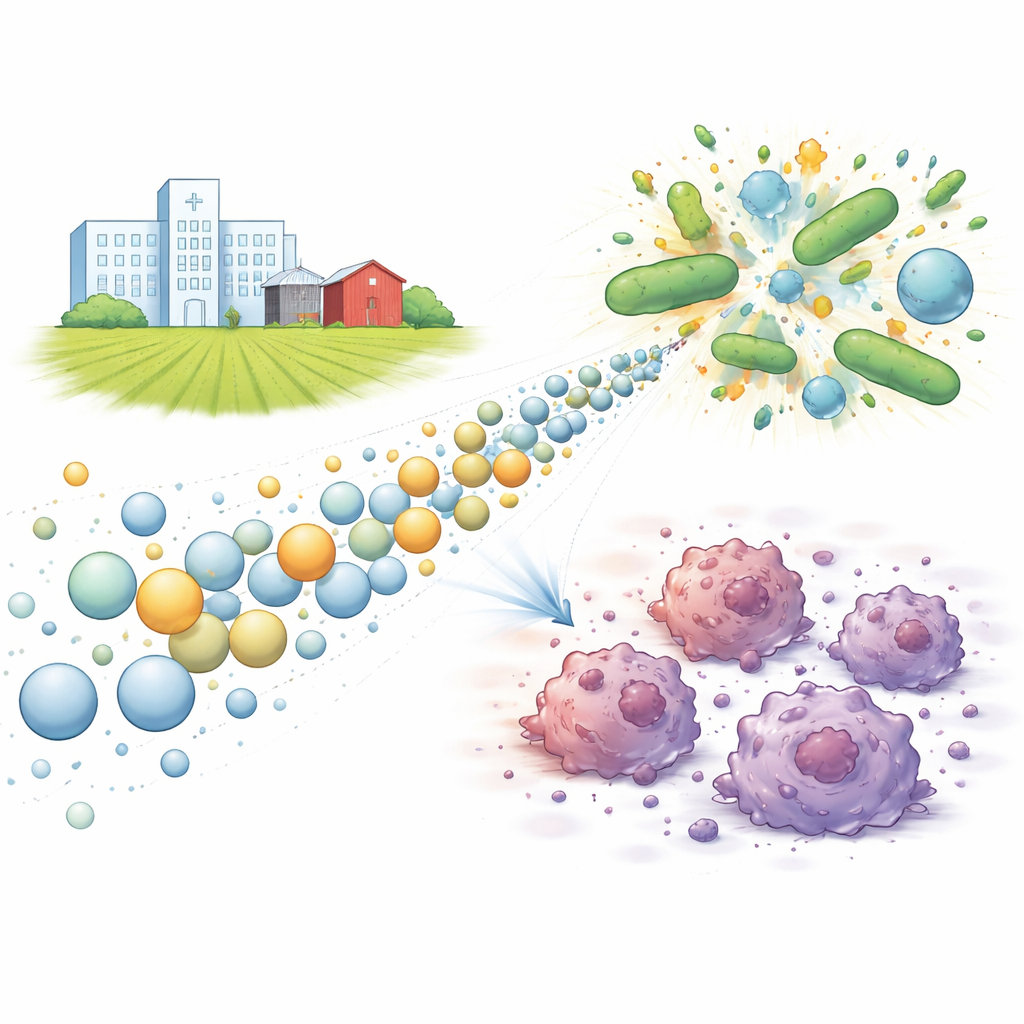
بناء واختبار الحبيبات الدقيقة
صنع الباحثون جسيمات أكسيد الزنك النانوية باستخدام وصفة كيميائية رطبة بسيطة في الماء. تم خلط ملح يحوي الزنك مع ملح كربونات بلطف وتسخينه لتشكيل مركب وسيط، ثم خبزه للحصول على أكسيد الزنك على شكل جسيمات دقيقة شبه كروية يبلغ قطرها نحو 30 مليار جزء من المتر. أكدوا الحجم والشكل والبنية البلورية والشحنة السطحية لهذه الجسيمات باستخدام أدوات مخبرية معيارية مثل المجهر الإلكتروني وقياسات امتصاص الضوء وتحليل الشحنة الكهربائية في السائل. كانت الجسيمات مستقرة في التعليق، ومع المعالجة بالموجات فوق الصوتية لفترة وجيزة أصبحت أكثر تجانسًا وأصغر قليلًا—عامل مهم لأن الحجم والشحنة السطحية يؤثران بشدة في كيفية تفاعل الجسيمات النانوية مع الخلايا.
إيقاف الجراثيم والأورام
عندما عرض الفريق مجموعة من البكتيريا المرتبطة بالمستشفيات لهذه الجسيمات، لاحظوا مناطق واضحة توقفت فيها النمو، خاصة بالنسبة للإشريكية القولونية. تنوعت الكميات الدنيا اللازمة لوقف النمو حسب النوع، إذ استسلمت بعض البكتيريا عند تركيزات منخفضة نسبيًا بينما احتاجت أخرى، مثل المكورات العنقودية الذهبية، إلى جرعات أعلى. يعكس ذلك اختلافات في بنية جدار الخلية والطبقات الواقية والأنظمة الدفاعية الداخلية. كما اختُبرت الجسيمات ضد سطرين خلويين بشريين لسرطان: أحدهما من نسيج الثدي (MCF-7) والآخر من نسيج الكبد (HepG2). في كلتا الحالتين انخفضت بقاء الخلايا السرطانية بشكل حاد مع زيادة تركيز الجسيمات النانوية، حيث مات نصف الخلايا تقريبًا عند نحو 79 ميكروغرامًا لكل مليلتر لخلايا سرطان الثدي وحوالي 151 ميكروغرامًا لكل مليلتر لخلايا سرطان الكبد. أظهرت الميكروسكوبيّة خلايا معالجة تصبح مستديرة ومنكمشة وتفقد أغشيتها السليمة — علامات بصرية على الإجهاد والموت الخلوي المبرمج، على الأرجح ناجمة عن تلف تأكسدي داخل الخلايا.
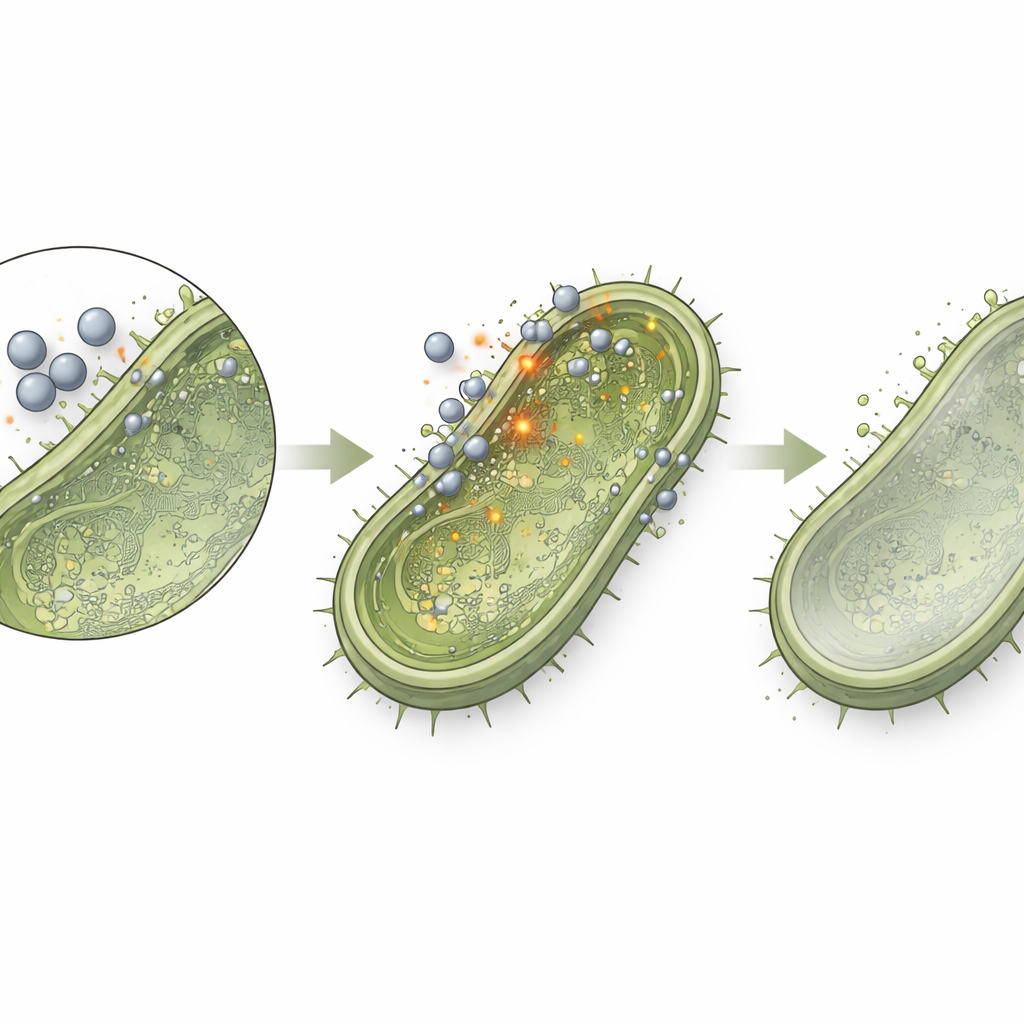
تفكيك البكتيريا بهدوء
ربما كانت أكثر أجزاء الدراسة إثارة عندما استخدم الباحثون عمدًا جسيمات أكسيد الزنك بتركيزات لا تكفي لإيقاف النمو البكتيري تمامًا. عند هذه الجرعات «تحت حد التركيز المثبط الأدنى» (sub-MIC)، بقيت البكتيريا حية لكن تعرّضت لوجود مستمر وهادئ للجسيمات. بقياس نشاط جينات محددة، وجد الفريق أن برامج الضراوة والتواصل الأساسية خفتت. تراجعت ثلاث جينات مرتبطة باللزوجة وغزو الأنسجة — rmpA في Klebsiella pneumoniae، وfnbA في بعض أنواع المكورات، وcna في Staphylococcus aureus — إلى نحو 60% من تعبيرها الطبيعي. أما جين luxS، اللاعب المركزي في نظام الإشارات الكيميائية الذي تستخدمه البكتيريا لتنسيق السلوك الجماعي وتكوين الأغشية الحيوية، فقد انخفض إلى نحو 80% من الوضع الطبيعي. هذا يعني أنه حتى عندما لا تقتل الجسيمات الميكروبات مباشرة، فإنها تجعلها أقل تنظيمًا وأقل غزوًا، وربما أسهل على الجهاز المناعي والأدوية الحالية للتعامل معها.
ماذا قد يعني ذلك للعلاجات المستقبلية
تشير النتائج مجتمعة إلى أن جسيمات أكسيد الزنك المصممة بعناية قد تكون أداة مرنة جديدة في الطب. عند جرعات أعلى، يمكنها إحداث ضرر مباشر وقتل مجموعة من البكتيريا الخطرة وتظهر سمية قوية تعتمد على الجرعة ضد الخلايا السرطانية. عند جرعات أقل وغير مميتة، تتصرف أكثر كس saboteurs جزيئية — تضعف جينات الضراوة البكتيرية وتزعزع أنظمة التواصل التي تجعل العدوى صعبة المعالجة. للقراء غير المتخصصين، الرسالة الأساسية هي أن جزيئات دقيقة ومصممة جيدًا يمكن ضبطها ليس فقط لمهاجمة الخلايا، بل لإعادة تشكيل سلوك الميكروبات الضارة بشكل لطيف. قد تساعد هذه الفاعلية المزدوجة — القتل عند الحاجة والتشتيت أو التعطيل عندما لا يكون القتل الكامل مطلوبًا — في إطالة عمر المضادات الحيوية الحالية وفتح طرق جديدة لعلاجات أكثر لطفًا واستهدافًا للسرطان والعدوى.
الاستشهاد: khedr, M., Emam, A.N., Dora, M.S. et al. Physicochemical optimization of zinc oxide nanoparticles enhances their antimicrobial and anticancer activities via RmpA, fnbA, cna, and LuxS gene expression suppression. Sci Rep 16, 11367 (2026). https://doi.org/10.1038/s41598-026-42733-3
الكلمات المفتاحية: جسيمات أكسيد الزنك النانوية, مقاومة المضادات الحيوية, الطب النانوي, علاج السرطان, الضراوة البكتيرية