Clear Sky Science · zh
通过冷适应获得心脏保护的 JAK/STAT 通路因果相关性
为何寒冷对心脏可能不像我们想的那样残酷
大多数人把寒冷天气视为对心脏健康的威胁,这也有道理:突如其来的寒冷会在易感人群中诱发心脏病发作。但这项研究探讨了另一面:当冷暴露是温和且持续的,机体可以发生适应性改变,实际上使心脏对心肌梗死的损伤更具抵抗力。研究者旨在揭示心肌细胞内的这种机制,聚焦于一种名为 JAK/STAT3 的信号通路,该通路将免疫信号、能量代谢与细胞存活连接起来。
用温和的寒冷“训练”机体
为探究这一问题,科学家将大鼠在五周内逐步适应约 9 °C(48 °F)的寒冷但不结冰的环境——足以激活防御反应,但不会引起颤抖或明显应激。对照组大鼠则维持室温。随后所有动物接受了实验室控制下的心肌梗死模型:阻断并随后恢复部分心肌的血流,以模拟人类冠状动脉突然阻塞后再通治疗的情形。这样团队便能测量心肌坏死的面积以及心脏在术后泵功能的表现。他们还在部分动物中使用了一种阻断 JAK2 的药物,以检验该通路是否真是冷适应益处的必要环节。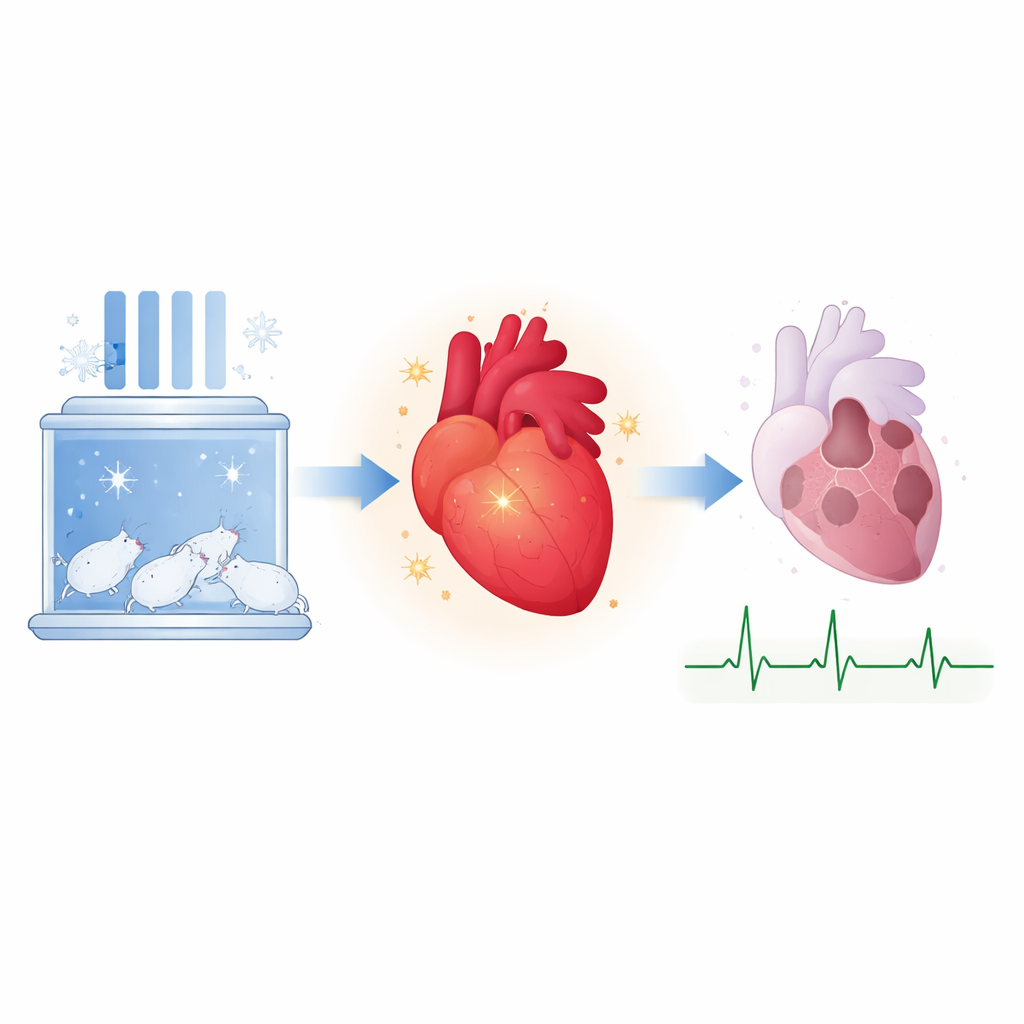
心脏“能量库”内的保护性开关
经冷适应的大鼠表现出显著更好的结局。与室温对照组相比,它们在模拟心梗期间的心肌坏死面积不到一半。保护的一个关键特征是线粒体更为健康——线粒体是细胞内产生能量的微小“动力站”。在线粒体在应激下失效时,会开启称为通透性转换孔的结构,这可触发细胞死亡。在冷适应心脏中,这些孔在遭遇钙这一应激信号时打开得更慢,表明线粒体更为稳健。但若在冷暴露结束前给予阻断 JAK2 的药物 AG490,这种线粒体韧性就会消失,心肌梗死的损伤面积回升接近对照水平。这一发现将冷诱导的保护性效应坚固地归因于活跃的 JAK/STAT3 信号通路。
缓和损伤与细胞死亡的信号
进一步研究中,科研人员观察了 STAT3 及相关蛋白在心肌细胞内的定位变化。正常心脏中,大量 STAT3 存在于线粒体和细胞膜。冷适应后,STAT3 出现重新分布:总量向细胞表面偏移,线粒体内相对减少,而与细胞核相关的特定活化形式在某些区室中有所下降。尽管这些变化较为微妙,线粒体内的 STAT3 活性似乎仍被保留,支持其非基因组作用——直接稳定能量产生并维持死亡触发孔关闭——对保护至关重要。同一时间,冷适应降低了与应激驱动细胞死亡相关的 p38 MAPK 水平,同时并未引起心脏肥大或升高血压。当 JAK2 被阻断时,p38 水平再次上升,凋亡(程序性细胞死亡)标志物增加,这表明冷方案通常通过该通路抑制有害的死亡信号。
有益而非有害的免疫讯号
研究还考察了心脏内的免疫化学信使。冷适应提高了白细胞介素-6(IL-6)的水平,IL-6 常与炎症相关,但也以能够保护性地激活 STAT3 而闻名。有趣的是,经典的促炎信号如肿瘤坏死因子α(TNF-α)和白细胞介素-1β 并未因为单纯冷暴露而上升,且在冷适应动物中当 JAK2 通路被阻断时这些促炎信号反而倾向于被抑制。这一模式表明,适度且控制良好的寒冷并不引发心脏炎性反应;相反,它似乎微调免疫讯号,使 IL-6 支持存活通路而不释放有害的炎症反应。总体而言,冷适应产生了一种与适应而非损伤相一致的平衡免疫谱。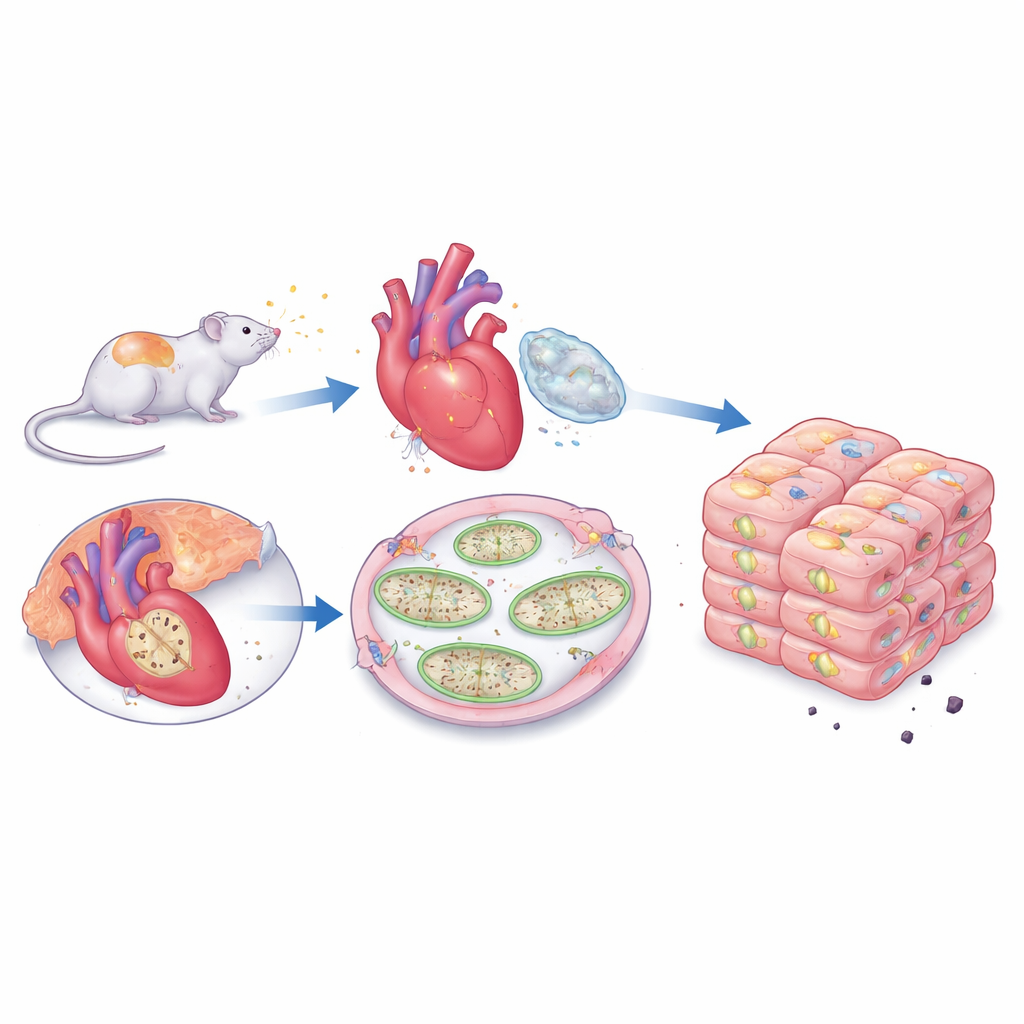
对未来心脏护理的可能启示
简言之,这项工作表明,长期生活在稳定、适度凉爽的环境中可以“训练”心脏更好地抵御未来的心肌梗死,而 JAK2/STAT3 信号轴是这一训练方案中的关键部分。通过增强线粒体功能并抑制有害的细胞死亡及炎性信号,冷适应缩小了血流中断与恢复时心肌坏死的范围。尽管长期冷暴露并非对患者的实际治疗方案,但理解其如何招募 JAK/STAT3 及相关通路,可能会启发开发新药或温和的降温策略来模拟其保护性效应——在危险来临之前增强心脏的韧性。
引用: Kasik, P., Galatik, F., Matous, P. et al. Causal relevance of the JAK/STAT pathway for cardioprotection via cold acclimation. Sci Rep 16, 12124 (2026). https://doi.org/10.1038/s41598-026-40532-4
关键词: 冷适应, 心脏保护, JAK2 STAT3, 线粒体, 缺血再灌注