Clear Sky Science · de
Kausale Relevanz des JAK/STAT-Signalwegs für den Herzschutz durch Kälteakklimatisation
Warum Kälte fürs Herz freundlicher sein kann, als wir denken
Die meisten von uns betrachten Kälte als Bedrohung für die Herzgesundheit — mit gutem Grund: plötzliche Kälteeinbrüche können bei gefährdeten Personen Herzinfarkte auslösen. Diese Studie beleuchtet jedoch die andere Seite der Medaille. Bei sanfter und anhaltender Kälteeinwirkung kann sich der Körper anpassen und das Herz widerstandsfähiger gegen Schäden durch einen Herzinfarkt machen. Die Forschenden wollten herausfinden, wie das in den Herzmuskelzellen geschieht, und richteten ihren Blick auf einen Signalweg namens JAK/STAT3, der Immunbotschaften, Energieproduktion und Zellüberleben verknüpft.
Den Körper durch sanfte Kälte trainieren
Um diese Frage zu untersuchen, gewöhnten die Wissenschaftler Ratten über fünf Wochen schrittweise an eine kühle, aber nicht gefrierende Umgebung von etwa 9 °C — kalt genug, um Schutzmechanismen zu aktivieren, aber nicht so streng, dass es zu Zittern oder Stress kommt. Andere Ratten blieben bei Raumtemperatur. Anschließend wurden alle Tiere einem kontrollierten Herzinfarkt im Labor unterzogen: Der Blutfluss zu einem Herzabschnitt wurde für eine Weile unterbrochen und dann wiederhergestellt, was dem entspricht, was bei Menschen mit einer plötzlichen Koronarverschlussereignis und anschließender Behandlung passiert. So konnte das Team messen, wie viel Herzgewebe abstirbt und wie gut das Herz danach pumpt. Einige Tiere erhielten außerdem ein Medikament, das JAK2 blockiert — das Enzym, das STAT3 aktiviert — um zu prüfen, ob dieser Weg tatsächlich für die Vorteile der Kälteakklimatisation erforderlich ist. 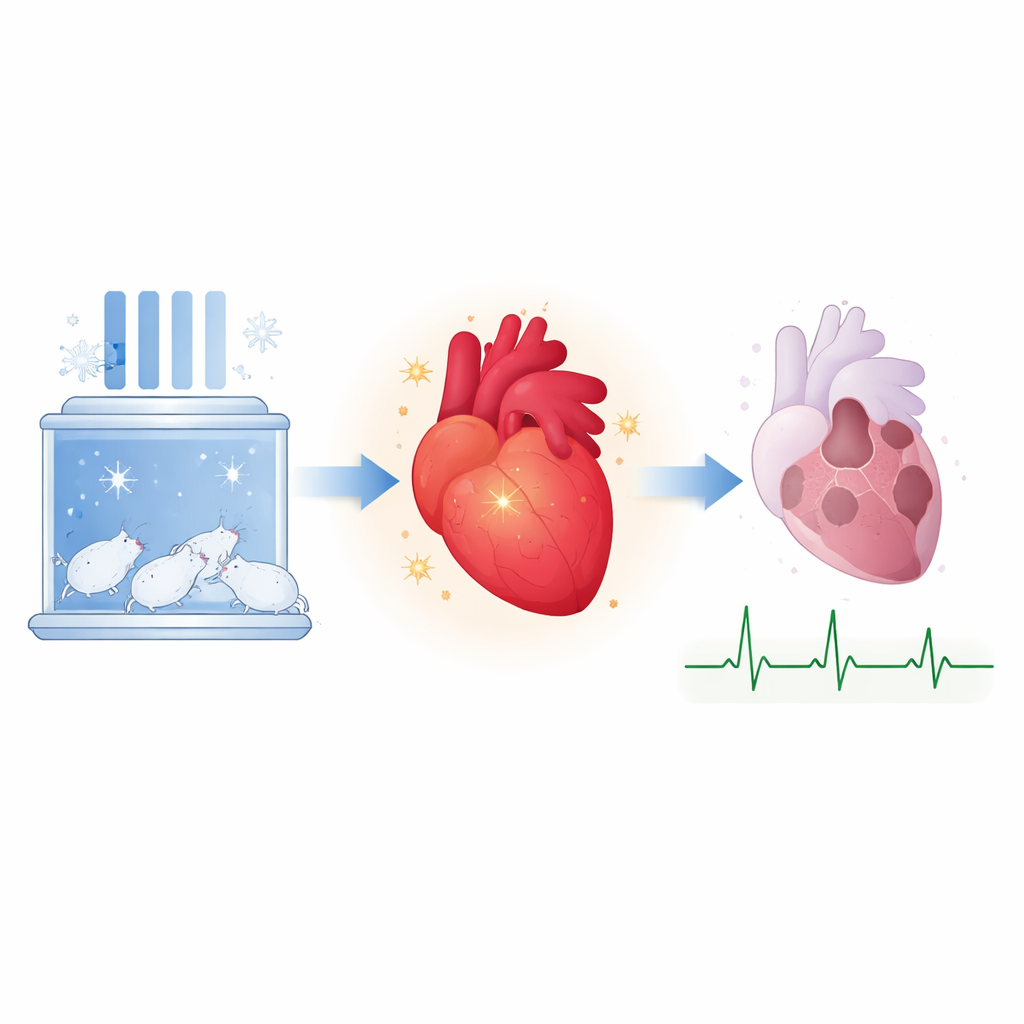
Ein schützender Schalter in den Kraftwerken des Herzens
Die kälteakklimatisierten Ratten schnitten auffallend besser ab. Im Vergleich zu den Kontrollen bei Raumtemperatur verlor ihr Herz weniger als die Hälfte des Gewebes während des simulierten Herzinfarkts. Ein zentrales Merkmal dieses Schutzes waren gesündere Mitochondrien — die winzigen Kraftwerke in den Zellen, die Energie erzeugen. Wenn Mitochondrien unter Stress versagen, öffnen sie eine Struktur namens Permeabilitätsübergangspore, die Zelltod auslösen kann. In den kälteakklimatisierten Herzen öffneten sich diese Poren bei Herausforderung mit Calcium, einem Stresssignal, langsamer, was auf robustere Mitochondrien hindeutet. Wurde jedoch das JAK2-blockierende Medikament AG490 kurz vor Ende der Kälteeinwirkung verabreicht, verschwand diese mitochondriale Widerstandskraft, und die Größe der Infarktverletzung stieg wieder auf Kontrollniveau. Das verknüpfte den kälteinduzierten Schutz eindeutig mit einem aktiven JAK/STAT3-Signalweg.
Signale, die Schäden und Zelltod dämpfen
Bei tiefergehenden Untersuchungen betrachteten die Forschenden, wie STAT3 und verwandte Proteine sich innerhalb der Herzmuskelzellen verteilten. In normalen Herzen befindet sich viel STAT3 in Mitochondrien und in Zellmembranen. Nach der Kälteakklimatisation zeigte sich eine Umverteilung: Gesamt-STAT3 verlagerte sich stärker zur Zelloberfläche und weniger in die Mitochondrien, während eine spezifische aktivierte Form, die mit dem Zellkern assoziiert ist, in bestimmten Kompartimenten abnahm. Trotz dieser subtilen Veränderungen schien die mitochondriale STAT3-Aktivität erhalten zu bleiben, was die Idee stützt, dass seine nicht-genetische Rolle — die direkte Stabilisierung der Energieproduktion und das Schließen der todauslösenden Poren — für den Schutz am wichtigsten ist. Gleichzeitig senkte die Kälteakklimatisation die Spiegel von p38 MAPK, einem Protein, das mit stressbedingtem Zelltod verknüpft ist, ohne dass es zu Herzvergrößerung oder Blutdruckanstieg kam. Wurde JAK2 blockiert, stiegen die p38-Spiegel wieder an und Marker für Apoptose, also programmierten Zelltod, nahmen zu, was darauf hindeutet, dass das Kälteprogramm normalerweise schädliche Todes‑Signale über diesen Weg dämpft.
Immunbotschaften, die helfen statt schaden
Die Studie untersuchte außerdem Immunbotenstoffe im Herzen. Die Kälteakklimatisation erhöhte die Spiegel von Interleukin‑6 (IL‑6), einem Zytokin, das oft mit Entzündung assoziiert wird, aber auch dafür bekannt ist, STAT3 auf eine protektive Weise zu aktivieren. Interessanterweise stiegen klassische proinflammatorische Signale wie Tumornekrosefaktor alpha (TNF‑α) und Interleukin‑1β nicht allein durch die Kälte und tendierten sogar dazu, bei kälteakklimatisierten Tieren gedämpft zu sein, wenn der JAK2‑Weg blockiert wurde. Dieses Muster legt nahe, dass moderate, kontrollierte Kälte das Herz nicht entzündet; vielmehr scheint sie Immunsignale so zu justieren, dass IL‑6 Überlebenswege unterstützt, ohne schädliche Entzündungen loszutreten. Insgesamt erzeugte die Kälteakklimatisation ein ausgewogenes Immunprofil, das eher zu Anpassung als zu Verletzung passt. 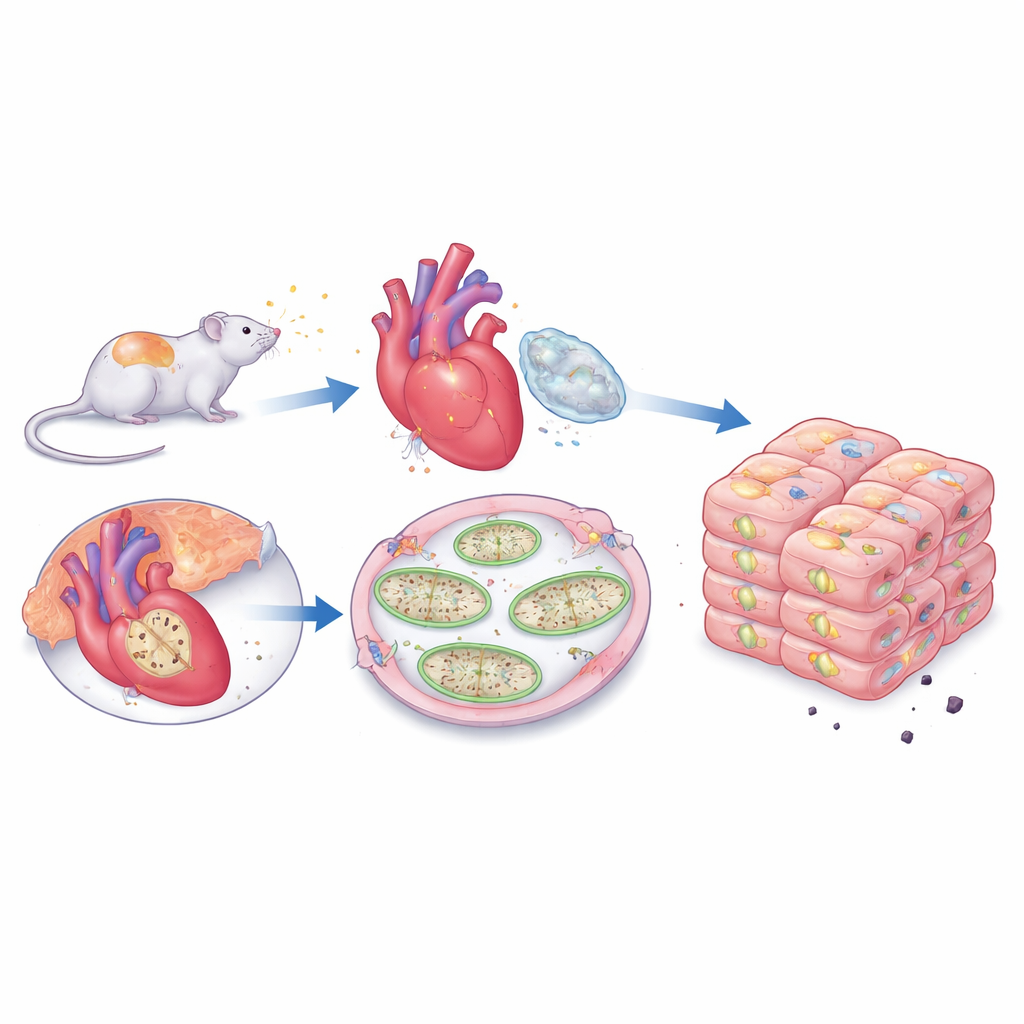
Was das für die künftige Herzmedizin bedeuten könnte
Einfach gesagt zeigt diese Arbeit, dass das Leben in einer gleichmäßig, mäßig kühlen Umgebung das Herz „trainieren“ kann, einem zukünftigen Herzinfarkt besser zu widerstehen, und dass die JAK2/STAT3‑Signalachse ein entscheidender Teil dieses Trainingsprogramms ist. Durch die Stärkung der Mitochondrien und die Herunterregulierung schädlicher Zell‑Todes‑ und Entzündungssignale verkleinert die Kälteakklimatisation den Bereich des Herzens, der abstirbt, wenn der Blutfluss unterbrochen und wiederhergestellt wird. Obwohl langfristige Kälteeinwirkung keine praktische Therapie für Patienten ist, könnte das Verständnis, wie sie JAK/STAT3 und verwandte Wege rekrutiert, zur Entwicklung neuer Medikamente oder sanfter Kühlstrategien inspirieren, die ihre schützenden Effekte nachahmen — und so das Herz widerstandsfähiger machen, bevor Probleme auftreten.
Zitation: Kasik, P., Galatik, F., Matous, P. et al. Causal relevance of the JAK/STAT pathway for cardioprotection via cold acclimation. Sci Rep 16, 12124 (2026). https://doi.org/10.1038/s41598-026-40532-4
Schlüsselwörter: Kälteakklimatisation, Herzschutz, JAK2 STAT3, Mitochondrien, Ischämie-Reperfusionsschaden