Clear Sky Science · zh
感染BmCPV的家蚕(Bombyx mori)中肠的基因组范围DNA甲基组和转录组分析
为什么蚕的肠道对我们很重要
家蚕看起来或许只是普通的养殖昆虫,但它们位于纺织、农业乃至生物医学产业的中心。当一种侵染肠道的病毒发生时,整批茧可能会遭到毁灭性损失。本研究探讨了这样一种病毒如何微妙地重塑蚕的遗传控制系统——不是通过改变DNA序列本身,而是通过调整其上的化学标记。理解这一隐蔽的调控层既有助于保护重要的经济昆虫,也有助于深化我们对病毒如何操纵宿主的更广泛认识。
一种具有巨大经济影响的肠道病毒
该研究聚焦于家蚕(Bombyx mori)及其常见病原体——家蚕细胞质多角体病毒(BmCPV)。这种双链RNA病毒专门攻击家蚕的中肠细胞——负责消化的器官。BmCPV的爆发会抑制幼虫生长并导致死亡,带来严重的经济损失。早期研究显示,BmCPV感染会改变许多蚕基因的开启或关闭状态,并改变包装DNA的蛋白质(即组蛋白)上的修饰。但另一类重要的DNA本身上的化学标记——DNA甲基化——在这一过程中如何发挥作用,仍然知之甚少。
DNA上的隐形代码
DNA甲基化是一种微小的化学变化:甲基基团被添加到DNA的特定位点,通常是在胞嘧啶(C)与鸟嘌呤(G)相邻的位置。尽管体积小,这一标记却能强烈影响邻近基因是否活跃。在许多动物中,DNA甲基化参与调控发育、沉默重复DNA,并微调基因的时间与空间表达。感染人类及其他脊椎动物的病毒已知会改变宿主的DNA甲基化以谋取优势。在昆虫中,整体甲基化水平较低,但早期工作提示蚕类病毒仍可能利用该机制。作者们着手在全基因组范围内检查BmCPV感染如何重塑家蚕中肠的甲基化图谱,以及这些变化如何与基因活性相关联。
全基因组读取化学标记
为此,研究团队感染了一个研究良好的蚕品系,并在感染后48小时和96小时取材收集中肠组织。他们还收集了相同年龄未感染幼虫的匹配肠样本。从这些组织中进行了两项大规模测量。首先,使用全基因组亚硫酸氢盐测序(whole-genome bisulfite sequencing),该方法可显示基因组中哪些胞嘧啶携带甲基。其次,使用RNA测序来测量在不同条件下哪些基因表达上升或下降。他们对数亿条DNA测序读段进行了严格过滤和比对,检查数据质量,并计算单个位点以及基因体、启动子和非翻译区等更广泛基因组区域的甲基化水平。
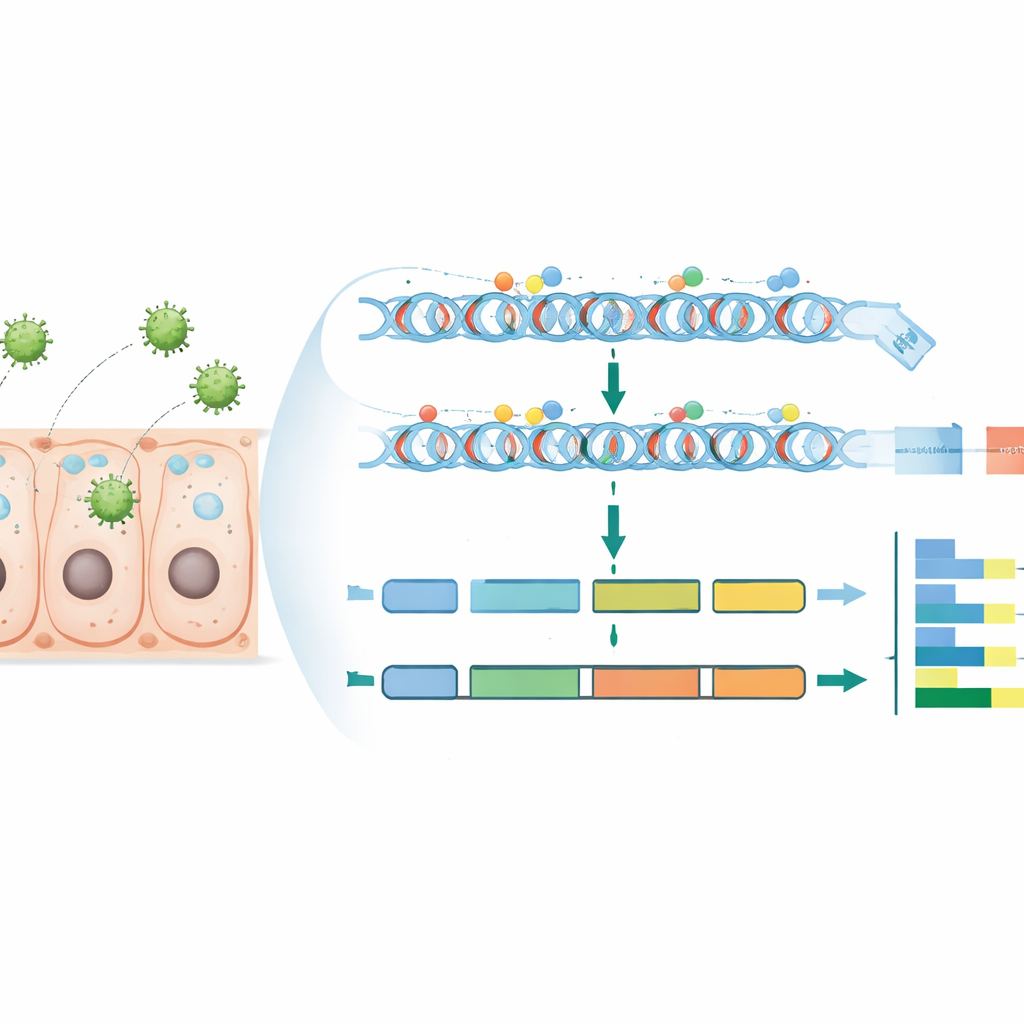
病毒调整控制的部位
研究者发现,与许多昆虫相似,家蚕的总体DNA甲基化水平较低,并且大多数甲基化位点存在于常见的CG(CpG)上下文中。在基因组内,甲基化并非均匀分布:它倾向于在与基因相关的区域(如外显子和非翻译区)更高,而在经典的CpG岛和重复DNA中较低。通过比较两个时间点的感染与未感染样本,他们定位了差异甲基化区(DMRs)——在感染期间甲基化增加或降低的DNA片段。随后,他们将这些区域与附近基因关联,尤其关注那些与基因上游的启动子区域重叠的DMR,因为这些启动子对基因的开启与关闭至关重要。最后,通过整合甲基化数据和RNA测序结果,他们识别出那些其表达变化与启动子甲基化变化密切相关的基因。
验证信号并共享数据
为确保这些全基因组模式是真实的,团队使用靶向方法验证了选定区域。他们采用甲基化特异性PCR确认选定位点的甲基化变化,并用定量PCR验证基因表达水平的变化。在每种情况下,聚焦检测的结果与大规模测序结果一致,从而增强了对数据集的信心。所有测序读段、处理后的甲基化轨迹以及甲基化位点和差异甲基化区的列表都已提交到公共数据库,为研究昆虫免疫、病毒—宿主相互作用或表观遗传调控的其他研究者提供了丰富资源。
这对蚕健康意味着什么
简而言之,这项研究表明,肠道病毒BmCPV不仅仅是入侵蚕细胞;它还与通过DNA甲基化对家蚕遗传控制旋钮进行微妙但广泛的重新调节相关联。特定基因在其起始区域附近获得或失去这些化学标记,而这些基因的表达也相应上升或下降。尽管这项工作尚不能直接转化为治疗方法,但它绘制了病毒似乎会触及的控制面板。从长远来看,这类洞见可能帮助育种者和生物技术专家设计更能抵抗感染的蚕系,并能揭示病毒如何操纵宿主表观遗传机制的共性原理。
引用: Qiu, Q., Liu, Z., Huang, Y. et al. Genome-scale DNA methylome and transcriptome profiling of midgut of Bombyx mori infected with BmCPV. Sci Data 13, 568 (2026). https://doi.org/10.1038/s41597-026-06922-z
关键词: 蚕病毒, DNA甲基化, 表观遗传学, 宿主–病毒相互作用, 家蚕中肠