Clear Sky Science · zh
雄激素在雄性胚胎后脑的活性推动致命性后颅窝A型室管膜瘤
为何男孩的大脑与一种罕见的儿童肿瘤有关联
有些脑肿瘤发生在极年幼的儿童身上,尽管经过手术和放疗,仍常常致命。其中最严重的一种位于大脑后部深处,称为后颅窝A型室管膜瘤。临床医生长期注意到这种癌症在男孩中更常见,且男孩的预后通常比女孩更差,但原因一直不明。本研究揭示了一个令人意外的罪魁:雄性性激素(即雄激素)在出生前和出生后不久作用于未成熟脑细胞。
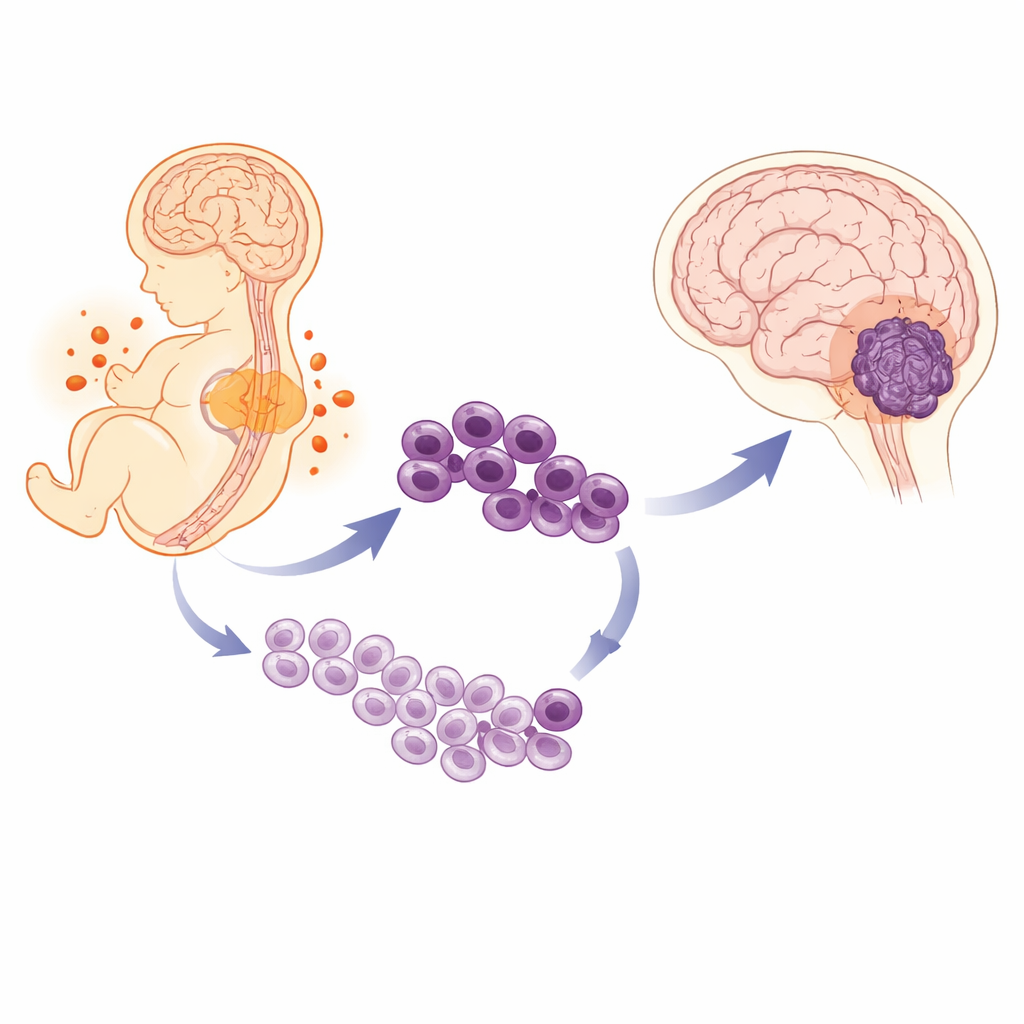
一种带有隐性偏差的儿童癌症
作者首先分析了大规模的患儿队列,证实男孩不仅发病率更高,长期生存率也比女孩差,即便接受相同的积极治疗。为了解肿瘤间的差异,研究团队采用单细胞RNA测序,这种技术能够逐个读取数千个细胞中哪些基因在表达。在男孩的肿瘤中,更大比例的细胞呈现出非常未分化的“类干”状态和行为,而女孩的肿瘤则含有更多表现出向专门化脑细胞分化进程较远的细胞。男孩肿瘤中原始细胞越富集,预后往往越差。
将肿瘤追溯到发育中的大脑
由于这些肿瘤出现在学步期儿童,并且与胎儿脑组织相似,研究人员怀疑正常脑发育中的某些因素可能为癌变奠定基础。他们构建了一个详尽的图谱,涵盖多发育阶段小鼠胚胎后脑的超过40万单细胞,并在采样时仔细平衡了雄性与雌性样本。该图谱展示了早期神经干细胞如何逐步转变为趋向形成神经胶质的祖细胞——即将成为支持性细胞(如星形胶质细胞)的细胞——然后再发展为成熟的胶质细胞。将雄性与雌性胚胎比较时,研究者发现雄性祖细胞,尤其在后脑区域,倾向于保持更为原始、快速分裂的状态,而雌性细胞则更明显地朝成熟终末型方向发展。
雄激素延缓关键脑细胞的成熟
为弄清这一差异是源于性染色体还是激素作用,研究团队使用了一种“四核心基因型”小鼠模型,该模型可以将有睾丸(从而产生雄激素)与XY染色体状态分离开来。跨不同基因型的比较表明,关键因素是睾丸及其产生的雄激素,而不是染色体性别。在有睾丸的胚胎中,后脑祖细胞显示出与干细胞维持、快速分裂和分化受阻相关的基因表达模式;而在有卵巢的胚胎中,同类细胞则更多表达与成熟和胶质发育相关的基因。在正常雄性胚胎中受雄激素增强的许多基因和调控开关,在男孩来源的最具侵袭性、类干的肿瘤细胞中也更为活跃,将肿瘤的行为直接关联回受激素塑形的发育程序。
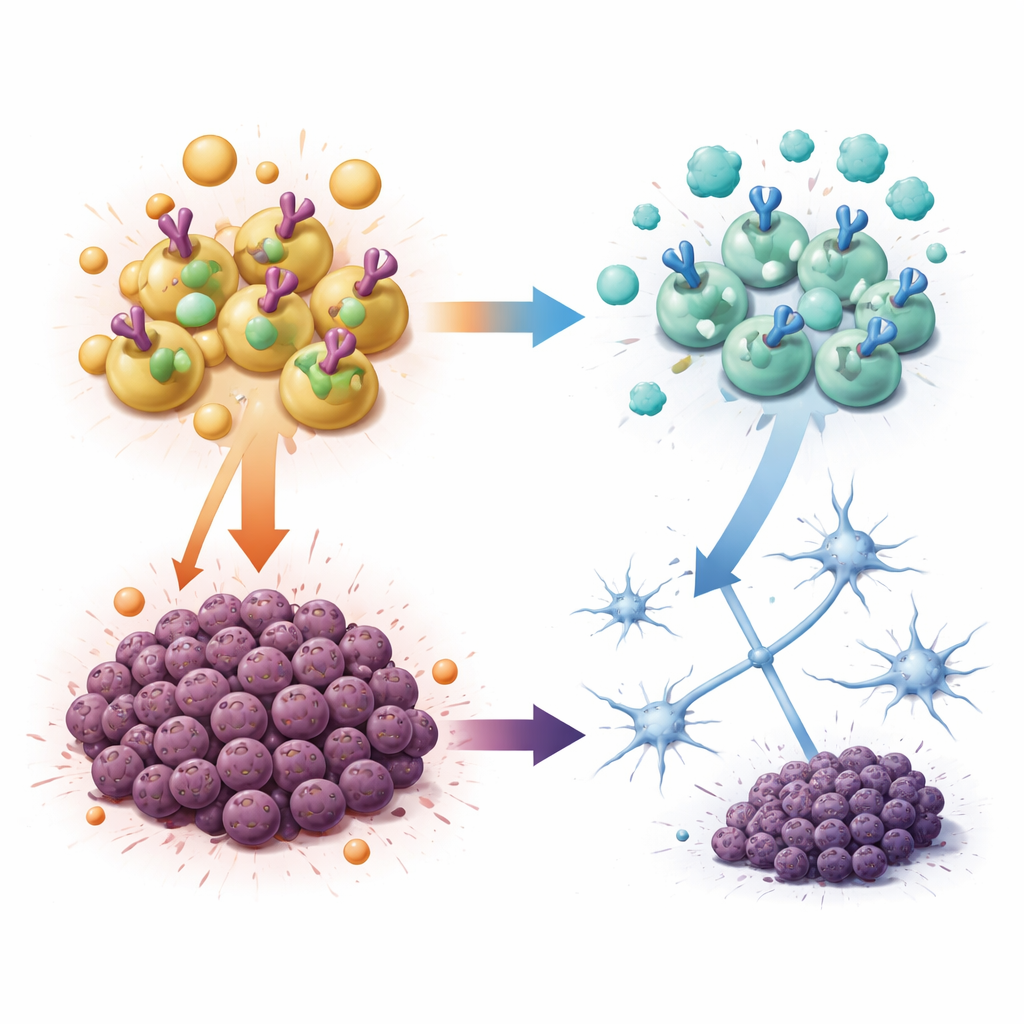
滋养肿瘤的激素——和使其饥饿的药物
研究人员随后探讨雄激素是否能直接改变肿瘤细胞的生长。在培养皿中,来自男孩和女孩的肿瘤细胞在暴露于睾酮或其强效同类二氢睾酮时复制和形成克隆的能力都增加,但暴露于雌激素或孕激素等女性激素时则没有这种反应。这些肿瘤细胞表达雄激素受体——一种在雄激素存在时进入细胞核并启动基因表达的蛋白。用已在前列腺癌中使用的药物恩扎卢胺阻断该受体,或用一种实验性化合物降解受体,均显著降低了这些肿瘤细胞的类干能力和增殖。重要的是,其他类型的儿童脑肿瘤细胞对雄激素或阻断雄激素的药物反应不大,提示这一脆弱性是特定于这种后脑肿瘤的。
这对儿童和未来疗法意味着什么
综上,这些发现支持一个简单却有力的观点:在发育中的后脑,雄激素使某些祖细胞在雄性中比雌性更长时间保持未成熟、快速增殖的状态。这个延长的时间窗增加了这些细胞发生恶性转化的机会,并且一旦转化,它们会保持高度类干和具侵袭性的特征,解释了为何男孩更易受这种肿瘤重创。因为塑造正常发育的相同激素信号也助长了癌症,所以针对雄激素信号的阻断疗法——经为婴幼儿谨慎调整——可能为这类毁灭性疾病提供首个有理性的靶向治疗方向。
引用: Zhang, J., Ong, W., Rasnitsyn, A. et al. Androgen activity in the male embryonic hindbrain drives lethal PFA ependymoma. Nature 652, 763–773 (2026). https://doi.org/10.1038/s41586-026-10264-6
关键词: 室管膜瘤, 雄激素信号, 儿童脑癌, 后脑发育, 癌症的性别差异