Clear Sky Science · de
Androgene Aktivität im embryonalen männlichen Hinterhirn treibt tödliches PFA-Ependymom an
Warum Jungenhirne und ein seltener Kindheitstumor zusammenhängen
Einige Hirntumoren treffen sehr junge Kinder und sind trotz Operation und Strahlentherapie oft tödlich. Einer der schlimmsten liegt tief hinten im Gehirn und heißt posterior fossa Typ A Ependymom. Ärztinnen und Ärzte beobachteten lange, dass dieser Krebs bei Jungen häufiger vorkommt und dass Jungen schlechtere Verläufe haben als Mädchen, aber die Ursache war unklar. Diese Studie deckt einen überraschenden Übeltäter auf: männliche Sexualhormone, also Androgene, die auf unreife Gehirnzellen vor und kurz nach der Geburt wirken.
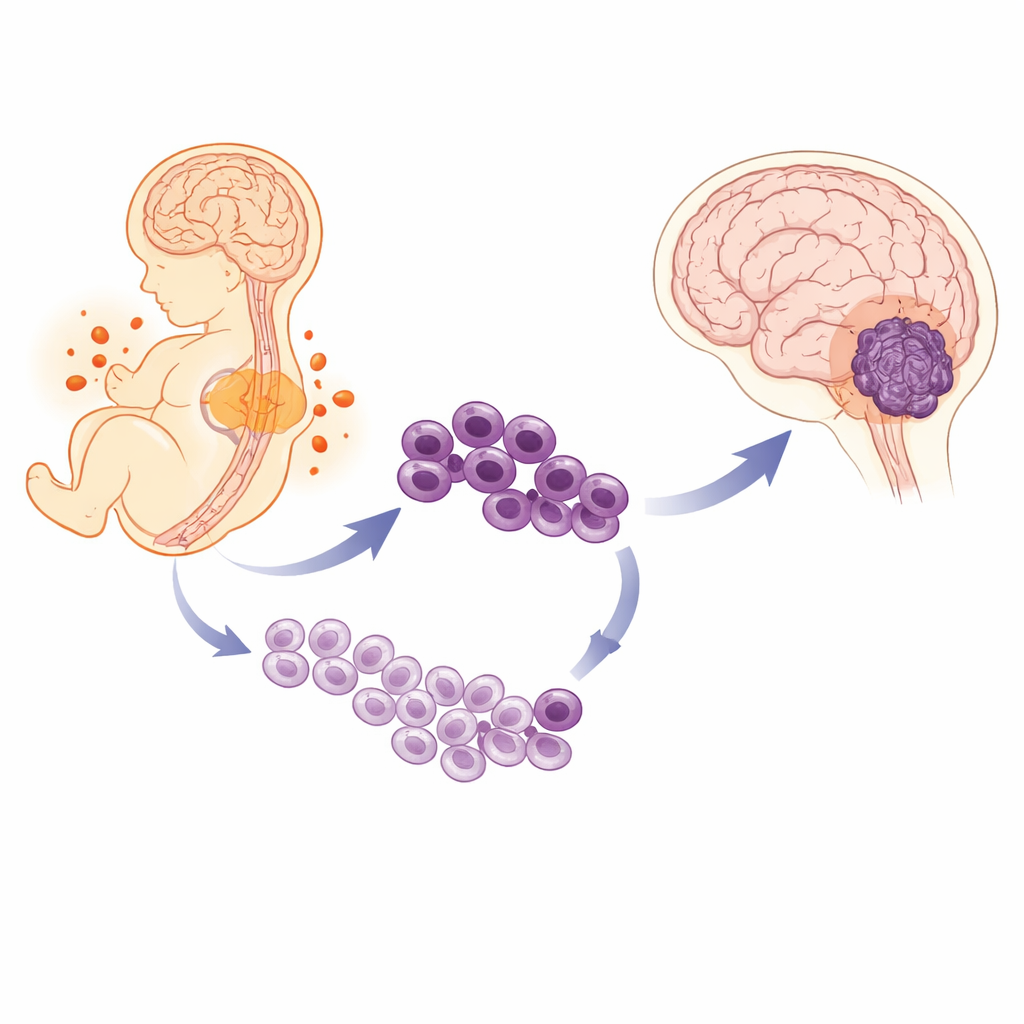
Ein kindlicher Krebs mit verborgenem Gefälle
Die Autorinnen und Autoren untersuchten zunächst große Kohorten von Kindern mit diesem Tumor und bestätigten, dass Jungen ihn nicht nur häufiger bekommen, sondern langfristig auch schlechter überleben als Mädchen, selbst bei gleicher aggressiver Behandlung. Um zu verstehen, was die Tumoren unterscheidet, nutzte das Team Einzelzell-RNA-Sequenzierung, eine Methode, die erfasst, welche Gene in tausenden Zellen einzeln aktiv sind. In Tumoren von Jungen bestand ein größerer Anteil der Zellen aus sehr unreifen „Stammzell-ähnlichen“ Zellen, während Tumoren von Mädchen mehr Zellen enthielten, die weiter in Richtung spezialisierter Gehirnzellen differenziert waren. Je stärker ein Tumor eines Jungen in diese primitiven Zellen angereichert war, desto schlechter war in der Regel das Ergebnis.
Den Tumor zurück ins sich entwickelnde Gehirn verfolgen
Da diese Tumoren bei Kleinkindern auftreten und fötalem Hirngewebe ähneln, vermuteten die Forschenden, dass etwas in der normalen Gehirnentwicklung den Boden für Krebs bereiten könnte. Sie erstellten einen detaillierten Atlas von über 400.000 Einzelzellen aus dem Hinterhirn von Mausembryonen in mehreren Entwicklungsstadien und balancierten männliche und weibliche Proben sorgfältig aus. Diese Karte zeigte, wie frühe neuronale Stammzellen allmählich zu gliogenen Vorläuferzellen werden—Zellen, die zu Stützfunktionen wie Astrozyten bestimmt sind—und dann zu reifen Gliazellen. Beim Vergleich von männlichen und weiblichen Embryonen zeigte sich, dass männliche Vorläuferzellen, insbesondere im Hinterhirn, dazu neigten, länger in einem primitiveren, schnell teilenden Zustand zu verharren, während weibliche Zellen stärkere Hinweise auf das Ausreifen in ihre Endformen zeigten.
Androgene verlangsamen die Reifung wichtiger Gehirnzellen
Um zu klären, ob dieser Unterschied von den Geschlechtschromosomen oder von Hormonen herrührt, verwendete das Team ein „Four-core genotype“-Mausmodell, das das Vorhandensein von Hoden (und damit die Produktion von Androgenen) von einem XY-Chromosomensatz trennt. Über die Genotypen hinweg war entscheidend das Vorhandensein von Hoden und Androgenen, nicht das chromosomale Geschlecht. In Embryonen mit Hoden zeigten Hinterhirn-Vorläuferzellen Genaktivitätsmuster, die mit Stammzell-Erhaltung, schneller Teilung und blockierter Differenzierung verknüpft sind. In Embryonen mit Ovarien zeigten dieselben Zelltypen eher Gene, die mit Reifung und Gliaentwicklung assoziiert sind. Viele der Gene und Kontrollschalter, die durch Androgene in normalen männlichen Embryonen verstärkt wurden, waren auch in den aggressivsten, stammzellartigen Tumorzellen von Jungen stärker aktiv, was das Verhalten des Tumors direkt mit hormongeprägten Entwicklungsprogrammen verknüpft.
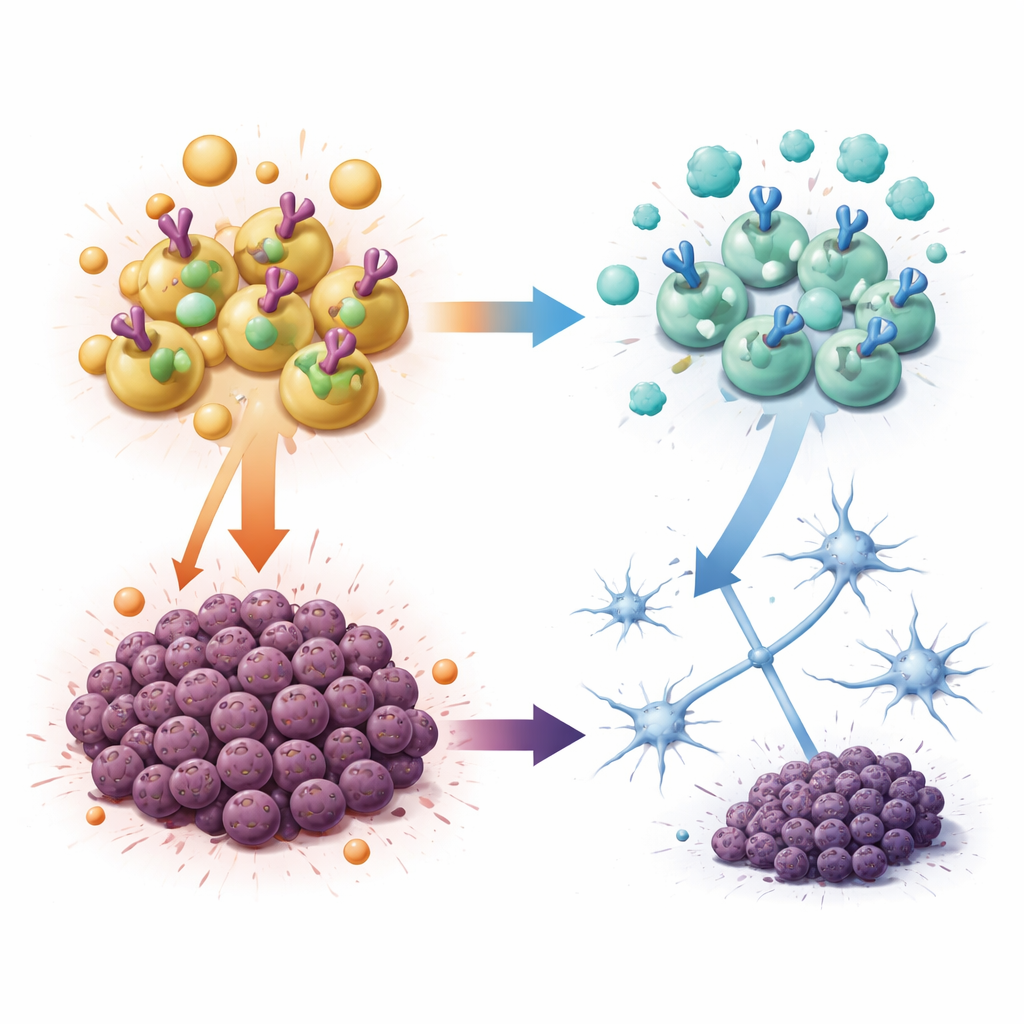
Hormone, die den Tumor nähren – und Medikamente, die ihn auszehren
Die Forschenden fragten dann, ob Androgene Tumorzellen direkt im Wachstum beeinflussen können. Im Zellkulturversuch vermehrten sich Tumorzellen sowohl von Jungen als auch von Mädchen und bildeten mehr Kolonien, wenn sie Testosteron oder sein starkes Derivat Dihydrotestosteron ausgesetzt waren, nicht jedoch bei Exposition gegenüber weiblichen Hormonen wie Östrogen oder Progesteron. Diese Tumorzellen trugen den Androgenrezeptor, ein Protein, das in den Zellkern wandert und Gene einschaltet, wenn Androgene vorhanden sind. Das Blockieren dieses Rezeptors mit Enzalutamid, einem bereits beim Prostatakarzinom eingesetzten Medikament, oder dessen Abbau mit einer experimentellen Verbindung verringerte deutlich die stammzellartige Kapazität und das Wachstum dieser Tumorzellen. Wichtig ist, dass andere pädiatrische Hirntumorzelltypen kaum auf Androgene oder androgenblockierende Medikamente reagierten, was darauf hindeutet, dass diese Verwundbarkeit spezifisch für diesen Hinterhirntumor ist.
Was das für Kinder und künftige Therapien bedeutet
Zusammengefasst stützen die Ergebnisse eine einfache, aber starke Idee: Im sich entwickelnden Hinterhirn halten Androgene bestimmte Vorläuferzellen bei männlichen Tieren länger in einem unreifen, schnell wachsenden Zustand als bei weiblichen. Dieses verlängerte Zeitfenster erhöht die Wahrscheinlichkeit, dass diese Zellen eine maligne Veränderung durchlaufen und nach der Transformation hochgradig stammzellartig und aggressiv bleiben, was erklärt, warum Jungen stärker von diesem Tumor betroffen sind. Da dieselben Hormonsignale, die die normale Entwicklung formen, auch den Krebs nähren, könnten Therapien, die die Androgen-Signalgebung blockieren—sorgfältig angepasst an Säuglinge und Kleinkinder—die erste rationale zielgerichtete Behandlung für diese verheerende Erkrankung bieten.
Zitation: Zhang, J., Ong, W., Rasnitsyn, A. et al. Androgen activity in the male embryonic hindbrain drives lethal PFA ependymoma. Nature 652, 763–773 (2026). https://doi.org/10.1038/s41586-026-10264-6
Schlüsselwörter: ependymom, androgene Signalgebung, pädiatrischer Hirntumor, Hinterhirnentwicklung, Geschlechtsunterschiede bei Krebs