Clear Sky Science · zh
经过1万代实验进化后,出芽酵母与裂殖酵母呈现平行但不同的适应路线
为什么微小的酵母能教给我们重大启示
当我们想到进化,常常会联想到化石和古老森林,而不是在塑料孔板中生长的微生物。然而通过在实验室中观察酵母细胞在数千代中如何适应,科学家们可以以快进模式重播进化。这项研究跟踪了两种相距较远的酵母近缘种,在完全相同的低氧、高糖环境中培养约1万代,提出了一个看似简单的问题:如果从相似的有机体出发并给予相同的挑战,它们会找到相同的遗传解决方案,还是各自沿着不同的道路前进?
在瓶中设置进化实验
研究人员关注的是一个广为人知的模式生物——出芽酵母,以及它较少为人熟知的近亲——裂殖酵母。这些物种共享大部分基因,但在基因组组织和生活方式上存在差异。例如,裂殖酵母高度依赖线粒体进行需氧呼吸,天然上不善于发酵;而出芽酵母则是发酵能手。研究团队在充满丰富高糖液体的小孔中培养了15个独立的裂殖酵母族群,孔盖盖着且不进行振荡——这些条件限制氧气并促进发酵。每天对培养物进行稀释,使只有一部分细胞存活并为下一轮提供种子,循环进行约1万代。研究过程中,他们冷冻保存样品、每隔1000代测序,并测量哪些族群比祖先生长更快。
相同环境,不同的进化回报
所有存活下来的裂殖酵母族群在实验条件下都比祖先更适应,表现为生长更好。但与之前在相同环境下研究的出芽酵母相比,裂殖酵母获得适应度的速度更慢。这一差异并非因为裂殖酵母在起始时更适合这些条件——事实上,起始时出芽酵母生长得更好。作者提出,出芽酵母的进化历史(包括基因组重复和长期在低氧生态位中的经验)使其拥有更多可用的“备用零件”和可调整的通路。相比之下,裂殖酵母具有更多必需基因并且更依赖呼吸,因而可供简单改变的“旋钮”更少,因此通过不同的变化组合来适应。
重接细胞处理糖与氧的线路
通过追踪突变随时间的变化,研究团队发现裂殖酵母很少依赖彻底破坏基因的粗糙手段。在出芽酵母适应中常见的使蛋白功能丧失的突变,在裂殖酵母的编码区相对稀少,并受到净化选择的筛除。相反,许多重要变化出现在调控基因何时打开或关闭的非编码DNA片段中,这与裂殖酵母基因组富含调控区是一致的。在独立的族群中,进化反复靶向了一小组与碳代谢和应激反应相关的“多次命中”基因。一个关键靶点是丙酮酸激酶基因——该酶位于糖分解的重要分叉点。围绕该基因的突变,结合另一个将碳引入线粒体的酶活性变化,有效地将碳流从呼吸转向发酵。换句话说,裂殖酵母重接其内部管线以在更少氧气的情况下生存。
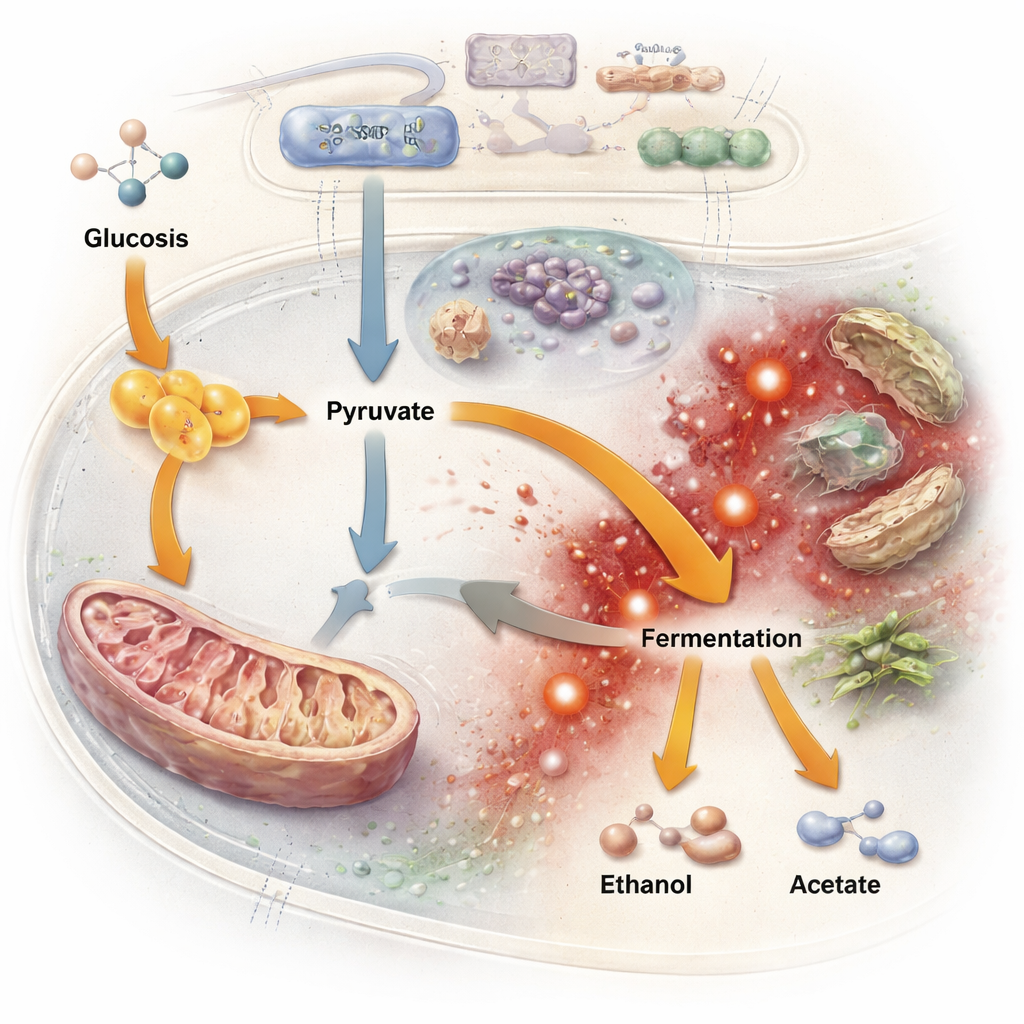
隐含代价:易碎的抗压防御
这种代谢改造伴随着代价。在低氧高糖环境中的发酵会导致乙醇、乙酸及其他副产物积累,这些物质会损伤线粒体并产生活性氧——会伤害细胞组分的高度反应性分子。当科学家用过氧化氢(一种氧化应激来源)挑战进化后的族群时,大多数比原始菌株更为敏感。在铁运输、氧化还原相关酶和一个主要的氧化应激调节因子中的遗传改变,指向保护系统的减弱。与此同时,RNA测序显示许多通路的基因活性普遍发生变化,包括关键分子的运输、脂质处理和自噬(细胞的回收系统)。值得注意的是,许多这些表达变化并非发生在本身被突变的基因上,这暗示进化常通过控制基因网络的“主开关”而非逐一微调各个基因来发挥作用。
这对我们理解进化有何启示
总体来看,研究勾勒出一种“平行但不同”的进化图景。出芽酵母与裂殖酵母,甚至与细菌等远缘微生物一样,倾向于通过重新定向碳流和调整中心代谢来应对低氧挑战。然而具体的基因、突变和副作用各不相同,受到各自基因组结构和进化历史的塑造。对于裂殖酵母而言,适应缺氧高糖环境通常意味着更依赖发酵并接受对氧化损伤更高的脆弱性。这项工作表明,要预测从微生物到癌细胞等生物在压力下将如何进化,我们必须同时考虑环境以及写入其基因组的隐性限制和历史。
引用: N’Guessan, A., Wang, V., Bakerlee, C.W. et al. Parallel but distinct adaptive routes in the budding and fission yeasts after 10,000 generations of experimental evolution. Nat Ecol Evol 10, 765–778 (2026). https://doi.org/10.1038/s41559-026-03017-1
关键词: 实验进化, 酵母适应, 代谢, 缺氧, 氧化应激