Clear Sky Science · de
Parallele, aber unterschiedliche Anpassungswege bei Spross- und Spaltpilzen nach 10.000 Generationen experimenteller Evolution
Warum winzige Hefen uns große Lektionen erteilen können
Wenn wir an Evolution denken, stellen wir uns oft Fossilien und uralte Wälder vor, nicht Mikroben in Plastikplatten. Doch indem Forscher Hefezellen über Tausende von Generationen im Labor beim Anpassen beobachten, können sie Evolution im Schnellvorlauf abspielen. Diese Studie verfolgte zwei weit entfernte Verwandte der Hefe, die unter exakt derselben sauerstoffarmen, zuckerreichen Umgebung über rund 10.000 Generationen gezüchtet wurden, um eine irreführend einfache Frage zu stellen: Wenn man mit ähnlichen Organismen startet und ihnen dieselbe Herausforderung gibt, finden sie dann dieselben genetischen Lösungen — oder treibt die Geschichte sie auf unterschiedliche Pfade?
Evolution in der Flasche ansetzen
Die Forschenden konzentrierten sich auf ein gut bekanntes Modell, die Sprosshefe, und ihren weniger bekannten Verwandten, die Spalthfe. Diese Arten teilen die Mehrheit ihrer Gene, unterscheiden sich jedoch in der Organisation ihres Genoms und in ihrer üblichen Lebensweise. Die Spalthfe verlässt sich zum Beispiel stark auf ihre Mitochondrien zur Sauerstoffatmung und ist natürlicherweise schlecht im Gären, während die Sprosshefe eine exzellente Gärfähigkeit besitzt. Das Team züchtete 15 unabhängige Populationen der Spalthfe in kleinen Vertiefungen, gefüllt mit nährstoffreichem, zuckerhaltigem Medium, unter Deckeln und ohne Schütteln — Bedingungen, die den Sauerstoff begrenzen und Gärung begünstigen. Täglich wurden die Kulturen verdünnt, sodass nur ein Bruchteil der Zellen die nächste Runde begründete; dies wiederholte sich über etwa 10.000 Generationen. Dabei wurden Proben eingefroren, alle 1.000 Generationen DNA sequenziert und gemessen, welche Populationen schneller wuchsen als ihre Vorfahren.
Gleiche Umgebung, unterschiedliche evolutionäre Gewinne
Alle überlebenden Spalthfe-Populationen wurden fitter als ihr Vorfahre, das heißt, sie wuchsen unter den experimentellen Bedingungen besser. Im Vergleich zur Sprosshefe, die in einer früheren Studie derselben Umgebung ausgesetzt war, erwarb die Spalthfe diese Fitnessgewinne jedoch langsamer. Das lag nicht daran, dass die Spalthfe ursprünglich besser an die Bedingungen angepasst gewesen wäre — tatsächlich wuchs die anfängliche Sprosshefe zu Beginn besser. Stattdessen schlagen die Autoren vor, dass die evolutionäre Vorgeschichte der Sprosshefe, einschließlich einer duplizierten Genomebene und langer Erfahrung mit sauerstoffarmen Nischen, ihr mehr genetische „Ersatzteile“ und Wege zum Feinjustieren bietet. Die Spalthfe mit mehr essentiellen Genen und einer stärkeren Abhängigkeit von der Atmung hat weniger einfache Stellschrauben und passt sich daher durch eine andere Mischung von Veränderungen an.
Umschaltung, wie Zellen mit Zucker und Sauerstoff umgehen
Durch das Verfolgen von Mutationen über die Zeit fanden die Forschenden heraus, dass die Spalthfe nur selten auf das grobe Mittel zurückgriff, Gene vollständig zu zerstören. Loss-of-function-Mutationen, die Proteine stören — in adaptierender Sprosshefe häufig — waren in den kodierenden Regionen der Spalthfe vergleichsweise selten und wurden durch reinigende Selektion ausgesiebt. Stattdessen traten viele wichtige Veränderungen in nicht-kodierenden DNA-Abschnitten auf, die steuern, wann Gene an- oder ausgeschaltet werden, was mit dem reichhaltigen Vorkommen regulatorischer Regionen im Genom der Spalthfe übereinstimmt. Über unabhängige Populationen hinweg traf die Evolution wiederholt eine kleine Gruppe von „Multi‑Hit“-Genen, die mit Kohlenstoffstoffwechsel und Stressantworten verknüpft sind. Ein zentrales Ziel war das Gen für Pyruvatkinase, ein Enzym an einem entscheidenden Verzweigungspunkt beim Zuckerabbau. Mutationen rund um dieses Gen, kombiniert mit veränderter Aktivität eines anderen Enzyms, das Kohlenstoff in die Mitochondrien leitet, verschoben den Kohlenstofffluss effektiv weg von der Atmung hin zur Gärung. Anders ausgedrückt: Die Spalthfe verkabelte ihre interne „Rohrleitung“ um, um mit weniger Sauerstoff auszukommen.
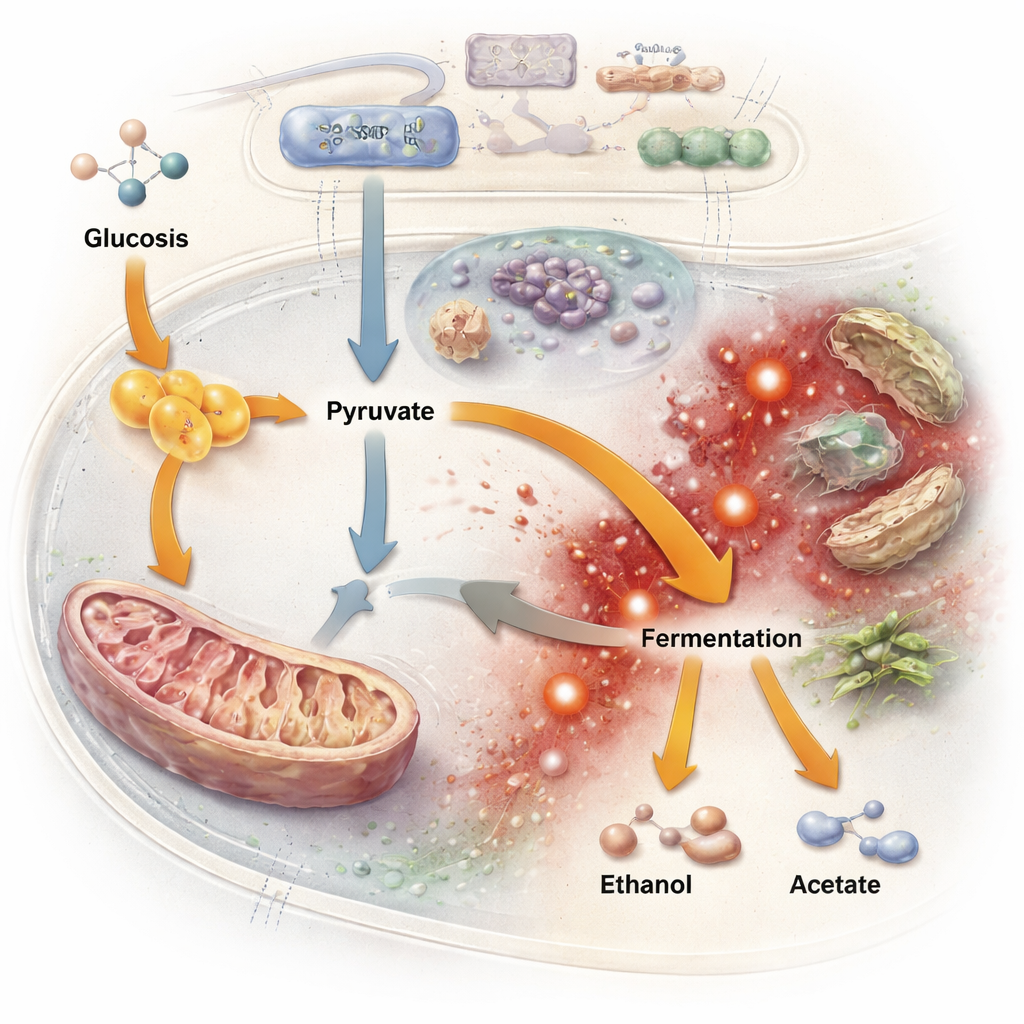
Der versteckte Preis: fragile Abwehr gegen Stress
Diese Stoffwechsel-Umstellung hatte ihren Preis. Gärung in einer sauerstoffarmen, zuckerreichen Welt kann zur Anreicherung von Ethanol, Acetat und anderen Nebenprodukten führen, die Mitochondrien schädigen und reaktive Sauerstoffspezies erzeugen — hochreaktive Moleküle, die zelluläre Komponenten schädigen. Als die Wissenschaftler die evolvierten Populationen mit Wasserstoffperoxid, einer Quelle oxidativen Stresses, herausforderten, waren die meisten empfindlicher als der ursprüngliche Stamm. Genetische Veränderungen in Eisenstoffwechsel, redoxbezogenen Enzymen und einem wichtigen Regulator der oxidativen Stressantwort deuteten auf geschwächte Schutzsysteme hin. Gleichzeitig zeigte die RNA-Sequenzierung weitreichende Verschiebungen in der Genaktivität über viele Wege hinweg, einschließlich Transport wichtiger Moleküle, Lipidverarbeitung und Autophagie (das Recycling-System der Zelle). Auffällig war, dass viele dieser Expressionsänderungen in Genen auftraten, die selbst nicht mutiert waren, was darauf hindeutet, dass Evolution häufig über „Hauptschalter“ wirkte, die Netzwerke von Genen steuern, statt jedes einzelne Gen direkt feinzujustieren.
Was uns das allgemein über Evolution sagt
Zusammen zeichnen die Ergebnisse ein Bild von „parallel, aber unterschiedlich“ verlaufender Evolution. Sowohl Spross- als auch Spalthfe — und sogar entfernte Mikroben wie Bakterien — neigen dazu, sauerstoffarme Herausforderungen zu lösen, indem sie den Kohlenstofffluss umleiten und den zentralen Stoffwechsel anpassen. Doch die genauen Gene, Mutationen und Nebenwirkungen unterscheiden sich und werden von der genetischen Architektur und der evolutionären Vorgeschichte jeder Art geprägt. Für die Spalthfe bedeutet die Anpassung an eine hypoxische, zuckerreiche Umgebung häufig eine stärkere Abhängigkeit von Gärung und die Akzeptanz einer erhöhten Verwundbarkeit gegenüber oxidativen Schäden. Diese Arbeit legt nahe, dass wir, um vorherzusagen, wie Organismen — von Mikroben bis zu Tumorzellen — unter Stress evolvieren werden, nicht nur die Umwelt, sondern auch die verborgenen Beschränkungen und Geschichten in ihren Genomen berücksichtigen müssen.
Zitation: N’Guessan, A., Wang, V., Bakerlee, C.W. et al. Parallel but distinct adaptive routes in the budding and fission yeasts after 10,000 generations of experimental evolution. Nat Ecol Evol 10, 765–778 (2026). https://doi.org/10.1038/s41559-026-03017-1
Schlüsselwörter: experimentelle Evolution, Hefe-Anpassung, Stoffwechsel, Hypoxie, oxidativer Stress