Clear Sky Science · zh
淋球菌外膜囊泡疫苗:细菌群体生物学、临床试验、免疫谱系与疫苗设计
为何这种性传播感染重要
淋病是全球最常见的性传播感染之一,且随着致病细菌对抗生素产生耐药性,治疗变得越来越困难。本文回顾了一条有前景的新防线:基于相关细菌天然脱落的小型囊泡构建的疫苗。文章解释了淋病菌如何躲避免疫系统、为何某些脑膜炎疫苗出人意料地能提供部分保护,以及科学家如何重新设计这些基于囊泡的疫苗以更直接地针对淋病。
一种变形的病原体,智胜免疫系统
罪魁祸首Neisseria gonorrhoeae数千年来一直在适应人类。它与亲缘菌种乃至其他物种交换DNA,使其能迅速获得抗生素耐药性。表面上的关键分子不断改变外观或开关表达,使病原体能够躲避免疫攻击并重新感染同一患者。用现代基因工具绘制这种多样性显示,今天的淋病群体由许多相关但不同的谱系构成。这对疫苗很重要:基于仅几株实验室菌株的疫苗可能无法覆盖现实感染中广泛存在的变异。
病原体如何将我们的防御变成它的优势
我们对抗细菌的第一道防线包括在血液中的穿孔补体蛋白和协调长期防护的免疫细胞。淋病已经学会劫持这两者。它修饰表面以招募人类“刹车”分子,关闭穿孔系统,并产生引发可结合但不杀灭的抗体的蛋白,阻碍更有用的抗体发挥作用。在生殖道等黏膜表面,它甚至可以利用补体蛋白作为进入细胞的桥梁。在组织内,它将免疫反应引向以Th17型(短暂的炎症反应)为主的模式,同时抑制形成免疫记忆的Th1和Th2反应。因此,自然感染通常不会留下持久的保护性免疫。
来自脑膜炎疫苗的意外帮助
一个意外线索来自新西兰,当地为控制B型脑膜炎暴发使用的一种疫苗后来与约三分之一的淋病病例减少相关联。该疫苗以及一种更新的疫苗4CMenB都含有外膜囊泡(OMV)——从脑膜炎菌表面掐下来的纳米级小囊泡——以及一些额外的蛋白。由于淋病菌和脑膜炎菌是近亲,它们的OMV携带重叠的表面靶点集合。随后在多个国家的随访研究以及小鼠实验证实,这些脑膜炎疫苗能诱导识别多种淋病蛋白的抗体并缩短感染持续时间,尽管这种保护只是部分性的,并且在反复暴露的人群中似乎较弱。
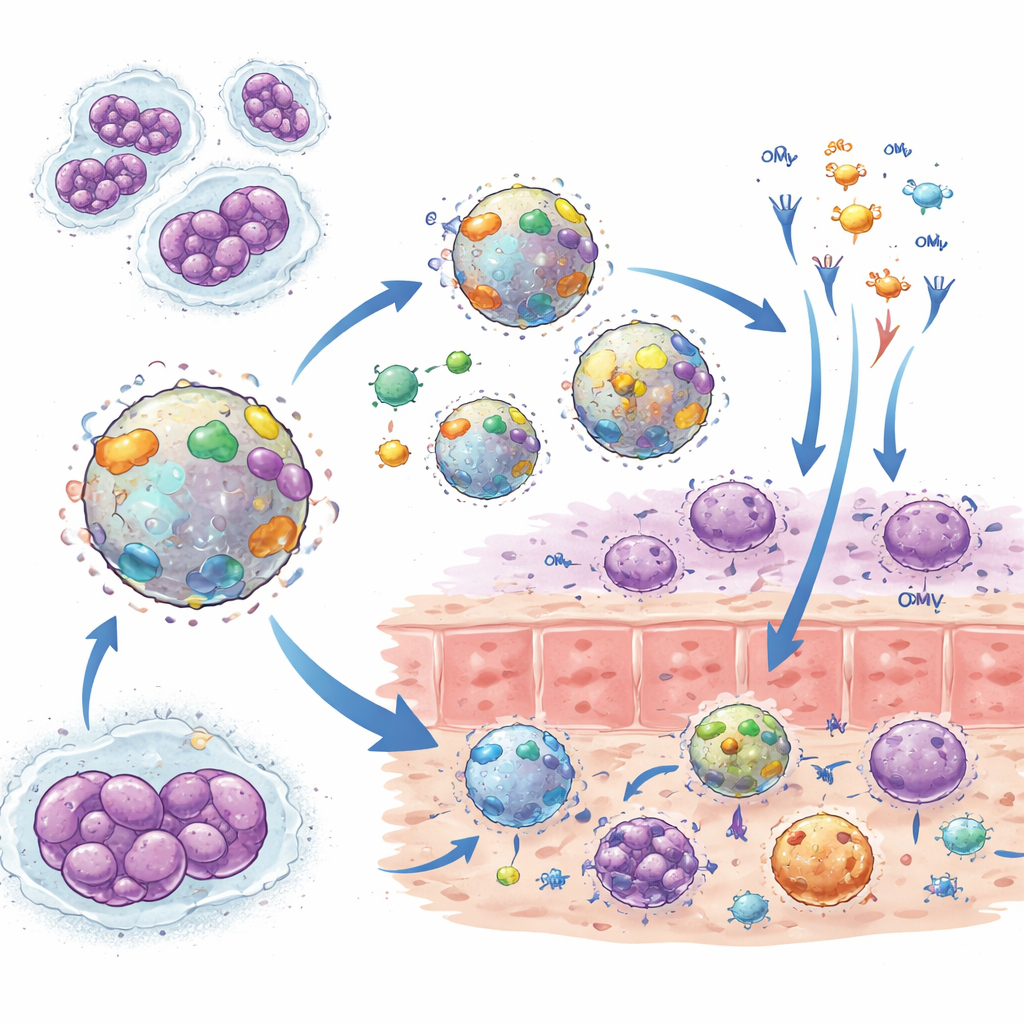
设计更聪明的基于囊泡的疫苗
受这些交叉保护线索的鼓舞,研究者现在正致力于为淋病量身定制的OMV疫苗。一种策略是继续使用脑膜炎菌,但去除一些高度可变或无益的成分,或减弱其表面的毒性部分,以聚焦免疫反应并提高安全性。另一种策略使用直接来自淋病菌株的OMV,结合增强免疫的佐剂,如缓慢释放促Th1信号(细胞因子IL-12)的小颗粒,或通过鼻腔或阴道等途径给药以刺激强烈的局部抗体反应。基因改造也可以替换更有用的蛋白版本或去除那些抑制免疫的成分,重塑囊泡使其呈现更丰富、更具保护性的靶点集合。
抗击淋病的未来方向
作者总结道,基于OMV的疫苗仍是随着抗生素效力下降、控制淋病的一条最有希望的途径之一。然而,要将部分保护转化为可靠的预防,需要谨慎选择用于疫苗的细菌菌株、深入目录化哪些囊泡成分最易被免疫系统识别,并对细菌进行重新工程,使其囊泡不再携带抑制免疫的伎俩。未来的临床研究,特别是在高危人群和两性人群中的研究,对确定哪些抗体和细胞反应真正能预防感染至关重要。如果成功,这些基于理性设计的OMV疫苗可大幅降低全球淋病及其并发症的负担,保护数百万人的生育力与性健康。
引用: Gu, Z., Unitt, A., Harrison, O.B. et al. Gonococcal outer membrane vesicle vaccines: bacterial population biology, clinical trials, immune profiling, and vaccine design. npj Vaccines 11, 85 (2026). https://doi.org/10.1038/s41541-026-01410-2
关键词: 淋病疫苗, 外膜囊泡, 抗微生物耐药性, 淋病奈瑟氏菌, 性传播感染